Clear Sky Science · pl
Aktywatory NRF2 i inhibitor eksportu jądrowego, selinexor, ograniczają koronawirusy, celując w sieć obejmującą ACE2, TMPRSS2 i XPO1 poprzez mechanizm niezależny od NRF2
Leki, które pomagają komórkom mówić „nie” koronawirusom
Większość dostępnych dziś terapii przeciw koronawirusom atakuje sam wirus. Ale wirusy łatwo się zmieniają, a nowe warianty szybko mogą osłabić skuteczność tych leków. W tym badaniu zbadano inną strategię: uczynienie naszych własnych komórek mniej przyjaznymi dla niebezpiecznych koronawirusów, takich jak SARS-CoV-2, oraz dla łagodniejszych sezonowych szczepów. Poprzez modyfikację sposobu, w jaki komórki obsługują kilka kluczowych białek-bramek, badacze pokazują, że istniejące małe cząsteczki mogą wyraźnie zmniejszyć zakażenie w modelach laboratoryjnych, i robią to w mechanizmie, który nie opiera się na znanej ścieżce przeciwwirusowej, z którą te związki były kojarzone.
Nowe spojrzenie na obronę przed koronawirusami
Zespół skupił się na związkach znanych z aktywowania komórkowego programu ochronnego kontrolowanego przez białko NRF2. Związki te — 4-oktylo itakonian (4OI), bardoksolon (BARD) i sulforafan (SFN) — przetestowano wraz z selinexorem (SEL), lekiem blokującym białko transportowe XPO1, które pomaga przenosić inne białka poza jądro komórkowe. W modelach komórek płucnych i nerkowych wszystkie cztery leki obniżały poziomy SARS-CoV-2 bez uszkadzania komórek. Działały również przeciw kilku wariantom budzącym niepokój. Co zaskakujące, po genetycznym usunięciu NRF2 wirusy replikowały się lepiej, co dowodzi, że NRF2 ma naturalnie ochronną rolę — jednak leki nadal były skuteczne, co pokazuje, że ich przeciwwirusowa siła pochodzi z innej drogi. 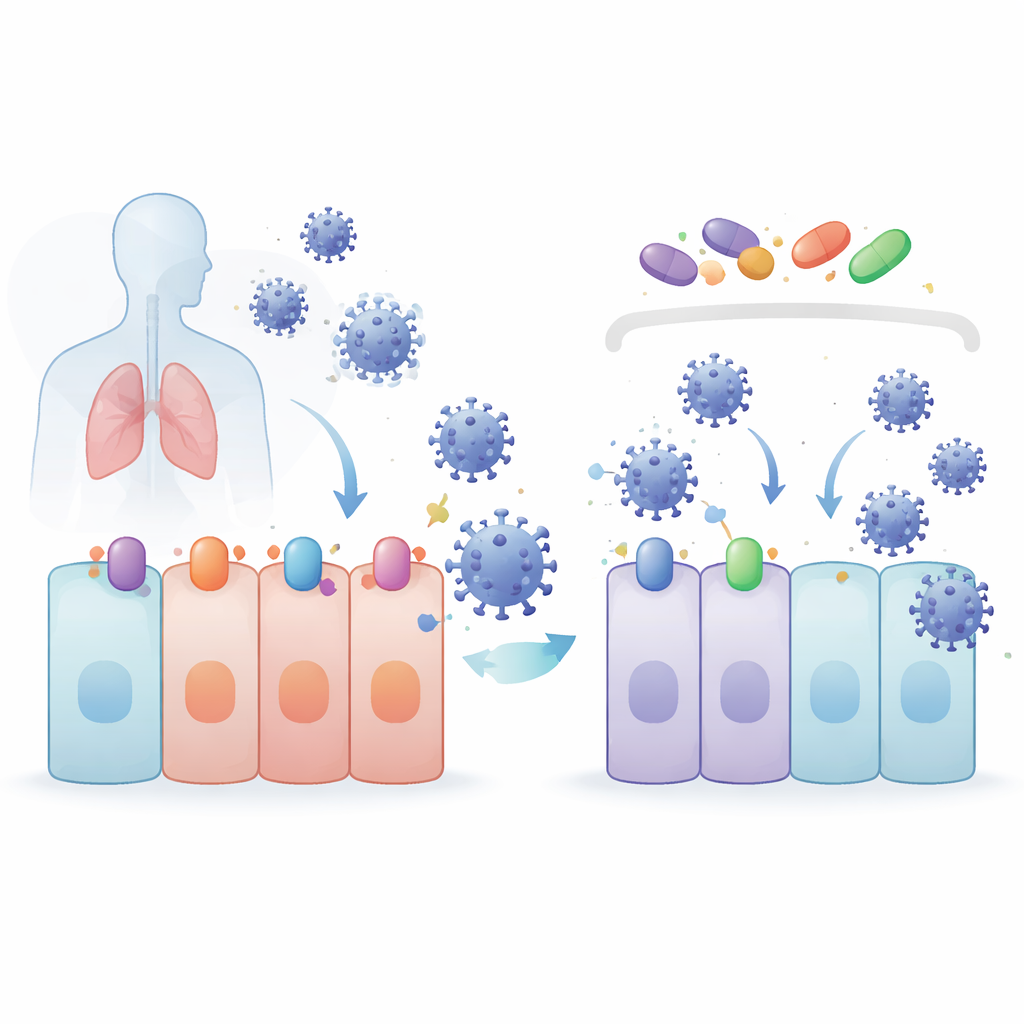
Zamykanie wirusowych drzwi wejściowych
Koronawirusy rozpoczynają zakażenie, przyczepiając się do receptorów na powierzchni komórki. Dla SARS-CoV-2 i jego bliskich krewnych głównymi drzwiami jest ACE2, wspierane przez enzym tnący zwany TMPRSS2. Białko eksportowe XPO1 także zdaje się wspomagać zakażenie. Badacze stwierdzili, że 4OI, BARD, SFN i SEL wszystkie obniżały ilości ACE2, TMPRSS2 i XPO1 w ludzkich komórkach płucnych. 4OI i SEL były szczególnie efektywne, gdy były obecne przed zakażeniem, i blokowały wejście cząstek podobnych do wirusa pokrytych kolcem koronawirusa. Innymi słowy, leki te nie tylko spowalniają wirusa po jego wejściu — pomagają usunąć zamki i klamki, których wirus potrzebuje, by w pierwszej kolejności otworzyć drzwi.
Jak komórki rozmontowują kluczowe pomocniki wirusa
Wnikliwsze badania wykazały, że 4OI przyspiesza rozkład białka ACE2. W normalnych warunkach ACE2 utrzymywało się przez wiele godzin; po dodaniu 4OI znikało z powierzchni komórkowej w ułamku tego czasu. Ten rozpad wymagał działania dwóch komórkowych „oznaczaczy”, NEDD4L i MDM2, które przyłączają do białek molekularne flagi „do usunięcia”. Zablokowanie tych oznaczaczy osłabiało zdolność 4OI do eliminacji ACE2. Co zaskakujące, zwykły mechanizm rozkładu białek przez proteasom nie był główną drogą. Zamiast tego ACE2 było kierowane do systemu recyklingu i utylizacji komórkowej — lizosomu. Leki te także obniżały aktywność genową dla ACE2 i XPO1, częściowo poprzez zmniejszenie aktywacji STAT3, białka, które normalnie zwiększa odczyt genu ACE2. 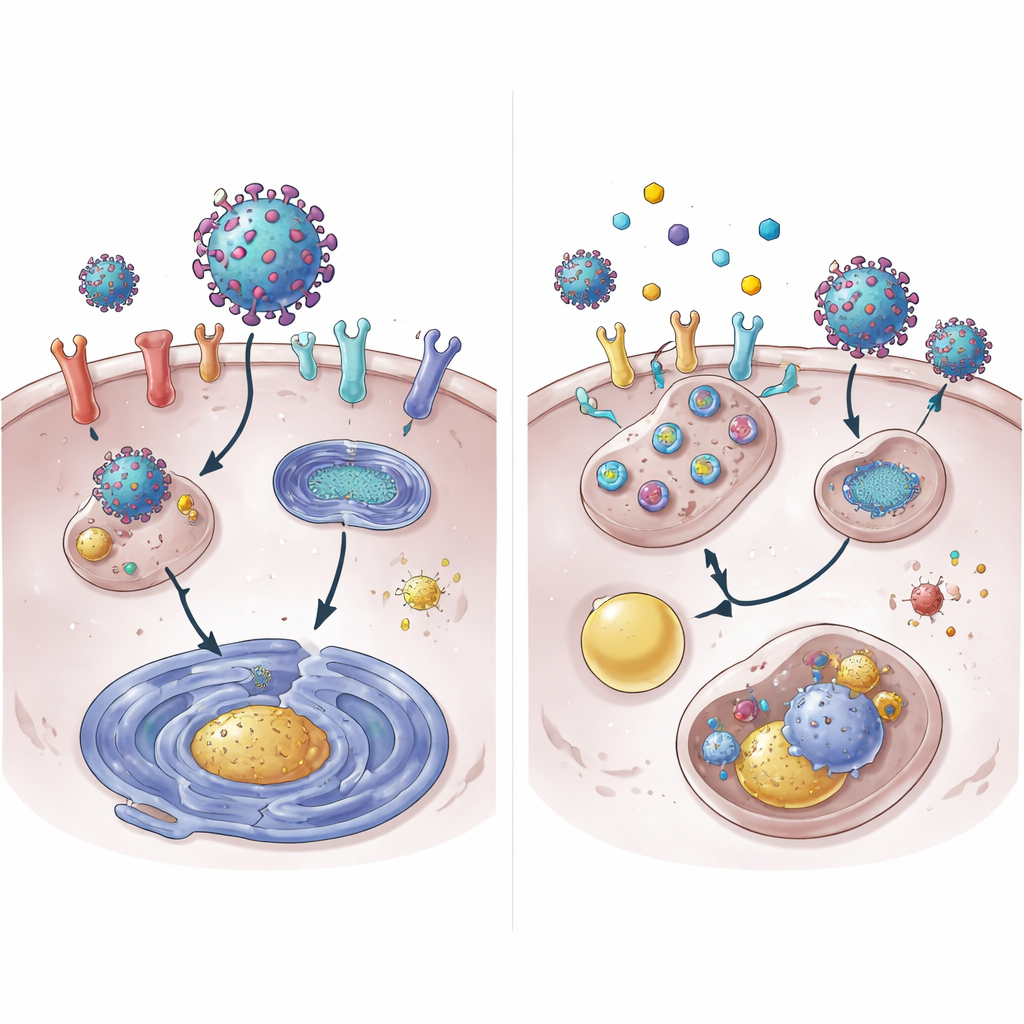
Koronawirusy sezonowe i związek z XPO1
Następnie naukowcy zwrócili się ku hCoV-229E, sezonowemu koronawirusowi, który zwykle powoduje łagodne przeziębienia, ale może być niebezpieczny u osób z osłabionym układem odpornościowym. Używając zmodyfikowanych wirusów, które świecą podczas replikacji, wykazali, że wszystkie cztery związki silnie hamowały 229E w komórkach płucnych i naczyń krwionośnych, nawet gdy NRF2 był nieobecny. W przeciwieństwie do SARS-CoV-2, ten wirus używa innego receptora, ANPEP, którego leki nie zmieniały. Zamiast tego ich efekt korelował blisko z tym, jak mocno obniżały XPO1. Wyciszenie XPO1 samo w sobie wyraźnie zmniejszyło replikację 229E, a efekt selinexoru niemal zniknął w komórkach o niskim poziomie XPO1. To porządkowanie — SEL najbardziej zależny od XPO1, BARD najmniej — sugeruje, że każdy związek ma nieco inny zestaw celów, z XPO1 jako centralnym węzłem dla wielu ich działań przeciwwirusowych.
Co to może znaczyć dla przyszłych terapii
Dla osób niebędących specjalistami kluczowa wiadomość jest taka, że można walczyć z koronawirusami nie tylko poprzez atakowanie wirusa, lecz także delikatnie przebudowując nasze własne komórki, aby były trudniejsze do zakażenia. W hodowlach komórek ludzkich zbadane związki pozbawiały istotnych miejsc dokujących i pomocniczych szlaków, od których zależą SARS-CoV-2 i powszechny wirus przeziębienia, i robiły to w dużej mierze niezależnie od samej ścieżki NRF2, która początkowo wzbudziła zainteresowanie. Choć wyniki te są nadal przedkliniczne i nie przekładają się bezpośrednio na leki, wskazują obiecującą drogę: substancje, które jednocześnie ograniczają wejście wirusa, łagodzą szkodliwy stan zapalny i chronią tkanki, celując w wspólną sieć białek gospodarza, takich jak ACE2, TMPRSS2 i XPO1.
Cytowanie: Waqas, F.H., Silva da Costa, L., Zapatero-Belinchón, F.J. et al. NRF2 activators and the inhibitor of nuclear export, selinexor, restrict coronaviruses by targeting a network involving ACE2, TMPRSS2, and XPO1 through an NRF2-independent mechanism. Commun Biol 9, 384 (2026). https://doi.org/10.1038/s42003-026-09724-6
Słowa kluczowe: leki ukierunkowane na gospodarza, wejście koronawirusa, ACE2 i TMPRSS2, aktywatory NRF2, inhibicja XPO1