Clear Sky Science · pl
Dwustopniowa strategia zależna od aktyny umożliwia Campylobacter jejuni promowanie agregacji mitochondriów i homeostazy żelaza dla przeżycia i przetrwania wewnątrzkomórkowego
Dlaczego ta drobna walka wewnątrz komórek ma znaczenie
Zatrucia pokarmowe po niedogotowanym kurczaku często przypisuje się bakteriom Campylobacter jejuni. Większość osób dochodzi do zdrowia, ale ten mikroorganizm zaskakująco dobrze przetrzymuje w różnych środowiskach, co ułatwia mu rozprzestrzenianie się od gospodarstwa do stołu. W badaniu sprawdzono, co się dzieje, gdy bakteria ukrywa się wewnątrz wolnożyjącej ameby — powszechnego mikroorganizmu słodkowodnego — i odkryto zadziwiająco wyrafinowany trik przetrwania polegający na przekształcaniu wewnętrznego szkieletu komórkowego, grupowaniu „baterii” energetycznych zwanych mitochondriami oraz kontrolowaniu żelaza i reaktywnej chemii tlenowej. Zrozumienie tej ukrytej fazy cyklu życiowego może wskazać nowe sposoby ograniczania zakażeń zanim bakteria trafi do ludzi.
Mikrob, który szkoli się w amebach
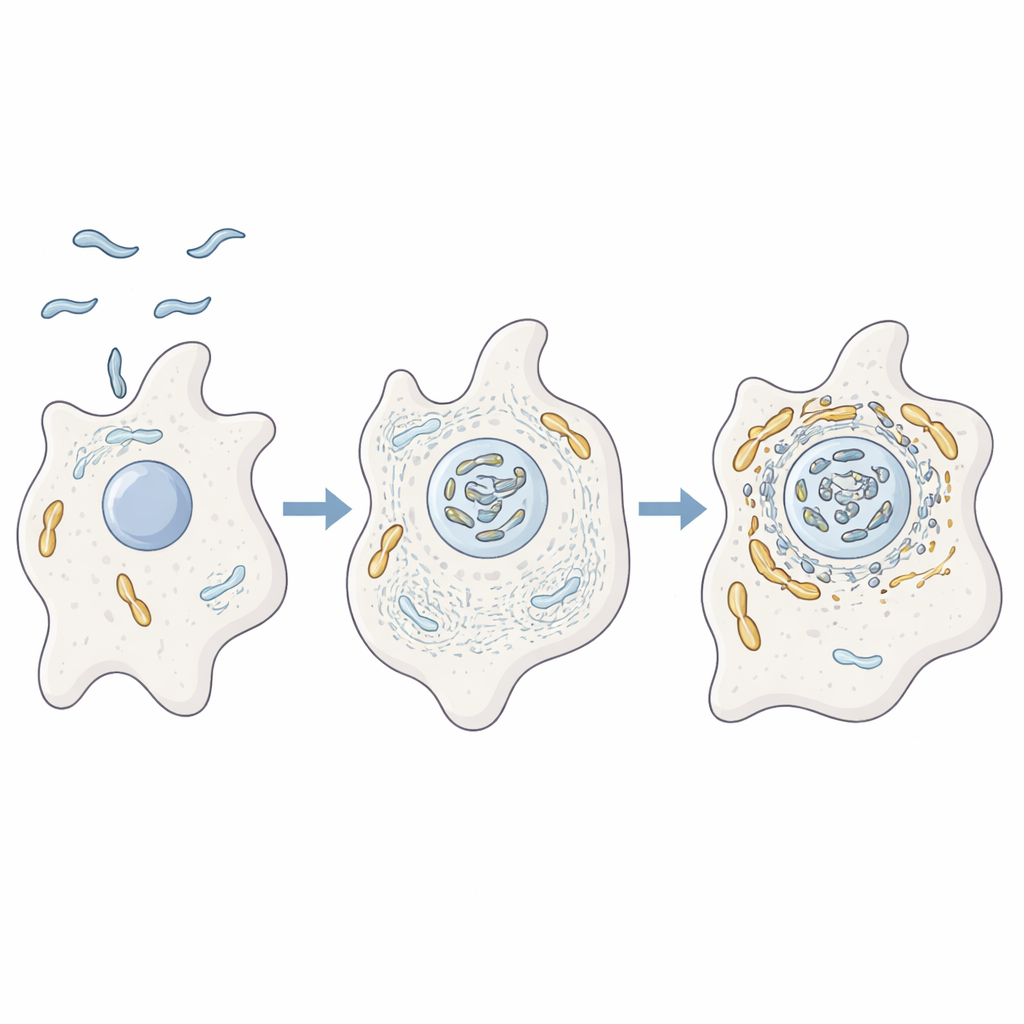
Autorzy badania analizowali zachowanie C. jejuni wewnątrz ameby Acanthamoeba castellanii, jednokomórkowego organizmu żyjącego w glebie i wodzie. Te ameeby działają jak pole treningowe dla wielu chorobotwórczych bakterii, oferując ochronę przed trudnymi warunkami i środkami dezynfekcyjnymi. Dzięki zaawansowanej analizie białek, mikroskopii i mutantom genetycznym badacze wykazali, że gdy C. jejuni zakaża ameby, znajduje się w bliskim sąsiedztwie mitochondriów gospodarza. Równocześnie wewnętrzne rusztowanie komórkowe złożone z aktyny oraz białka regulujące kształt i ruch komórki są silnie skoncentrowane w pobliżu tych mitochondriów, co sugeruje, że bakteria aktywnie przearanżowuje wewnętrzną architekturę gospodarza.
Wygięcie szkieletu komórkowego, by przesunąć „baterie”
Aby sprawdzić, czy aktyna rzeczywiście napędza tę interakcję, zespół zablokował tworzenie się filamentów aktynowych lub ich rozgałęzianie się w sieci. W tych warunkach mitochondria przestały się gromadzić w pobliżu bakterii i pozostały rozproszone, a przeżywalność bakterii spadła. Następnie skupili się na dwóch bakteryjnych pomocnikach, CiaD i CiaI, które są wstrzykiwane do komórek gospodarza przez wici bakterii — ogoniasty organellum. Okazało się, że CiaD stymuluje wzrost aktyny i sprzyja powstawaniu kolczastych wypustek na powierzchni ameby, pomagając komórce pochwycić bakterie. Po wejściu do środka mitochondria gromadziły się wokół przegrody bakteryjnej w sposób zależny od aktyny, umieszczając bakterię w uprzywilejowanej strefie bogatej w maszynerię energetyczną gospodarza.
Cząsteczkowy przełącznik przebudowujący mitochondria
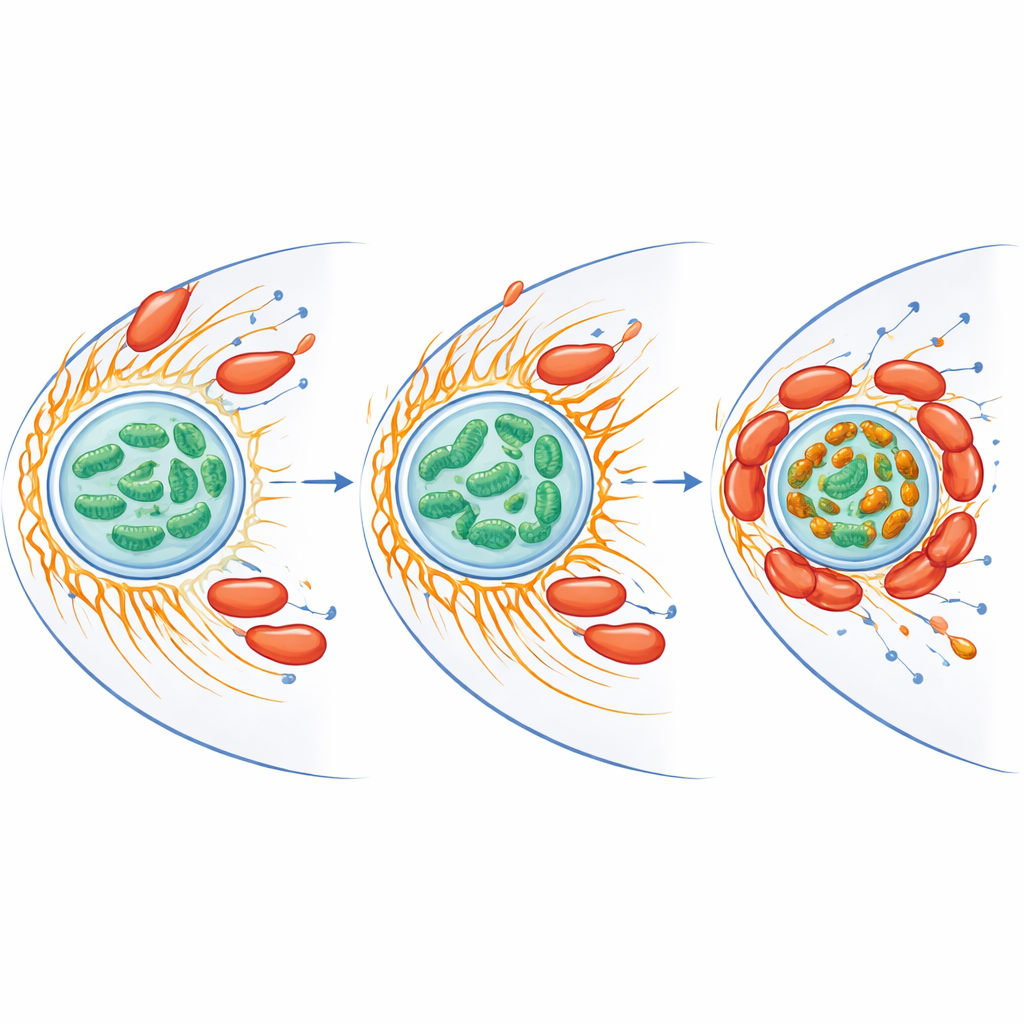
Podczas gdy CiaD jest kluczowy dla wejścia, CiaI kontroluje to, co dzieje się później. Gdy badacze usunęli gen dla CiaI, C. jejuni przestało wywoływać silne skupianie mitochondriów i słabo przeżywało wewnątrz ameb. Dodanie oczyszczonego CiaI przyłączonego do małych kulek, bez żywych bakterii, wystarczyło, by pobliskie mitochondria zaczęły się łączyć i tworzyć skupiska oraz lokalnie usuwać aktynę. Testy biochemiczne wykazały, że CiaI wiąże cząsteczki przenoszące energię w sposób kooperatywny, zachowując się jak przełącznik molekularny, który może włączać lub wyłączać swoją aktywność w zależności od warunków wewnątrz gospodarza. Autorzy proponują, że po wzroście aktyny napędzanym przez CiaD, CiaI powoduje lokalny rozpad aktyny i przebudowuje sieć mitochondrialną w gęste agregaty otaczające przegrody zawierające bakterie.
Przeprogramowanie żelaza i stresu wewnątrz komórki gospodarza
Mitochondria robią więcej niż produkują energię — zajmują się też żelazem i wytwarzają reaktywne formy tlenu, chemicznie agresywne postacie tlenu, które mogą zabijać drobnoustroje. Badacze stwierdzili, że zakażenie zmniejsza ogólną ilość wolnego żelaza w mitochondriach, ale jednocześnie tworzy jasne, bogate w żelazo skupiska tam, gdzie mitochondria agregowały wokół bakterii. Białka zaangażowane w obrót żelaza i obronę przed stresem oksydacyjnym wzrosły zarówno w gospodarzu, jak i w bakterii. Gdy zespół usunął wolne żelazo za pomocą związku chelatującego, falowy wzrost reaktywnych form tlenu w amebie osłabł, a przeżywalność C. jejuni znacząco wzrosła. Mitochondria w zakażonych komórkach wykazywały także wyższy potencjał błonowy, oznakę zwiększonej aktywności, co sugeruje, że bakteria skłania „baterie” gospodarza do stanu sprzyjającego jej przetrwaniu przy jednoczesnym ograniczeniu szkodliwej chemii tlenowej.
Co to oznacza dla bezpieczeństwa żywności i zakażeń
Podsumowując, wyniki wspierają dwustopniową strategię: najpierw CiaD stymuluje wzrost aktyny, by pomóc bakterii wejść do ameby i przyciągnąć mitochondria w stronę miejsca wejścia; następnie CiaI lokalnie rozpada aktynę i przebudowuje mitochondria w bogate w żelazo skupiska owinięte wokół przegrody bakteryjnej, jednocześnie osłabiając oksydacyjne mechanizmy obronne gospodarza. To precyzyjne sterowanie kształtem komórki, wykorzystaniem energii i równowagą metali pomaga C. jejuni przetrwać wewnątrz ameb i prawdopodobnie przyczynia się do jego zdolności do utrzymywania się w środowisku i późniejszego zakażania ludzi. Ujawnienie kluczowych graczy w tej mikroskopijnej szarpaninie wskazuje na nowe cele — takie jak białka Cia, kontakty aktyna–mitochondrium czy szlaki gospodarowania żelazem — które można by zaburzyć, aby zmniejszyć zanieczyszczenie i choroby.
Cytowanie: Nasher, F., Wren, B.W. A two-step actin-mediated strategy enables Campylobacter jejuni to promote mitochondrial aggregation and iron homeostasis, for intracellular survival and persistence. Commun Biol 9, 431 (2026). https://doi.org/10.1038/s42003-026-09713-9
Słowa kluczowe: Campylobacter, ameby, mitochondria, cytoszkielet aktynowy, homeostaza żelaza