Clear Sky Science · pl
Wielowarstwowa regulacja receptorów kainainowych GluK3 jest pośredniczona przez podjednostki Neto i cynk
Dlaczego małe przełączniki w mózgu mają znaczenie
Każda myśl, wspomnienie i nastrój w mózgu zależy od mikroskopijnych przełączników, które pozwalają na przepływ naładowanych cząstek do i z komórek nerwowych. W tym badaniu skupiono się na jednym z takich przełączników — mało znanym receptorze o nazwie GluK3. Odkrywając, jak białka partnerskie i jony cynku precyzyjnie modulują zachowanie GluK3, praca dostarcza wskazówek, jak obwody mózgowe utrzymują równowagę — i jak ta równowaga może się przechylić w zaburzeniach takich jak padaczka, depresja czy schizofrenia.
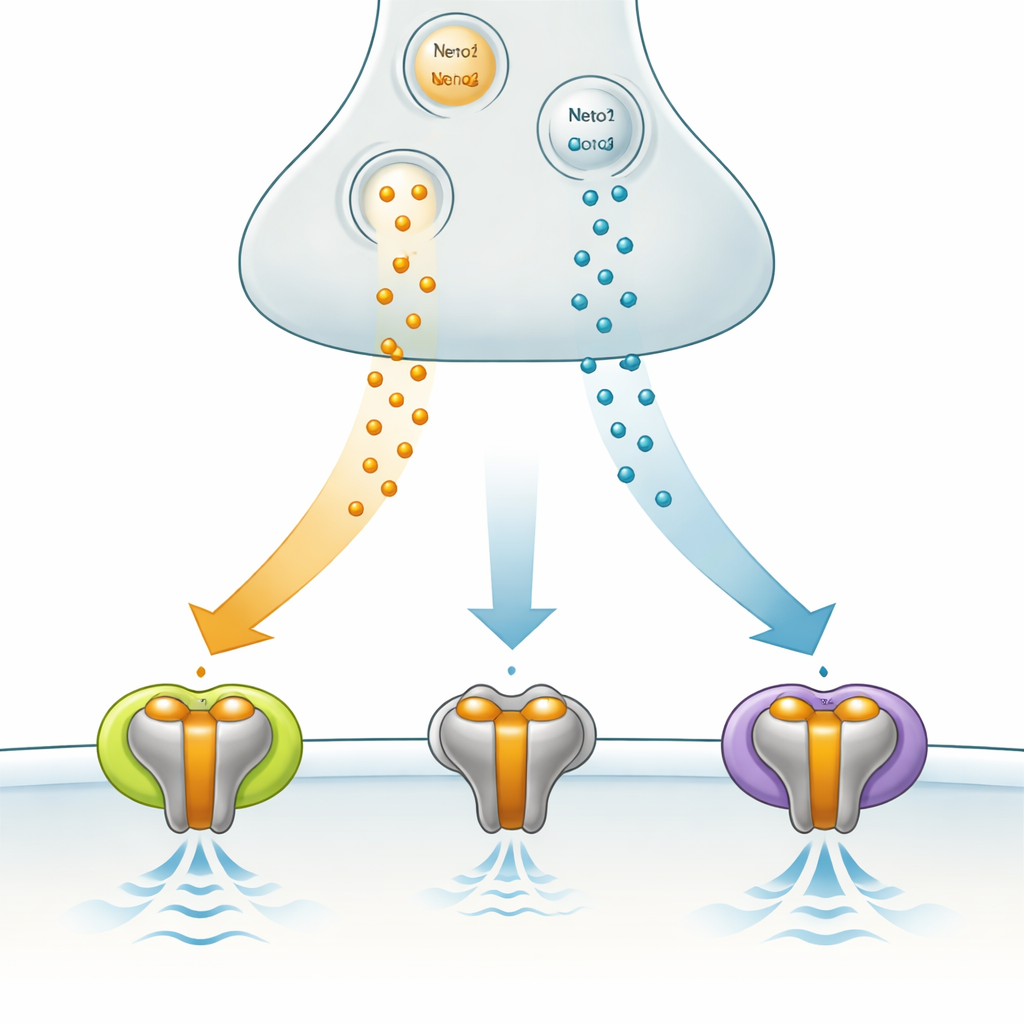
Specjalizowana bramka sygnałowa w mózgu
GluK3 należy do rodziny receptorów kainainowych, będącej częścią większej grupy receptorów glutaminianowych, które pośredniczą w szybkiej komunikacji między neuronami. W odróżnieniu od niektórych swoich krewnych, GluK3 nie włącza ani nie wyłącza sygnałów w sposób trywialny; działa raczej jak filtr, który najlepiej odpowiada na krótkie, silne impulsy przekaźnika chemicznego — glutaminianu. Jest skoncentrowany w obszarach mózgu takich jak hipokamp, kluczowy dla pamięci i kształtowania rytmów sieci, a zmiany w funkcji GluK3 powiązano z zachowaniami związanymi z lękiem. Te cechy czynią GluK3 obiecującym, choć wciąż słabo poznanym, celem do modulowania aktywności mózgu w zdrowiu i chorobie.
Białka pomocnicze, które pociągają za sznurki
Zespół badał, jak dwa białka pomocnicze, Neto1 i Neto2, zmieniają zachowanie GluK3 w ludzkich komórkach zaprojektowanych do produkcji tych składników. Oba białka spowalniały tempo, w jakim GluK3 przechodzi w stan wyłączenia po aktywacji, i oba zmniejszały naturalną formę wewnętrznego zablokowania, która normalnie ogranicza przepływ prądu. Jednak miały przeciwne efekty na szybkość, z jaką GluK3 może zostać ponownie wykorzystany. W obecności Neto1 receptory szybko odzyskiwały gotowość, reagując na szybkie, powtarzane sygnały. W obecności Neto2 odzyskiwanie było znacznie wolniejsze, sprzyjając integracji sygnałów w dłuższych odstępach czasu. W istocie, poprzez wybór różnych białek pomocniczych, synapsa może zdecydować, czy GluK3 działa jak detektor szybkich impulsów, czy jako wolniejszy sensor uśredniający.
Cynk jako druga warstwa kontroli
Wiele zakończeń nerwowych uwalniających glutaminian jednocześnie uwalnia cynk, który może wiązać się z receptorami i zmieniać ich działanie. Wcześniejsze badania wykazały, że cynk w nietypowy sposób wzmacnia aktywność GluK3, podczas gdy zwykle tłumi inne typy receptorów. Tutaj autorzy stwierdzili, że to wzmocnienie zależy w dużym stopniu od tego, które białko Neto jest obecne. Gdy GluK3 działa samodzielnie, cynk w przybliżeniu podwaja czas, przez jaki receptor pozostaje aktywny, i umiarkowanie zwiększa prąd. Dodanie Neto1 tłumi ten efekt. Natomiast gdy GluK3 współdziała z Neto2, cynk i Neto2 działają razem, aby znacznie wzmocnić prąd — znacznie bardziej niż każdy z nich oddzielnie. Sugeruje to, że synapsy bogate w Neto2 i cynk mogą silnie wzmacniać sygnały zależne od GluK3 podczas intensywnej aktywności, natomiast synapsy z przewagą Neto1 pozostają bardziej powściągliwe.
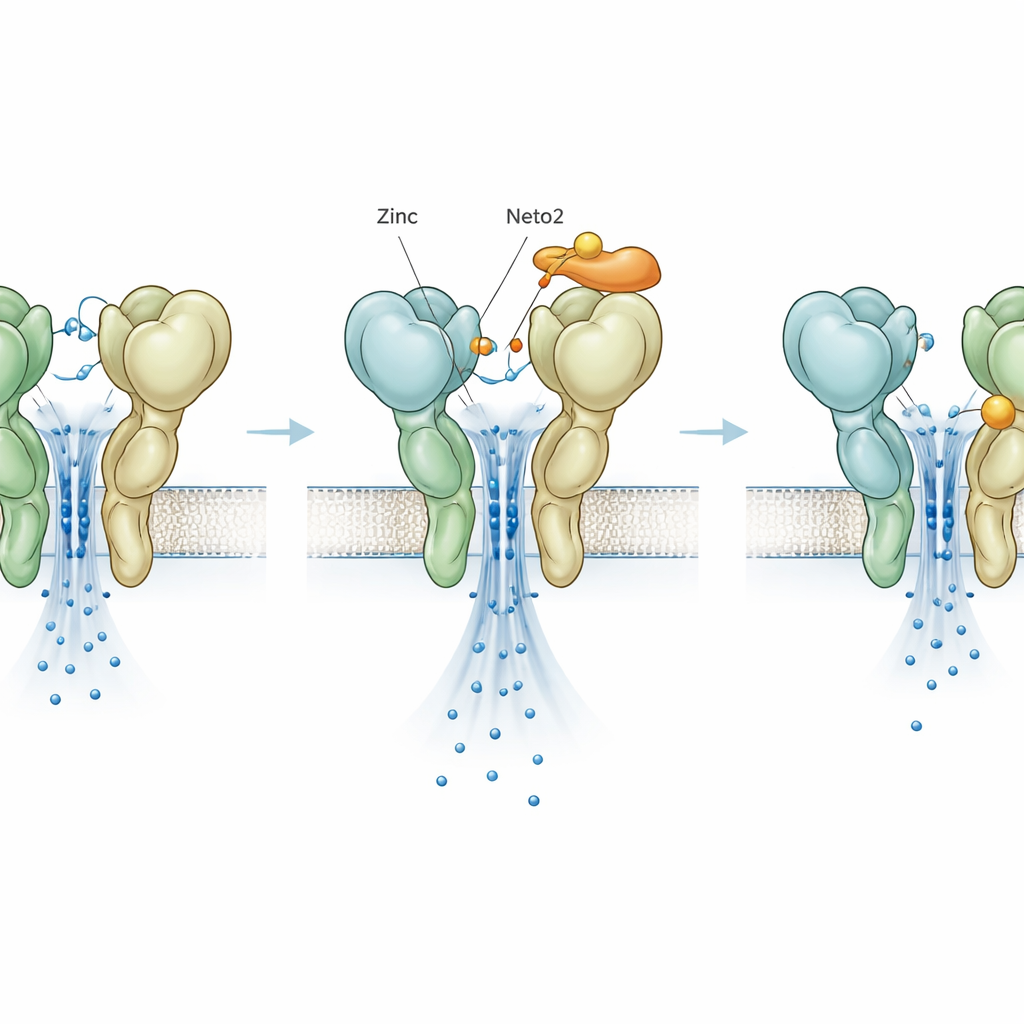
Ukryty hamulec ujawniony przez mutację
Aby oddzielić działanie cynku od wpływu białek pomocniczych, badacze wprowadzili jedną zmianę literową w GluK3, nazwaną D759G, która usuwa znane miejsce wiązania cynku. Jak oczekiwano, sama ta mutacja uczyniła receptor bardziej stabilnym i wolniejszym w przechodzeniu w stan wyłączenia, naśladując typowy efekt cynku. Zaskakująco, po dodaniu cynku do tego mutanta nie obserwowano już wzmocnienia aktywności; zamiast tego cynk przyspieszał wyłączanie i zmniejszał prąd, ujawniając drugie, wcześniej ukryte miejsce cynkowe działające jako hamulec. Neto1 i Neto2 nadal wywierały swoje charakterystyczne efekty na mutancie, pokazując, że ich zasadniczy wpływ nie zależy od pierwotnego miejsca wiążącego cynk. Jednak nawet to nowo odkryte hamujące działanie cynku było różnie modulowane przez oba białka pomocnicze, dodając kolejny regulowany element do tego systemu.
Widzenie struktury stojącej za zachowaniem
Aby powiązać funkcję z formą, zespół zastosował krioelektronową mikroskopię, aby zobrazować zmutowany receptor GluK3 zamrożony w stanie nieaktywnym. Obrazy wykazały, że region wiążący glutaminian tworzy bardziej zwarte, ciasno upakowane ciało w mutancie D759G w porównaniu z normalnym GluK3. To strukturalne „dociśnięcie” prawdopodobnie utrudnia receptorowi przejście do kształtu wyłączonego, wyjaśniając, dlaczego mutant, podobnie jak GluK3 związanego z cynkiem, pozostaje aktywny dłużej. Jednocześnie obrazy pokazały, że nie wszystkie części receptora są zablokowane w jednej konfiguracji, wskazując na z natury elastyczną architekturę szczególnie wrażliwą na drobne chemiczne impulsy.
Co to oznacza dla zdrowia mózgu
Podsumowując, badanie ukazuje GluK3 nie jako prosty przełącznik włącz/wyłącz, lecz jako precyzyjnie regulowane centrum, w którym zbiega się glutaminian, białka pomocnicze i cynk. Neto1 i Neto2 ustalają, jak szybko sygnały wygasają i jak szybko receptory mogą ponownie reagować, podczas gdy cynk może albo dalej wzmacniać, albo w niektórych warunkach hamować aktywność poprzez wiele miejsc wiążących. Ponieważ GluK3, białka Neto i cynk współistnieją w synapsach zaangażowanych w pamięć i są powiązane z padaczką oraz zaburzeniami psychiatrycznymi, zrozumienie tej wielowarstwowej kontroli może naprowadzić przyszłe terapie, które delikatnie dostrają sygnalizację synaptyczną zamiast jej całkowitego wyłączania.
Cytowanie: Vinnakota, R., Dawath, B.K., Assaiya, A. et al. Multilayered regulation of GluK3 kainate receptors is mediated by Neto subunits and zinc. Commun Biol 9, 420 (2026). https://doi.org/10.1038/s42003-026-09707-7
Słowa kluczowe: receptory kainainowe, GluK3, białka Neto, synaptyczny cynk, plastyczność synaptyczna