Clear Sky Science · pl
Nadużywanie narkotyków uzależniających i depresja — spojrzenie na epigenetykę
Dlaczego te badania mają znaczenie w życiu codziennym
Narkotyki uzależniające i depresja bywają traktowane jako odrębne problemy, tymczasem często występują razem u tej samej osoby. Niniejszy przegląd wyjaśnia, jak długotrwałe stosowanie substancji takich jak metamfetamina, kokaina, opioidy i konopie może zostawiać trwałe „molekularne blizny” w mózgu, które zwiększają ryzyko wystąpienia depresji. Odkrywając te ukryte zmiany, artykuł wskazuje kierunki dla przyszłych testów ostrzegających osoby najbardziej podatne — oraz dla bardziej precyzyjnych terapii mogących odwracać uszkodzenia, zamiast jedynie maskować objawy.
Jak uzależnienie i przygnębienie splatają się ze sobą
Autorzy rozpoczynają od przedstawienia bliskiego klinicznego związku między nadużywaniem narkotyków a depresją. Osoby wielokrotnie używające substancji uzależniających znacznie częściej zgłaszają utrzymujące się przygnębienie, utratę przyjemności, problemy ze snem i myśli samobójcze. Regiony mózgu kontrolujące nagrodę, motywację, pamięć i podejmowanie decyzji — okolica brzuszna nakrywki, jądro półleżące, kora przedczołowa i hipokamp — są istotne w obu stanach. Przewlekła ekspozycja na narkotyki zaburza neuroprzekaźniki takie jak dopamina i serotonina, hormony stresu kontrolowane przez oś podwzgórze-przysadka-nadnercza, sygnały immunologiczne oraz zaopatrzenie energetyczne neuronów. Wspólnie te zmiany czynią mózg mniej odpornym na stres i bardziej podatnym na stany depresyjne, nawet długo po ostatniej dawce.
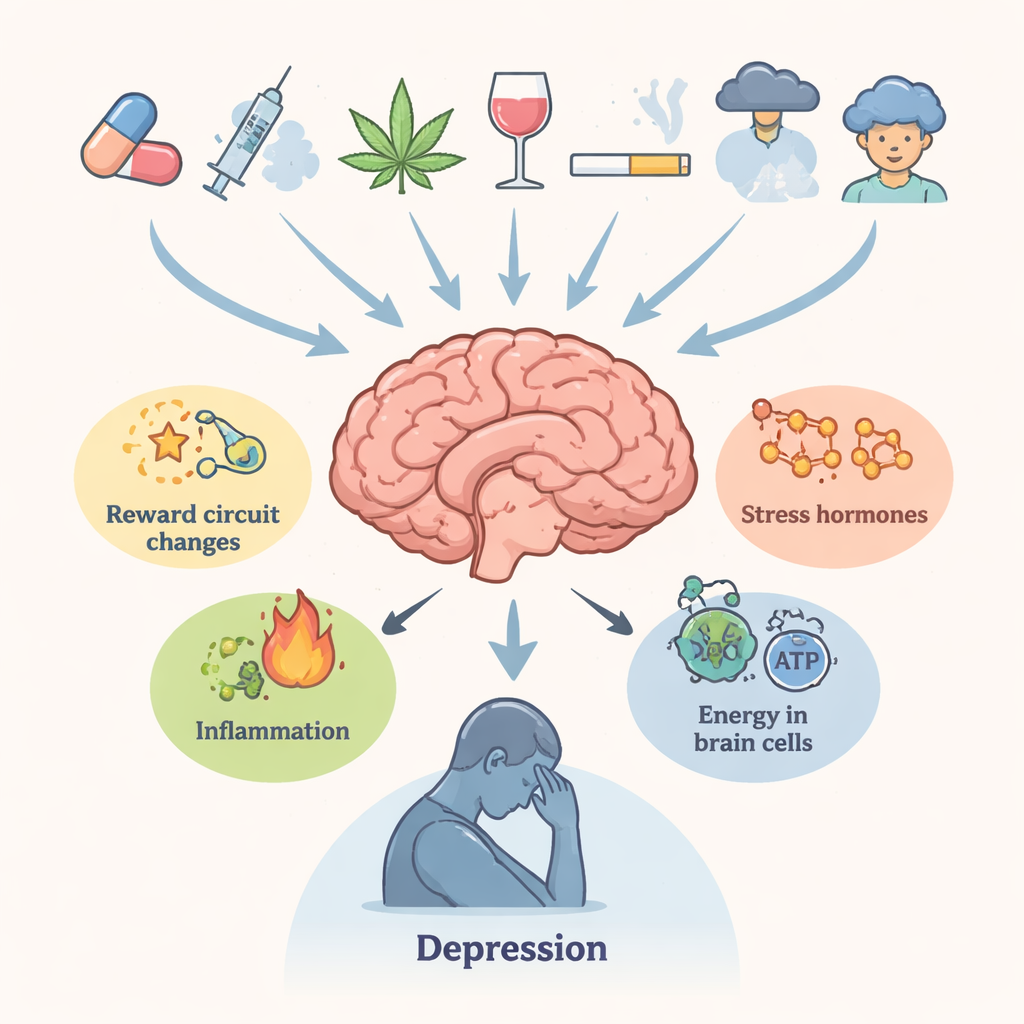
Substancje, które przebudowują chemię mózgu
Przegląd omawia kilka głównych klas narkotyków. Stymulanty typu amfetaminowego i ich pokrewne, w tym syntetyczne „sole do kąpieli”, wywołują potężne wybuchy dopaminy i innych przekaźników, które z czasem uszkadzają zakończenia nerwowe, zaburzają równowagę glutaminianu, przeciążają siateczkę śródplazmatyczną i skłaniają komórki do szkodliwego autodigestion (autofagii). Używanie konopi w okresie dojrzewania wiąże się z późniejszą depresją i ryzykiem samobójstwa, prawdopodobnie poprzez długotrwałe zmiany w receptorach kannabinoidowych, strukturze istoty białej i czułości obwodów dopaminergicznych. Opioidy, choć łagodzą ból, mogą wywoływać zapalenie, niewydolność mitochondriów i obniżenie sygnałów wspierających wzrost, takich jak neurotroficzny czynnik pochodzenia mózgowego (BDNF). Kokaina wielokrotnie aktywuje system stresowy i zmienia kluczowe regulatory, takie jak FKBP5, przyczyniając się do lęku i przygnębienia podczas odstawienia. W każdym przypadku zaburzenia biologiczne mają tendencję do utrzymywania się, co pomaga wyjaśnić, dlaczego symptomy emocjonalne mogą trwać dłużej niż oczywista intoksykacja.
Epigenetyka: pamięć ekspozycji
Aby zrozumieć, dlaczego skutki narkotyków utrzymują się, autorzy koncentrują się na epigenetyce — chemicznych etykietach i molekularnych przełącznikach, które regulują aktywność genów bez zmiany liter DNA. Substancje uzależniające modyfikują metylację DNA (znak na zasadach cytozyny), zmieniają grupy chemiczne na histonach pakujących DNA oraz wpływają na RNA niekodujące, które dopracowują, które białka są wytwarzane. Na przykład metamfetamina i kokaina przesuwają wzory metylacji w obszarach mózgu związanych z nagrodą, zmieniając poziomy enzymów dodających lub usuwających te znaki. Opioidy i stymulanty przebudowują acetylację i metylację histonów w genach kontrolujących receptory glutaminianowe, sygnalizację stresową i strukturę synaps. Dziesiątki mikroRNA, długich RNA niekodujących i RNA kolistych wzrastają lub spadają pod wpływem narkotyków, wspólnie wpływając na zapalenie, wzrost neuronów i siłę synaps. Te zmiany epigenetyczne działają jak molekularna „pamięć” historii używania narkotyków.
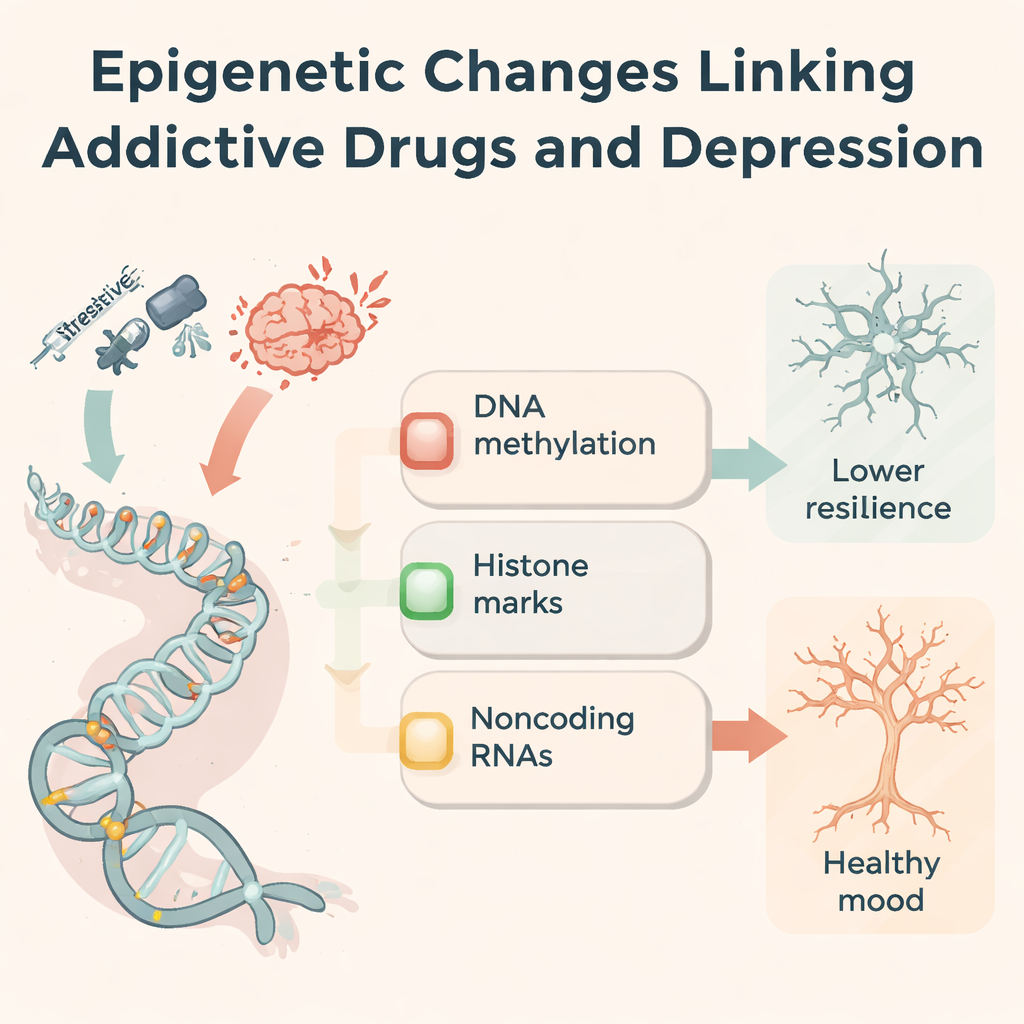
Wspólne ścieżki molekularne w depresji i uzależnieniu
Ta sama aparatura epigenetyczna pojawia się również u osób i zwierząt z depresją, które nigdy nie zażywały narkotyków. Doświadczania stresowe mogą zmieniać metylację receptorów hormonów stresu (takich jak NR3C1 i FKBP5), redukować pomocne czynniki wzrostu jak BDNF oraz przebudowywać szlaki immunologiczne i glutaminergiczne. Wiele tych samych RNA niekodujących zmienianych przez narkotyki jest również źle regulowanych w depresji, wpływając na rodzenie się nowych neuronów, reakcję mikrogleju na zapalenie i siłę połączeń synaptycznych. Autorzy proponują trójskładnikowe ramy: regulację odpowiedzi na stres, przebudowę obwodów nagrody i plastyczność synaptyczną. Wzdłuż tych osi uzależnienie i depresja wielokrotnie zbiegają się wokół małego zestawu genów i znaków, co dostarcza biologicznego wyjaśnienia, dlaczego oba zaburzenia tak często współwystępują.
Co to oznacza dla przyszłej profilaktyki i leczenia
Na zakończenie przegląd argumentuje, że zmiany epigenetyczne mogłyby stać się wczesnymi biomarkerami ostrzegawczymi i celami dla terapii nowej generacji. Leki o szerokim działaniu, które usuwają znaki epigenetyczne, wykazały już pewne efekty przeciwdepresyjne u zwierząt, ale są zbyt nieprecyzyjne do rutynowego stosowania u ludzi. Nowe narzędzia — takie jak edytory epigenomu oparte na CRISPR oraz terapie modulujące specyficzne mikroRNA lub długie RNA — mogą kiedyś regulować problematyczne geny w wybranych komórkach mózgu, oszczędzając inne. Autorzy przestrzegają, że większość obecnych danych pochodzi od gryzoni i z analiz tkanki masowej mózgu, a biologia ludzka jest bardziej złożona. Mimo to, ujawniając, jak narkotyki uzależniające i depresja zapisują się w tym samym molekularnym „notesie”, praca ta daje nadzieję na bardziej spersonalizowane i trwalsze terapie.
Cytowanie: Zhang, W., Xu, M., Wang, C. et al. Addictive drug abuse and depression-a focus on epigenetics. Commun Biol 9, 297 (2026). https://doi.org/10.1038/s42003-026-09705-9
Słowa kluczowe: uzależnienie i depresja, epigenetyka, nadużywanie narkotyków, metylacja DNA, RNA niekodujące