Clear Sky Science · pl
Aromatyczna plamka w czynnikach transkrypcyjnych podobnych do WhiB ułatwia interakcję z głównym czynnikiem sigma u Mycobacterium tuberculosis
Jak bakterie wyczuwają zagrożenie
Mycobacterium tuberculosis, zarazek wywołujący gruźlicę, przetrwa w organizmie ludzkim dzięki szybkiemu przeprogramowywaniu, które geny są włączane lub wyłączane w zmieniających się warunkach, na przykład po ekspozycji na antybiotyki lub ataku układu odpornościowego. To badanie odkrywa drobny element strukturalny — „aromatyczną plamkę” — w rodzinie bakteryjnych białek, która pomaga im chwytać główny mechanizm sterujący odczytem genów. Zrozumienie tego mikroskopijnego uścisku dłoni wyjaśnia, jak gruźlica i pokrewne bakterie się adaptują, i może wskazać nowe sposoby osłabienia tego patogenu.
Specjalna rodzina białek-regulatorów bakterii
Praca koncentruje się na białkach podobnych do WhiB (Wbl), grupie spotykanej wyłącznie u promieniowców (actinobacteria) i ich wirusów, w tym u Mycobacterium tuberculosis. Białka te zawierają mały klaster żelazo–siarkowy, metalowy kofaktor pozwalający im wyczuwać zmiany w natlenowaniu i inne stresy. Wbl są znane z kontrolowania kluczowych procesów, takich jak podział komórkowy, odpowiedź na stres oksydacyjny i niedobór składników odżywczych oraz oporność na antybiotyki. Jednak większość z nich nie ma klasycznych motywów używanych przez wielu regulatorów do bezpośredniego wiązania DNA, co pozostawia od dawna nierozwiązaną zagadkę: jak właściwie kontrolują aktywność genów?
Chwytanie głównego „czytnika” genów
Wcześniejsze badania wykazały, że kilka białek Wbl aktywuje geny przez wiązanie się z zachowaną regionem 4 głównego czynnika sigma. Czynnik sigma to część polimerazy RNA — enzymu odczytującego DNA — która rozpoznaje miejsce startu transkrypcji. U Mycobacterium tuberculosis ten główny czynnik sigma używa tego samego regionu 4 do rekrutacji wielu różnych regulatorów. Autorzy połączyli krystalografię rentgenowską, biochemiczne testy wyciągania kompleksów (pull-down) oraz kalorymetrię, aby wykazać, że praktycznie wszystkie testowane białka Wbl z tego bakterium (z jedną specjalną odmianą) przylegają do dokładnie tego samego miejsca w regionie 4 sigma i robią to z bardzo silnym wiązaniem.
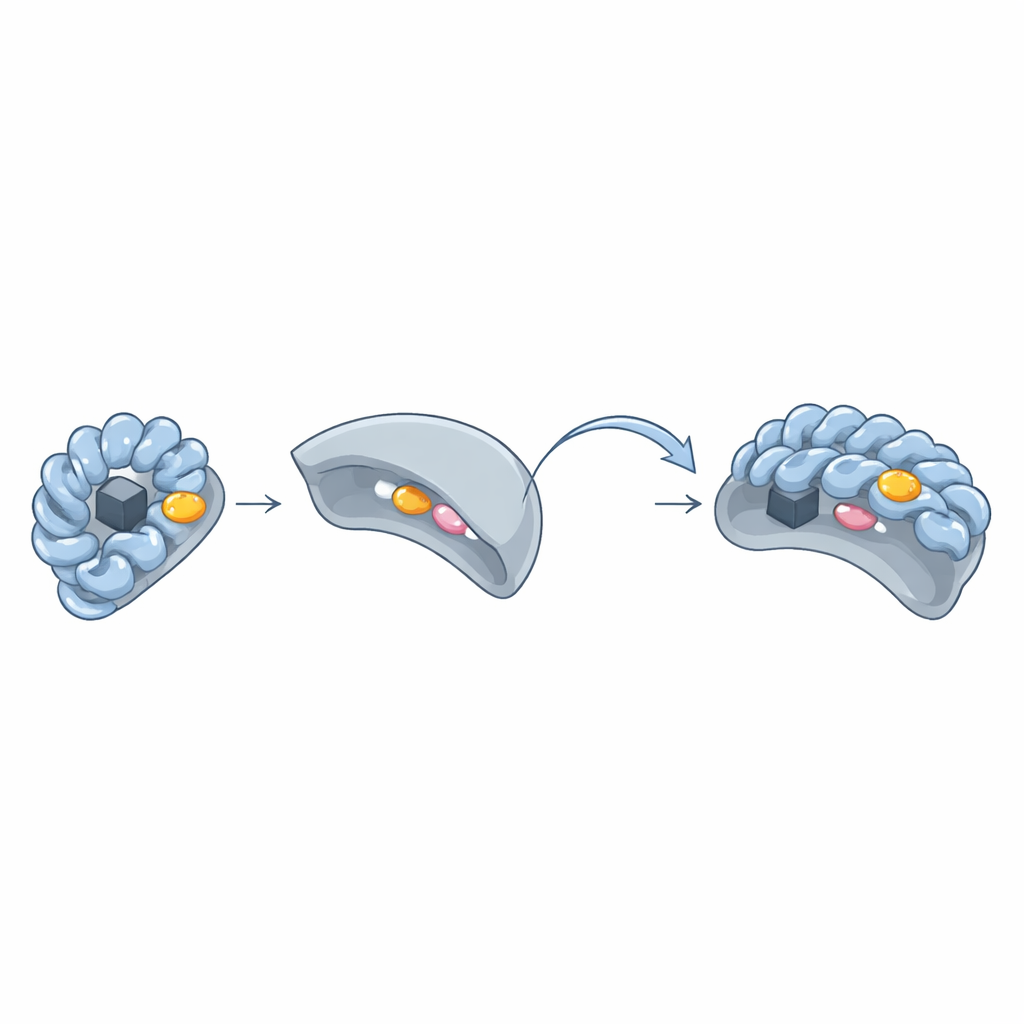
Ukryty „aromatyczny”, zamek i klucz
Porównując trójwymiarowe struktury par Wbl–sigma, zespół odkrył powtarzający się skupisko dużych, pierścieniowatych aminokwasów — tryptofanu, fenyloalaniny, tyrozyny lub histydyny — tworzące „aromatyczną plamkę” na powierzchni białek Wbl. Plamka ta otacza klaster żelazo–siarkowy i naciska bezpośrednio na dwa kluczowe aminokwasy w regionie 4 sigma. Gdy badacze zamienili pozostałości z aromatycznej plamki na prostsze, białka Wbl nie mogły już tworzyć stabilnych kompleksów z sigma, a ich klastry żelazo–siarkowe często stawały się niestabilne. Nawet w wariantach Wbl, które wydawały się nietypowe — takich jak WhiB6 czy WhiB5 — alternatywne reszty lub pobliskie aromatyczne łańcuchy boczne kompensowały, zachowując ten sam styl interakcji.
Wspólny projekt u bakterii i ich wirusów
Aby ocenić, jak rozpowszechniona jest ta cecha, autorzy przeanalizowali 995 sekwencji białek Wbl z różnych gatunków promieniowców i ich infekujących wirusów (bakteriofagów actinobacteria). Pogrupowali te białka na 29 podrodzin i stwierdzili, że pięć głównych gałęzi, reprezentowanych przez pięć białek Wbl z Mycobacterium tuberculosis, stanowi około 80% wszystkich sekwencji. Modelowanie strukturalne z użyciem AlphaFold ujawniło, że prawie wszystkie Wbl — ponad 98% — mają co najmniej dwie aromatyczne reszty w pozycjach odpowiadających aromatycznej plamce, a niemal wszystkie posiadają przynajmniej jedną w najważniejszych centralnych pozycjach. Eksperymenty z kilkoma białkami Wbl kodowanymi przez fagów potwierdziły, że te wirusowe wersje również wiążą ten sam region sigma w sposób zależny od plamki, co wskazuje, że ten sam projekt molekularny jest wykorzystywany zarówno u bakterii, jak i ich fagów.
Ewolucyjna przepychanka o kontrolę
Drzewo filogenetyczne zbudowane na podstawie tych 995 sekwencji ukazuje mieszanie się białek Wbl fagów i bakterii, z wyraźnymi oznakami poziomego transferu genów w obu kierunkach. Niektóre wirusowe Wbl leżą u podstaw głównych gałęzi bakteryjnych, sugerując, że fag mógł podarować te regulatory wczesnym bakteriom, które następnie zaadaptowały je do własnych potrzeb. Inne wirusowe Wbl wydają się osadzone w przeważnie bakteryjnych klastrach, co wskazuje na późniejsze transfery genów z powrotem do fagów. Ponieważ białka Wbl ściśle kontrolują odpowiedzi na stres, rozwój komórki i oporność na leki poprzez swoje aromatyczne plamki wiążące sigma, te wymiany tam i z powrotem prawdopodobnie ukształtowały sposób, w jaki zarówno bakterie, jak i ich wirusy manipulują maszynerią transkrypcyjną gospodarza.
Co to oznacza dla gruźlicy i nie tylko
Mówiąc prosto, to badanie pokazuje, że wielu regulatorów promieniowców dzieli drobne, lecz kluczowe lepkie miejsce — aromatyczną plamkę — które pozwala im zadokować do tej samej części „silnika” odczytującego geny i precyzyjnie dostroić, które geny są aktywne pod wpływem stresu. U Mycobacterium tuberculosis ten wspólny mechanizm dokowania pomaga koordynować odpowiedzi wspierające przetrwanie, wirulencję i oporność na antybiotyki. Ujawniając, jak działa to mikroskopijne „złącze” i jak szeroko jest zachowane, praca wskazuje potencjalny słaby punkt, który pewnego dnia mógłby zostać wykorzystany, aby zaburzyć zdolność patogenu do adaptacji i przetrwania wewnątrz gospodarza.
Cytowanie: Guiza Beltran, D., Wan, T., Seravalli, J. et al. Aromatic patch in whiB-like transcription factors facilitates primary sigma factor interaction in mycobacterium tuberculosis. Commun Biol 9, 424 (2026). https://doi.org/10.1038/s42003-026-09698-5
Słowa kluczowe: Mycobacterium tuberculosis, czynniki transkrypcyjne, czynnik sigma, białka żelazo–siarkowe, ewolucja bakteriofagów