Clear Sky Science · pl
Dowód zasadności terapii genowej NF1 w szczurzych modelach ksenograftów plexiformnych nerwiaków
Dlaczego te badania są ważne
Osoby z genetycznym schorzeniem nerwiakowłókniakowatością typu 1 (NF1) często rozwijają duże, deformujące guzy nerwów zwane nerwiakami plexiformnymi. Zmiany te mogą powodować ból, problemy z poruszaniem się oraz poważne problemy estetyczne, a obecne metody leczenia są ograniczone, a zabiegi chirurgiczne często niemożliwe. Ponieważ NF1 wynika z uszkodzenia jednego genu, wielu badaczy liczy, że terapia genowa — naprawa lub zastąpienie wadliwego genu — mogłaby kiedyś zmniejszyć lub nawet zlikwidować te guzy. To badanie daje wczesny, ale przekonujący test tej koncepcji na myszach, stawiając prostą, lecz doniosłą hipotezę: jeśli przywrócisz brakujący gen NF1 w już istniejących guzach, czy one znikną?
Budowa realistycznego modelu guza u myszy
Badacze najpierw potrzebowali systemu laboratoryjnego, który wiernie odzwierciedlałby ludzkie nerwiaki plexiformne. Wykorzystali ludzkie komórki Schwanna, komórki podporowe owijające nerwy, pobrane od pacjenta, którego komórki utraciły obie działające kopie genu NF1. Te komórki umieszczono obok uszkodzonych nerwów kulszowych u myszy z upośledzonym układem odpornościowym. W ciągu kilku tygodni nerwy konsekwentnie rozwijały pogrubioną, silnie komórkową tkankę o nieuporządkowanej strukturze i gęstych pasmach kolagenu — cechy charakteryzujące nerwiaki plexiformne. Kontrolne operacje bez tych komórek pozbawionych NF1 lub z komórkami mającymi tylko jedną uszkodzoną kopię NF1 nie prowadziły pewnie do powstania guzów. Pokazało to, że ludzkie komórki z całkowitą utratą NF1 napędzały wzrost guza i stworzyły solidny, szybki model choroby.
Włączanie NF1 z powrotem w komórkach guza
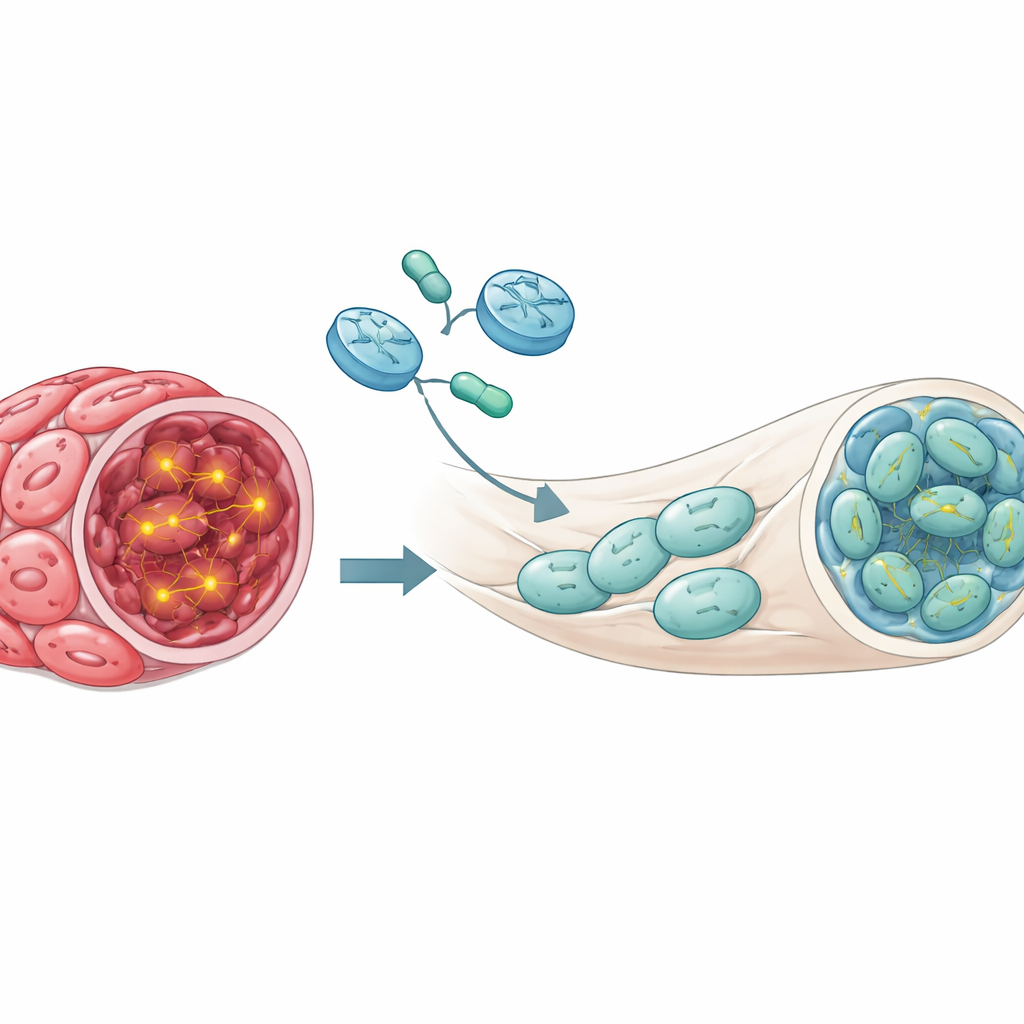
Mając ten model, zespół zmodyfikował komórki Schwanna formujące guzy tak, by niosły przełączalną wersję genu NF1 pochodzącą od myszy. Przełącznik reagował na powszechny antybiotyk doksycyklinę: gdy myszy piły wodę zawierającą doksycyklinę, dodany gen NF1 się włączał w wszczepionych komórkach. Myszy najpierw miały czas na rozwój guzów, a dopiero potem gen został włączony. Wyniki były uderzające. U zwierząt, w których NF1 pozostał wyłączony, większość nerwów kulszowych nadal miała neurofibromy. W przeciwieństwie do tego, gdy NF1 zostało ponownie aktywowane, większość nerwów wyglądała pod mikroskopem normalnie, a chemiczne markery nadaktywnego sygnalizowania wzrostu były znacząco zmniejszone. W istocie, przywrócenie NF1 cofnęło tkankę nowotworową w kierunku zdrowego stanu nerwu.
Odwrócenie utraty NF1 w inny sposób
Aby pokazać, że ten efekt nie ogranicza się do jednego inżynieryjnego zabiegu, naukowcy zbudowali drugi, komplementarny model. Tym razem zaczęli od ludzkich komórek Schwanna, które miały tylko jedną uszkodzoną kopię NF1 — podobnie jak osoby z NF1 dziedziczą tę mutację we wszystkich swoich komórkach. Dodali przełącznik genetyczny, który mógł tymczasowo obniżyć aktywność pozostałego NF1 w obecności doksycykliny. Gdy myszy piły doksycyklinę, poziomy NF1 jeszcze spadły i guzy szybko się formowały. Co kluczowe, gdy po rozwoju guzów doksycyklina została usunięta, poziomy NF1 wzrosły ponownie i wiele nerwów wróciło do bardziej normalnej struktury. Ponownie, wskaźniki sygnalizacji związanej ze wzrostem spadły w nerwach, które się znormalizowały. Razem te dwa przeciwne podejścia przełączające — włączanie NF1 lub znoszenie jego tłumienia — prowadzą do tego samego wniosku: przywrócenie NF1 w komórkach guza może cofnąć już ustaloną chorobę.
Testowanie bardziej realistycznego sposobu dostarczenia
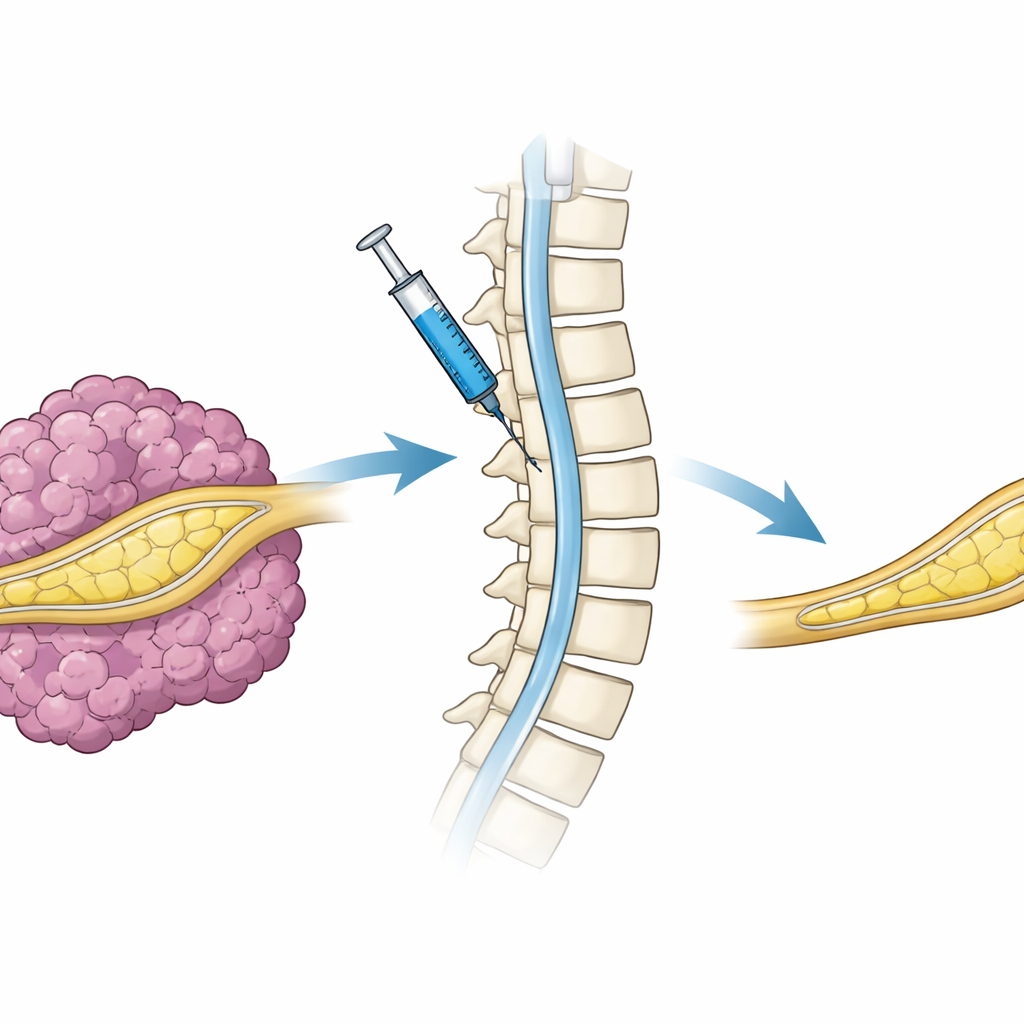
Ponad genetyczne przełączniki wbudowane w komórki w laboratorium, prawdziwa terapia musiałaby dostarczyć działający gen NF1 do układu nerwowego żyjącego pacjenta. Aby zbadać ten etap, naukowcy zapakowali pełny gen NF1 do wektora lentivirusowego i wstrzyknęli go do przestrzeni płynowej wokół rdzenia kręgowego myszy z guzami, drogą znaną jako podoponowe (intrathecal) podanie. Zwierzęta otrzymywały następnie doksycyklinę, aby dostarczony gen się włączył. W porównaniu z myszami otrzymującymi wirusa kontrolnego, te lec towane wirusem niosącym NF1 rozwijały istotnie mniej guzów, a ich tkanka nerwowa wyglądała bardziej normalnie. Choć był to krótki eksperyment z jednorazową dawką, pokazał, że dostarczenie genu NF1 przez płyn rdzeniowy może dotrzeć do nerwów obwodowych i istotnie zmniejszyć obciążenie guzem.
Co ta praca oznacza dla osób z NF1
To badanie nie oferuje jeszcze gotowego leczenia dla pacjentów, ale odpowiada na kluczowe pytanie: w starannie zaprojektowanych modelach mysich, które ściśle przypominają ludzkie nerwiaki plexiformne, przywrócenie NF1 w komórkach guza może zmniejszyć lub znormalizować istniejące guzy. Praca dostarcza dowodu zasadności, że terapia genowa NF1 jest strategią realną, a nie tylko teoretyczną nadzieją. Wciąż pozostaje wiele wyzwań — znalezienie najbezpieczniejszych i najwydajniejszych nośników dostawy, określenie, jaka ilość aktywności NF1 jest wystarczająca, oraz testy długoterminowych skutków w bardziej naturalnych modelach. Mimo to te wyniki kładą naukowe podstawy pod przyszłe terapie genowe, które mogłyby kiedyś przynieść trwałą ulgę od nerwiaków plexiformnych u osób żyjących z NF1.
Cytowanie: Hewa Bostanthirige, D., Plante, C., Caron, M. et al. Proof-of-principle of NF1 gene therapy in plexiform neurofibroma xenograft mouse models. Commun Biol 9, 419 (2026). https://doi.org/10.1038/s42003-026-09695-8
Słowa kluczowe: nerwiakowłókniakowatość typu 1, terapia genowa, nerwiak plexiformny, komórki Schwanna, dostawa lentivirusowa