Clear Sky Science · pl
Heterogeniczność między neuronami VIP i GRP leży u podstaw sygnalizacji receptora AVP w jądrze nadskrzyżowaniowym myszy
Dlaczego nasz zegar biologiczny trudno jest zresetować
Każdy, kto wysiadł z długiego lotu zdezorientowany lub miał problemy z pracą na nocne zmiany, wie, że nasz wewnętrzny zegar nie lubi nagłych zmian harmonogramu. Artykuł stawia bardzo konkretnie sformułowane pytanie sedna tego problemu: w obrębie głównego zegara mózgu, dlaczego niektóre komórki nerwowe silnie odczuwają sygnał czasowy, podczas gdy ich sąsiedzi w dużej mierze go ignorują? Śledząc pojedynczy sygnał chemiczny przez ten niewielki obwód zegarowy u myszy, autorzy odkrywają ukrytą podgrupę komórek, która pomaga określić, jak oporny jest nasz zegar biologiczny w obliczu „jet lagu”. 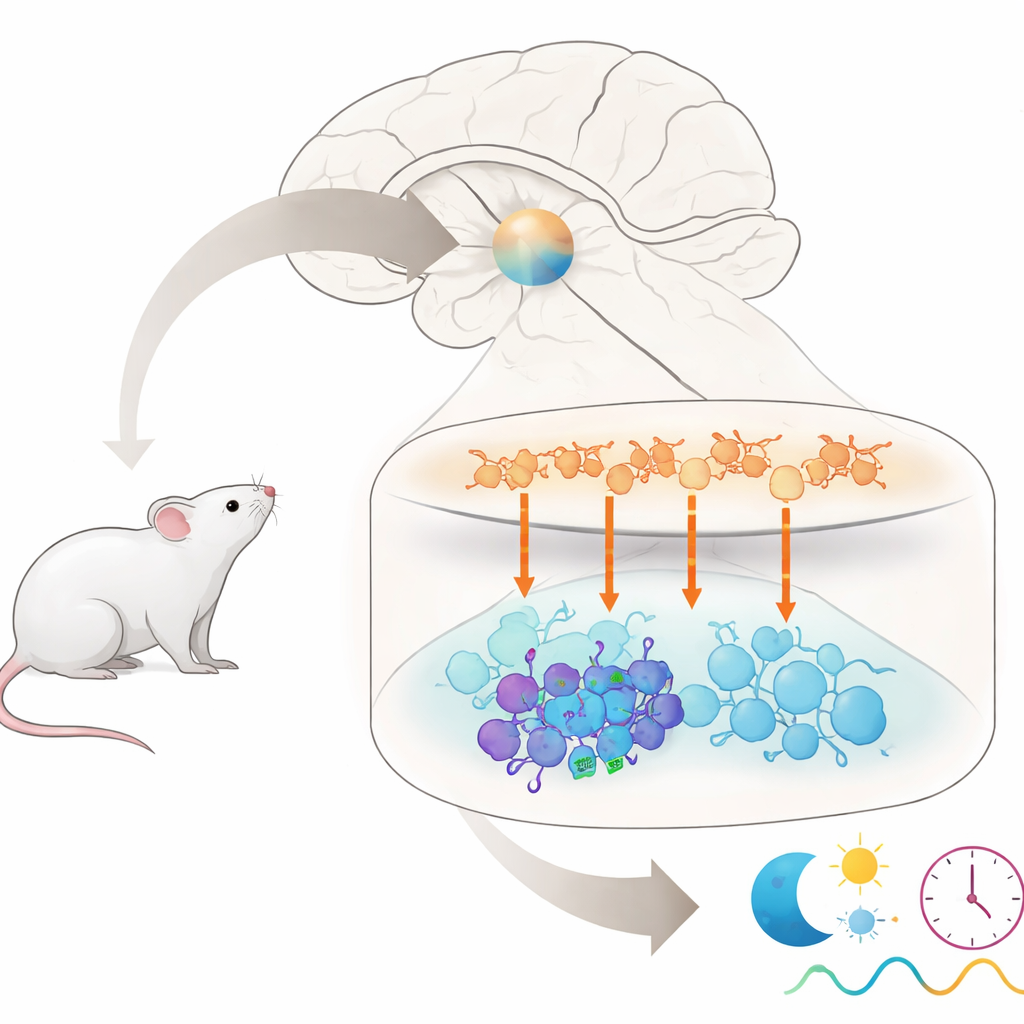
Niewielki zegar z wieloma różnymi uczestnikami
Główny zegar u ssaków znajduje się w małym obszarze mózgu zwanym jądrem nadskrzyżowaniowym, w skrócie SCN. Choć zawiera tylko około 20 000 komórek nerwowych, składa się z kilku odrębnych grup, które komunikują się ze sobą za pomocą różnych przekaźników chemicznych. Komórki w górnym obszarze „powłoki” głównie uwalniają przekaźnik zwany argininową wazopresyną (AVP), podczas gdy komórki w dolnym obszarze „rdzenia” często uwalniają inne przekaźniki, w tym peptyd jelitowo-naczyniowy (VIP) i peptyd uwalniający gastrynę (GRP). Razem te grupy muszą zachować synchronizację, aby generować 24-godzinne rytmy rządzące snem, uwalnianiem hormonów i wieloma innymi funkcjami organizmu. Jednak które dokładnie komórki w rdzeniu nasłuchują sygnałów od komórek AVP w powłoce pozostawało niejasne.
Śledzenie połączeń od komórek nadawczych do odbiorczych
Naukowcy najpierw odwzorowali, jak komórki AVP z powłoki fizycznie łączą się z komórkami VIP i GRP w rdzeniu. Użyli wirusa, by oznakować wychodzące włókna i możliwe miejsca kontaktu neuronów AVP u myszy, a następnie barwili przekroje mózgu, by zobaczyć, gdzie te włókna się kończą. Stwierdzili, że włókna AVP tworzyły pozorne miejsca kontaktowe zarówno na komórkach VIP, jak i GRP, ale w różnych proporcjach: około jedna czwarta komórek VIP i ponad połowa komórek GRP wykazywała takie przylegania. Pokazało to, że neurony AVP docierają do obu typów komórek rdzenia, ale nie ujawniało jeszcze, które z nich faktycznie reagują na sygnał. Aby to sprawdzić, zespół zastosował optogenetykę — aktywując neurony AVP światłem niebieskim — i poszukiwał c-Fos, markera aktywacji komórkowej, w neuronach VIP i GRP.
Mała podgrupa VIP, która naprawdę „słyszy” AVP
Gdy neurony AVP były stymulowane światłem, wiele komórek AVP samoistnie włączało c-Fos, co było spodziewane. Co ważne, mała podgrupa komórek VIP w rdzeniu również wykazała aktywację c-Fos, mimo że same nie wyrażały bezpośrednio białka wrażliwego na światło. Wskazywało to, że są one napędzane pośrednio przez sygnał AVP. W przeciwieństwie do tego, komórki GRP rzadko wykazywały c-Fos, mimo otrzymywania kontaktów AVP. Autorzy poszukali następnie transkryptu receptora AVP znanego jako V1a w tych populacjach przy użyciu czułych metod obrazowania RNA. Odkryli, że V1a był obecny tylko w mniejszości komórek VIP i był ledwie wykrywalny w komórkach GRP. Tak więc spośród wielu neuronów VIP mała podgrupa pozytywna na V1a wydaje się specjalnie dostrojona do odbierania i reagowania na sygnały AVP, podczas gdy większość neuronów GRP nie reaguje.
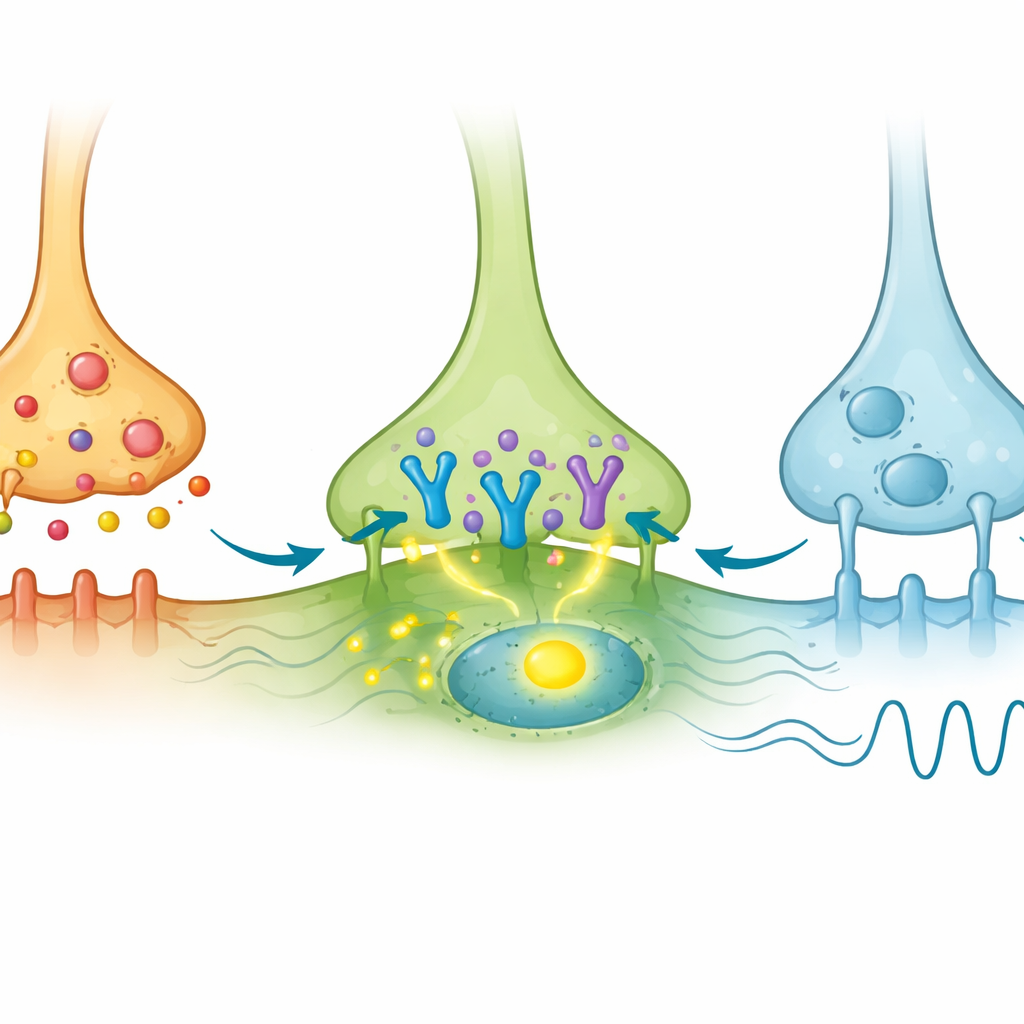
Jak niewielka grupa komórek wpływa na odzyskiwanie po jet lagu
Aby zbadać funkcję tych neuronów VIP noszących V1a, badacze stworzyli myszy, u których receptor V1a został usunięty tylko z komórek VIP. Zwierzęta te zachowały normalną długość rytmu dobowego w całkowitej ciemności, co pokazuje, że ten receptor w neuronach VIP nie jest potrzebny do ustawienia podstawowego tempa zegara. Jednak gdy harmonogram światło–ciemność został nagle przyspieszony lub opóźniony o osiem godzin, by naśladować jet lag, zmodyfikowane myszy dostosowywały swoje wzorce aktywności szybciej niż ich normalne rodzeństwo, zwłaszcza po przyspieszeniach i u samców. W innych eksperymentach usunięcie V1a w całym mózgu lub specyficznie w SCN wywoływało podobne zachowanie „odporne na jet lag”. Nowe wyniki sugerują zatem, że zaskakująco mała grupa neuronów VIP niosących receptory V1a może mieć nieproporcjonalny wpływ na to, jak sztywny lub elastyczny jest cały zegar.
Co to oznacza dla naszego poczucia czasu
W codziennym ujęciu badanie pokazuje, że w centralnym zegarze mózgu neurony produkujące AVP działają jak strażnicy czasu w górnej warstwie, wysyłając sygnały przez receptory V1a do wybranej grupy neuronów VIP w dolnej warstwie. Te nieliczne komórki VIP pomagają całej sieci opierać się nagłym zmianom cyklu światło–ciemność, spowalniając tempo, w jakim zegar się resetuje po przesunięciu. Usunięcie ich receptora wrażliwego na AVP sprawia, że system chętniej się przesuwa, ułatwiając dostosowania podobne do jet lagu u myszy. Poprzez zmapowanie tej ukrytej różnorodności wśród neuronów zegarowych, praca oferuje bardziej szczegółowy schemat połączeń stabilizujących nasze wewnętrzne poczucie czasu — i sugeruje, że selektywne modyfikowanie podobnych ścieżek u ludzi mogłoby pewnego dnia pomóc w radzeniu sobie z jet lagiem lub innymi zaburzeniami rytmu.
Cytowanie: Zhou, H., Moriyasu, D., Hsiao, SW. et al. Heterogeneity between VIP and GRP neurons underlies AVP receptor signaling in the mouse suprachiasmatic nucleus. Commun Biol 9, 414 (2026). https://doi.org/10.1038/s42003-026-09694-9
Słowa kluczowe: zegar okołodobowy, jądro nadskrzyżowaniowe, sygnalizacja wazopresynowa, neurony VIP, jet lag