Clear Sky Science · pl
Malonylacja lizyny reguluje ruchliwość ludzkich plemników
Dlaczego ruch plemników ma znaczenie
Dla wielu par borykających się z niewyjaśnioną niepłodnością kluczowym, ukrytym problemem bywa to, że plemniki po prostu nie pływają wystarczająco sprawnie, by dotrzeć do i zapłodnić komórkę jajową. Badanie to analizuje subtelną chemiczną „etykietę” na białkach plemników — zwaną malonylacją lizyny — która wydaje się działać jak niewidoczny hamulec dla ich ruchu. Odkrywając, jak ta modyfikacja zmienia źródła energii plemnika i wewnętrzne sygnalizowanie, praca wskazuje na nowe sposoby diagnozowania i potencjalnie leczenia powszechnej formy męskiej niepłodności związanej z obniżoną ruchliwością plemników.
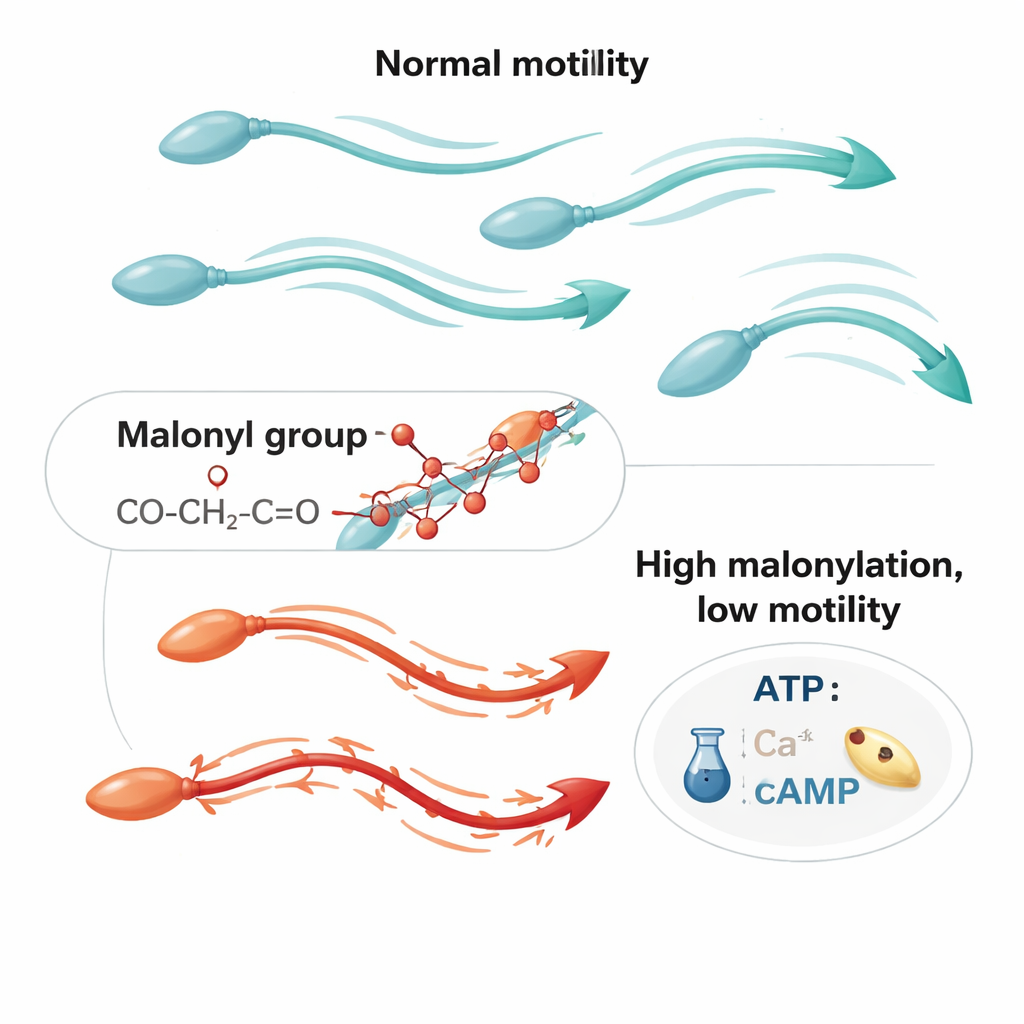
Nowa chemiczna etykieta na białkach plemników
Białka w komórkach często ulegają modyfikacjom po syntezie, zyskując małe grupy chemiczne, które mogą włączać lub wyłączać ich aktywność. Jedna z takich zmian, malonylacja lizyny, została odkryta dopiero w 2011 roku i powiązano ją z metabolizmem energetycznym w wielu typach komórek. Autorzy wcześniej wykazali, że ludzkie plemniki zawierają liczne malonylowane białka, lecz nie było jasne, co to oznacza dla płodności. W nowym badaniu zmapowali miejsca występowania tej etykiety w plemnikach i stwierdzili, że koncentruje się ona w ogonku — długiej, biczykowatej strukturze, której rytmiczne uderzenia napędzają ruch. Za pomocą testów biochemicznych i mikroskopii o wysokiej rozdzielczości pokazali, że malonylowane białka są szczególnie obfite w mitochondriach ogonka i płynie otaczającym te struktury — kluczowych miejscach produkcji energii i kontroli ruchu.
Kto zakłada i kto usuwa hamulec
Zespół zapytał następnie, które molekuły dodają i usuwają tę malonylową etykietę w ludzkich plemnikach. Znaleźli dowody, że enzym znany jako P300 działa jako „pisarz”, pomagając przenosić grupy malonylowe na reszty lizynowe, podczas gdy inny enzym, SIRT5, pełni rolę „mazacza”, który je usuwa. Gdy zablokowano SIRT5 chemicznym inhibitorem, ogólny poziom malonylacji wzrósł; gdy zahamowano P300, malonylacja zmalała. Pokazali także, że mleczan sodu (sodium malonate), mała cząsteczka wchłaniana przez plemniki i przekształcana do malonyl-CoA, zwiększała malonylację bez zaburzania innych podobnych modyfikacji chemicznych. Razem wyniki te opisują system regulacyjny, w którym malonyl-CoA dostarcza etykietę, P300 ją przyłącza, a SIRT5 usuwa — precyzyjnie dostrajając białka ogonka plemnika odpowiedzialne za ruch.
Wyższa malonylacja w słabo poruszających się plemnikach
Aby sprawdzić, czy ta chemia ma związek z rzeczywistą bezpłodnością, badacze porównali plemniki mężczyzn z prawidłowymi profilami nasienia z plemnikami od pacjentów z asthenozoospermią, schorzeniem definiowanym przez słabą ruchliwość postępową. Plemniki z grupy asthenozoospermicznej miały istotnie wyższe poziomy malonylacji lizyny i niższe poziomy SIRT5. W całym zestawie próbek większa malonylacja silnie korelowała z gorszym pływaniem do przodu oraz z obniżonym poziomem ATP, głównej jednostki energetycznej komórki. U podgrupy mężczyzn z wyjątkowo wysoką malonylacją plemniki wykazywały znacząco słabszą glikolizę — szlak spalania cukrów dostarczający dużej części paliwa dla ruchu ludzkich plemników. Te wzorce sugerują, że nadmierna malonylacja wiąże się zarówno z zaburzoną produkcją energii, jak i z gorszą wydolnością pływania.
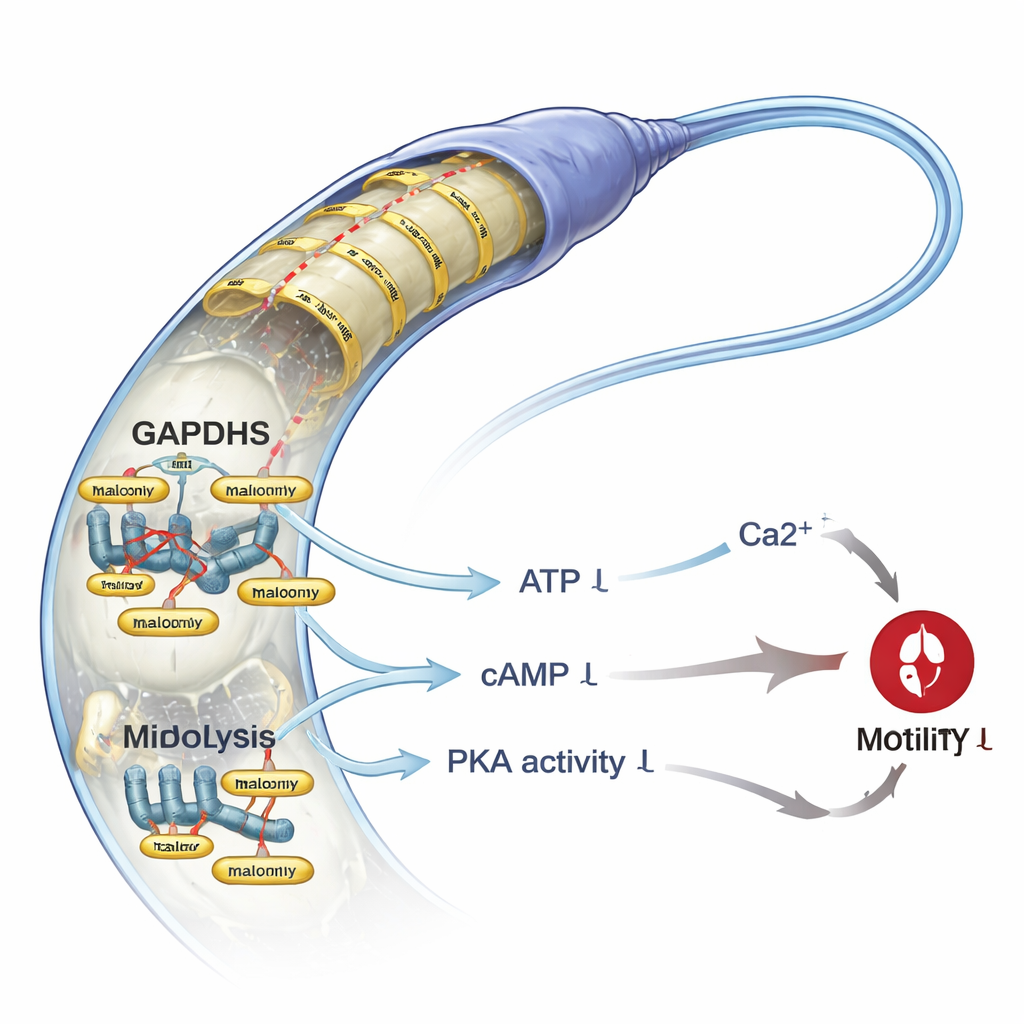
Eksperymentalne „dokręcenie” hamulca
Naukowcy zapytali następnie, co się stanie, jeśli celowo podniosą poziom malonylacji w inaczej zdrowych plemnikach. Leczenie próbek od mężczyzn z normalnymi parametrami nasienia mleczanem sodu zwiększyło poziomy malonylacji, ale nie zabiło komórek. Zmiana ta jednak znacząco zmniejszyła całkowitą i postępową ruchliwość oraz utrudniła plemnikom przeciskanie się przez lepkie medium imitujące żeński układ rozrodczy. Testy mechanistyczne wyjaśniły przyczynę: plemniki traktowane mleczanem sodu miały niższą wydajność glikolityczną, mniej ATP i obniżone ilości cAMP — przekaźnika, który aktywuje kluczowy enzym PKA. Aktywność PKA spadła, podobnie jak fosforylacja białek leżących w dalszym ciągu ścieżki, znanych z wspierania ruchliwości. Jednocześnie wewnętrzny poziom wapnia w plemnikach zmalał o około połowę, mimo że główny kanał wapniowy plemników, CatSper, nie był bezpośrednio dotknięty. To połączenie — mniej energii, słabsze sygnalizowanie i obniżony poziom wapnia — daje spójne wyjaśnienie zaobserwowanej utraty ruchliwości.
Od molekularnych etykiet do męskiej płodności
Sumując wszystkie ustalenia, badanie proponuje, że malonylacja lizyny działa jako negatywny regulator ruchliwości ludzkich plemników. Gdy poziomy malonylacji rosną — z powodu niskiego SIRT5, wysokiego malonyl-CoA lub zaburzeń w powiązanych szlakach — kluczowe białka napędzające glikolizę i gospodarkę wapniową, takie jak GAPDHS i VDAC3, stają się nadmiernie oznakowane. Tłumi to produkcję energii i krytyczne kaskady sygnałowe w ogonku plemnika, prowadząc do ospałego ruchu i gorszej zdolności do penetrowania gęstych płynów. Dla czytelnika nieznającego tematu wniosek jest taki, że plemniki potrzebują nie tylko odpowiedniej liczby; potrzebują także precyzyjnie wyregulowanych systemów chemicznych, które napędzają ich pływanie. Zakłócenia w małej, odwracalnej etykiecie, takiej jak malonylacja, mogą przyczyniać się do niewyjaśnionej męskiej niepłodności i w przyszłości dawać nowe biomarkery lub cele terapeutyczne mające na celu przywrócenie witalności plemników.
Cytowanie: Cheng, Y., Tian, Y., Chen, H. et al. Lysine malonylation regulates human sperm motility. Commun Biol 9, 178 (2026). https://doi.org/10.1038/s42003-026-09683-y
Słowa kluczowe: ruchliwość plemników, męska niepłodność, modyfikacja potranslacyjna, malonylacja lizyny, metabolizm energetyczny