Clear Sky Science · pl
Strukturalne podstawy rozpoznawania receptorów u nietoperzy przez SARS-CoV-2 i pokrewne koronawirusy SARS2
Dlaczego ta opowieść o nietoperzach i wirusach wciąż ma znaczenie
Pandemia COVID-19 rozpoczęła się ponad sześć lat temu, a naukowcy wciąż układają, jak wirus wywołujący chorobę, SARS-CoV-2, stał się tak sprawny w infekowaniu ludzi. Kluczową zagadką jest to, w jaki sposób ten wirus i jego bliscy krewni znalezieni u nietoperzy przyczepiają się do białka zwanego ACE2 na powierzchni komórek — to pierwszy i decydujący krok w infekcji. Zrozumienie tych mikroskopijnych interakcji „zamek‑i‑klucz” może wyjaśnić, skąd pochodzi wirus, jak się zaadaptował i co może się wydarzyć, gdy pokrewne wirusy przeskoczą na ludzi w przyszłości. 
Przyglądając się wirusowemu uściskowi dłoni
Badanie koncentruje się na białku kolca, koronie wirusa, która chwyta ACE2. Mały obszar kolca, domena wiążąca receptor (RBD), działa jak czubek palca chwytający „klamkę” ACE2. Wcześniejsze prace wykazały, że gdy koronawirusy przeskakują między gatunkami — na przykład z nietoperzy na cywety, a potem na ludzi — RBD często zdobywa mutacje poprawiające uchwyt do ACE2 nowego gospodarza. SARS-CoV-2 stawiał jednak zagadkę: jego pierwotna forma już bardzo dobrze wiązała ludzki ACE2, nawet zanim minęło dużo czasu na adaptację, a niektóre wirusy nietoperzy spokrewnione z SARS-CoV-2 wydawały się wiązać ludzki ACE2 lepiej niż nietoperzy ACE2. Skłoniło to niektórych do zastanowienia się, czy SARS-CoV-2 nie jest wyjątkiem od zwykłych reguł ewolucyjnych.
Testując receptory nietoperzy i ludzi
Aby zbadać tę zagadkę, badacze przeanalizowali dwa koronawirusy nietoperzy blisko spokrewnione z SARS-CoV-2, znane jako BANAL-52 i BANAL-236. Porównali, jak silnie RBD tych wirusów i SARS-CoV-2 przyczepiają się do ACE2 pochodzącego od ludzi oraz od kilku gatunków nietoperzy. Korzystając z badań wiązania w komórkach, wysokoprecyzyjnych pomiarów biosensorowych i testów zakażeń z użyciem nieszkodliwych „pseudowirusów”, odkryli wyraźny wzorzec. RBD BANAL-52 wiązał najsilniej ACE2 jednego gatunku nietoperza, Rhinolophus sinicus, a nieco słabiej ludzki ACE2. RBD SARS-CoV-2 natomiast wykazywał umiarkowaną preferencję dla ludzkiego ACE2 nad nietoperzym ACE2. Ogólnie RBD BANAL-52 wiązał zarówno receptory nietoperzy, jak i ludzkie mocniej niż RBD SARS-CoV-2, ale był najsilniej dopasowany do konkretnego nietoperzego ACE2. 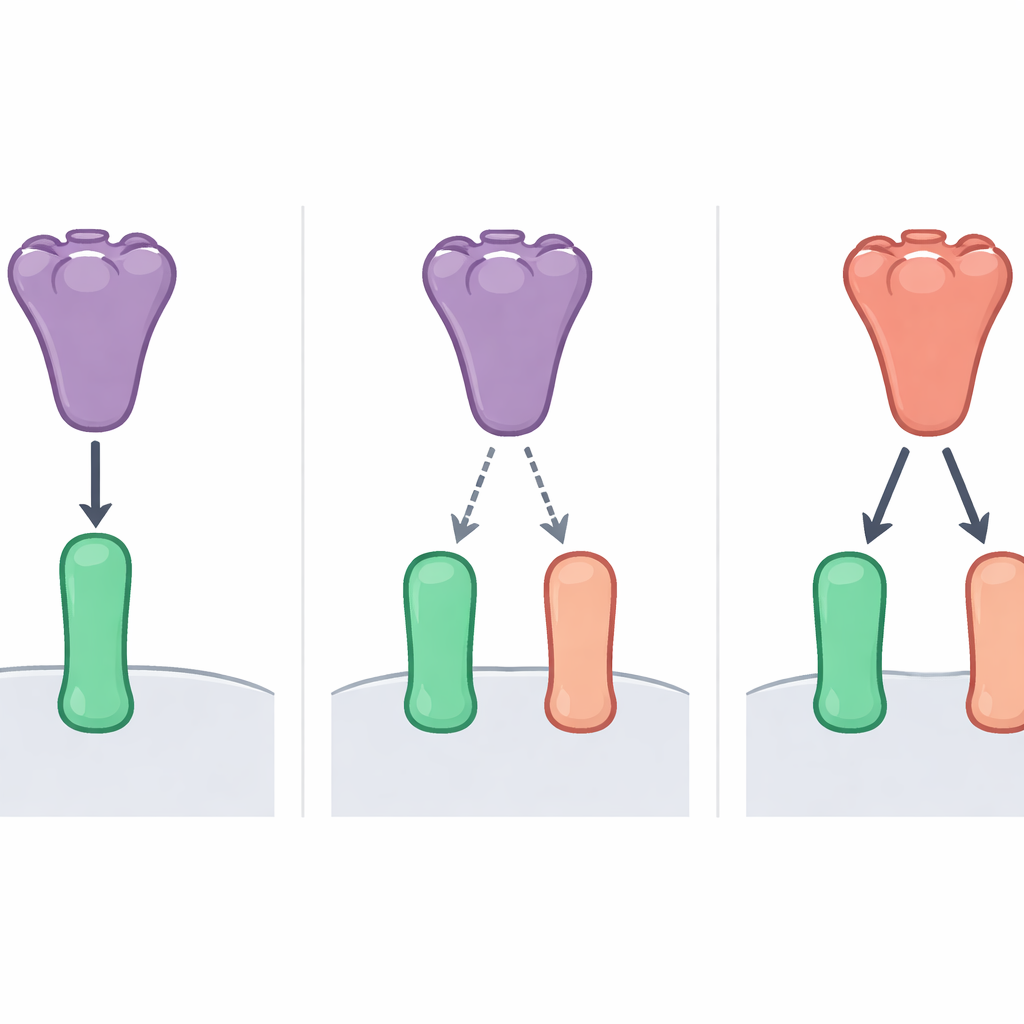
Jak pojedyncza zmiana na poziomie atomowym przechyla szalę
Zespół sięgnął następnie po krystalografię rentgenowską, która ujawnia struktury na poziomie atomowym, aby zobaczyć dokładnie, jak wirusowy „palec” i ACE2 „klamka” stykają się ze sobą. Skupili się na dwóch kluczowych miejscach: jednym w RBD wirusa (zwanym resztą 498) i jednym w ACE2 (resztą 41). W BANAL-52 zarówno miejsce wirusowe, jak i miejsce na nietoperzym ACE2 używają tego samego składnika budulcowego, histydyny, co pozwala na bardzo ciasną, warstwową interakcję — układanie się jak dwie monety i dodatkowe wiązanie wodorowe. W ludzkim ACE2 to samo miejsce zawiera pokrewny, lecz nieco inny składnik — tyrozynę, która nadal dobrze się układa z histydyną BANAL-52, ale pozbawiona jest dodatkowego wiązania wodorowego. SARS-CoV-2 zamiast tego używa glutaminy w tej pozycji wirusowej, która nie może układać się w ten sam sposób, co skutkuje słabszym wiązaniem zarówno z ACE2 nietoperzy, jak i ludzi. Celowa zamiana tych aminokwasów w nietoperzym ACE2 potwierdziła, że wzmocnienie lub osłabienie tego jednego punktu kontaktu może odwrócić preferencję wirusa lub gospodarza.
Dlaczego ludzki ACE2 jest tak gościnnymi drzwiami
Ponad ten pojedynczy kontakt autorzy zapytali, dlaczego ogólnie ludzki ACE2 jest tak efektywną bramą dla koronawirusów. Porównując ACE2 nietoperzy i ludzi obok siebie, zidentyfikowali kilka cech specyficznych dla ludzi, które poprawiają wirusowy uścisk. Dwie pozycje w ludzkim ACE2, zawierające aminokwasy histydynę (na miejscu 34) i metioninę (na miejscu 82), tworzą silniejsze wiązania wodorowe i „tłuste” powierzchnie, które pomagają RBD wirusa osadzić się bardziej pewnie. Inna ludzka reszta, treonina na pozycji 27, faktycznie nieco osłabia wiązanie w porównaniu z wersją nietoperzą, ale ogólnie dodatkowe korzystne kontakty przeważają. Te szczegóły pasują do wcześniejszych badań pokazujących, że ludzki ACE2 ma wiele „gorących punktów”, które naturalnie czynią go atrakcyjnym receptorem dla szerokiego spektrum koronawirusów.
Przeformułowanie historii pochodzenia
Sumując wszystkie dane, badanie argumentuje, że SARS-CoV-2 i jego nietoperze krewni nadal podążają zwykłym scenariuszem ewolucyjnym. Kolce BANAL-52 wydają się najlepiej przystosowane do ACE2 pewnych nietoperzy, jednocześnie będąc kompatybilnymi z ludzkim ACE2. Kolce SARS-CoV-2 z kolei są lepiej dostrojone do ludzkiego ACE2 niż do nietoperzego, wspomagane przez specyficzne punkty kontaktowe na receptorze ludzkim. Małe zmiany w zaledwie kilku pozycjach — szczególnie w reszcie wirusowej 498 i sąsiednich miejscach — mogą przesunąć równowagę, który gospodarz jest preferowany. Dla osób niebędących specjalistami wniosek jest taki, że nie ma potrzeby odwoływać się do egzotycznych wyjaśnień: standardowe, dobrze rozumiane zasady strukturalne interakcji białko–białko wystarczają, by wyjaśnić, jak te wirusy rozpoznają komórki nietoperzy i ludzi, i wspierają bliskie pokrewieństwo ewolucyjne między SARS-CoV-2 a spokrewnionymi koronawirusami nietoperzy.
Cytowanie: Hsueh, FC., Shi, K., Aihara, H. et al. Structural basis for bat receptor recognition by SARS-CoV-2 and bat SARS2-like coronaviruses. Commun Biol 9, 398 (2026). https://doi.org/10.1038/s42003-026-09682-z
Słowa kluczowe: ewolucja SARS-CoV-2, koronawirusy nietoperzy, receptor ACE2, zakres gospodarzy wirusa, wiązanie białka kolca