Clear Sky Science · pl
Wirus afrykańskiego pomoru świń — białko kodowane MGF 505–3R osłabia odporność wrodzoną poprzez ubikwitynację MyD88 i jego degradację
Dlaczego to ma znaczenie dla zdrowia zwierząt i nie tylko
Afrykański pomór świń zdziesiątkował gospodarstwa hodowlane na całym świecie, zagrażając bezpieczeństwu żywnościowemu i powodując ogromne straty ekonomiczne. Wirus odpowiadający za chorobę jest śmiertelny częściowo dlatego, że potrafi ominąć wczesne systemy alarmowe organizmu. W badaniu odkryto, w jaki sposób jeden z białkowych produktów wirusa, nazywany MGF 505–3R, potajemnie sabotuje kluczowy przełącznik alarmowy w komórkach oraz pokazano, że niewielki fragment tego białka można przekształcić w silne narzędzie przeciwzapalne u myszy.
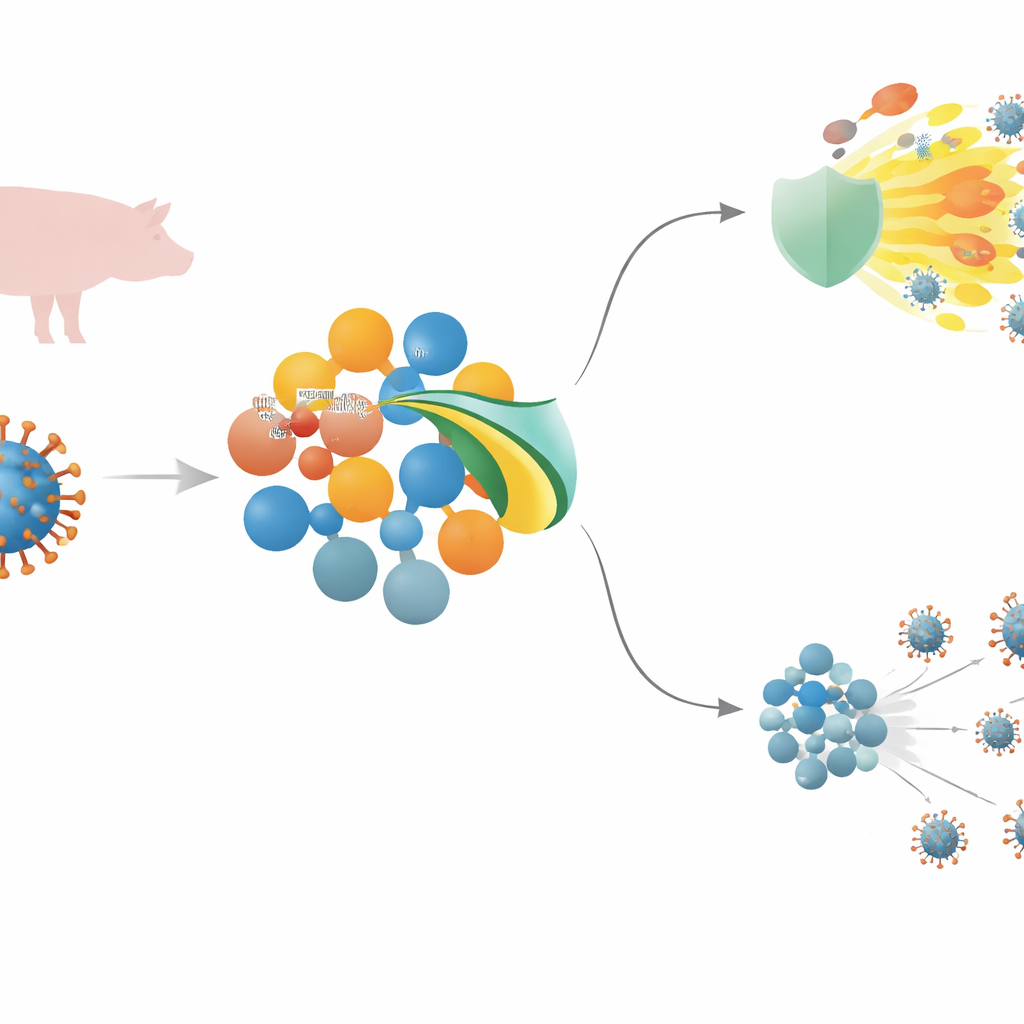
Śmiertelny wirus świń i pierwsza linia obrony organizmu
Wirus afrykańskiego pomoru świń (ASFV) to duży wirus z materiałem genetycznym w postaci DNA, który może zabić niemal każde zakażone zwierzę. Aby się utrzymać, musi przechytrzyć odporność wrodzoną — szybką, frontową linię obrony, która wykrywa intruzów i wywołuje stan zapalny oraz produkcję cząsteczek przeciwwirusowych. W centrum tej odpowiedzi znajduje się szlak sygnałowy obejmujący sensory na powierzchni komórki, białko przekaźnikowe MyD88 oraz główny przełącznik NF–κB, które wspólnie napędzają produkcję mediatorów zapalnych i interferonów przeciwwirusowych. ASFV niesie wiele genów uważanych za zakłócające te sygnały, jednak mechanizmy działania kilku z nich, w tym MGF 505–3R, nie były wcześniej dobrze poznane.
Jak wirus przecina przewody alarmu immunologicznego
Naukowcy przebadali białka ASFV pod kątem zdolności do tłumienia aktywności NF–κB i odkryli, że MGF 505–3R jest szczególnie silnym inhibitorem. W obecności tego białka wirusowego komórki wystawione na różne bodźce immunologiczne produkowały znacznie mniej cytokin prozapalnych oraz dużo niższe ilości interferonów typu I i III. Dokładniejsza analiza wykazała, że MGF 505–3R działa bezpośrednio na MyD88 — centralny adapter łączący wiele sensorów immunologicznych z NF–κB. MGF 505–3R wiąże MyD88 i oznacza je do usunięcia za pośrednictwem komórkowego systemu rozkładu białek, poprzez modyfikację ubikwitynową typu K48. W miarę degradacji MyD88, NF–κB nie jest w stanie przemieścić się do jądra i włączyć ochronnych genów, co sprawia, że komórki stają się bardziej podatne na replikację wirusa.
Zbliżenie na niewielki, lecz potężny fragment białka
Aby zidentyfikować kluczowy fragment MGF 505–3R, zespół skonstruował skrócone wersje białka i przetestował ich działanie. Odkryli, że aminokwasy 89–277 są zarówno niezbędne, jak i wystarczające do wiązania MyD88, promowania jego ubikwitynacji oraz blokowania aktywacji NF–κB. Kierując się przewidywaniami komputerowymi struktury białka, wyizolowali dwa krótkie peptydy z tego regionu. Jeden z nich, pep3R–1, wyróżniał się: silnie obniżał aktywność NF–κB, blokował fosforylację i przemieszczenie do jądra podjednostki p65 NF–κB oraz zmniejszał ekspresję cytokin zapalnych i interferonów w komórkach odpornościowych stymulowanych różnymi sygnałami zagrożenia. W hodowlach komórkowych zarówno pełnej długości MGF 505–3R, jak i pep3R–1 nie tylko tłumiły sygnalizację przeciwwirusową, lecz także umożliwiały testowemu wirusowi bardziej efektywną replikację, podkreślając siłę tego szlaku w kontroli zakażeń.
Przekształcenie wirusowego chytrego triku w potencjalny lek
Zespół sprawdził następnie, czy peptyd można wykorzystać do ukojenia szkodliwego zapalenia zamiast wspomagać wirusy. W modelu myszy z zapaleniem jelita wywołanym związkiem chemicznym DSS, zwierzęta zwykle tracą na wadze, rozwijają krwawą biegunkę i wykazują poważne uszkodzenia oraz nacieki komórek odpornościowych w jelicie grubym. Myszy traktowane pep3R–1 radziły sobie znacznie lepiej: wskaźniki choroby były niższe, jelita grube były dłuższe i zdrowsze, a badanie mikroskopowe ujawniło zachowaną strukturę tkanek z znacznie mniejszą liczbą komórek zapalnych. Poziomy kluczowych cząsteczek zapalnych, takich jak TNF–α, IL–1β, IL–6, oraz enzymu związanego z napływem białych krwinek, były zmniejszone w tkance jelita i we krwi. W odrębnym eksperymencie pep3R–1 również złagodził odpowiedź zapalną na ogólnoustrojową toksynę bakteryjną, co wskazuje, że może tłumić zarówno miejscowe, jak i uogólnione burze zapalne.
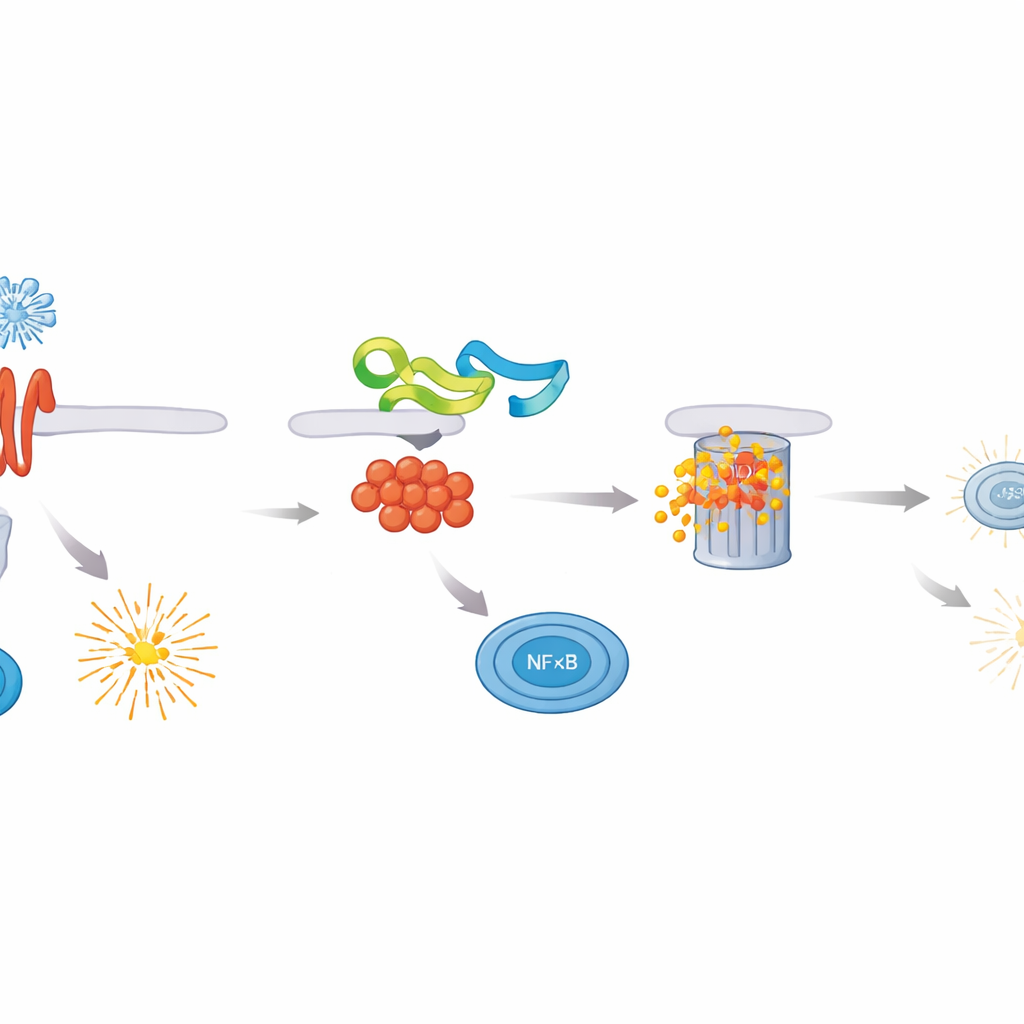
Co to oznacza dla świń, ludzi i przyszłych terapii
Badanie pokazuje, że białko ASFV MGF 505–3R pomaga wirusowi przetrwać, rozmontowując centralny przekaźnik immunologiczny MyD88, tym samym wyłączając zarówno obronę zapalną, jak i interferonową. Jednocześnie niewielki fragment tego białka, pep3R–1, można zaadaptować do bezpiecznego łagodzenia nadmiernego zapalenia u myszy, w tym w modelu choroby jelit. Chociaż pozostaje wiele do zrobienia — na przykład poprawa stabilności, dostarczania i testy w dodatkowych modelach chorobowych — badanie ujawnia zarówno krytyczny słaby punkt, który można wykorzystać w strategiach przeciwwirusowych, jak i obiecujący wzorzec do projektowania nowych peptydowych leków przeciwzapalnych inspirowanych wirusowymi mechanizmami unikania odporności.
Cytowanie: Liu, H., Sun, L., Wang, F. et al. African swine fever virus–encoded protein MGF 505–3R impairs innate immunity via ubiquitin–mediated degradation of MyD88. Commun Biol 9, 407 (2026). https://doi.org/10.1038/s42003-026-09681-0
Słowa kluczowe: afrykański pomór świń, odporność wrodzona, NF-kappaB, MyD88, peptyd przeciwzapalny