Clear Sky Science · pl
Nieprawidłowa homeostaza żelaza pośredniczy w uszkodzeniu komórek rzęsowych ślimaka i utracie słuchu u myszy pozbawionych Gprasp2
Dlaczego to ma znaczenie dla codziennego słyszenia
Utratę słuchu często upraszcza się do „zużycia”, lecz u wielu osób podłożem są ukryte defekty genetyczne. Badanie to ujawnia, jak rzadko badany gen GPRASP2 chroni delikatne komórki odbierające dźwięk w uchu wewnętrznym przed uszkodzeniem wywołanym przez żelazo. Pokazując dokładnie, co się dzieje, gdy ten gen jest nieobecny, praca otwiera drogę do precyzyjniejszych diagnoz i przyszłych terapii dziedzicznych problemów ze słuchem, a być może także związanych zaburzeń nastroju.
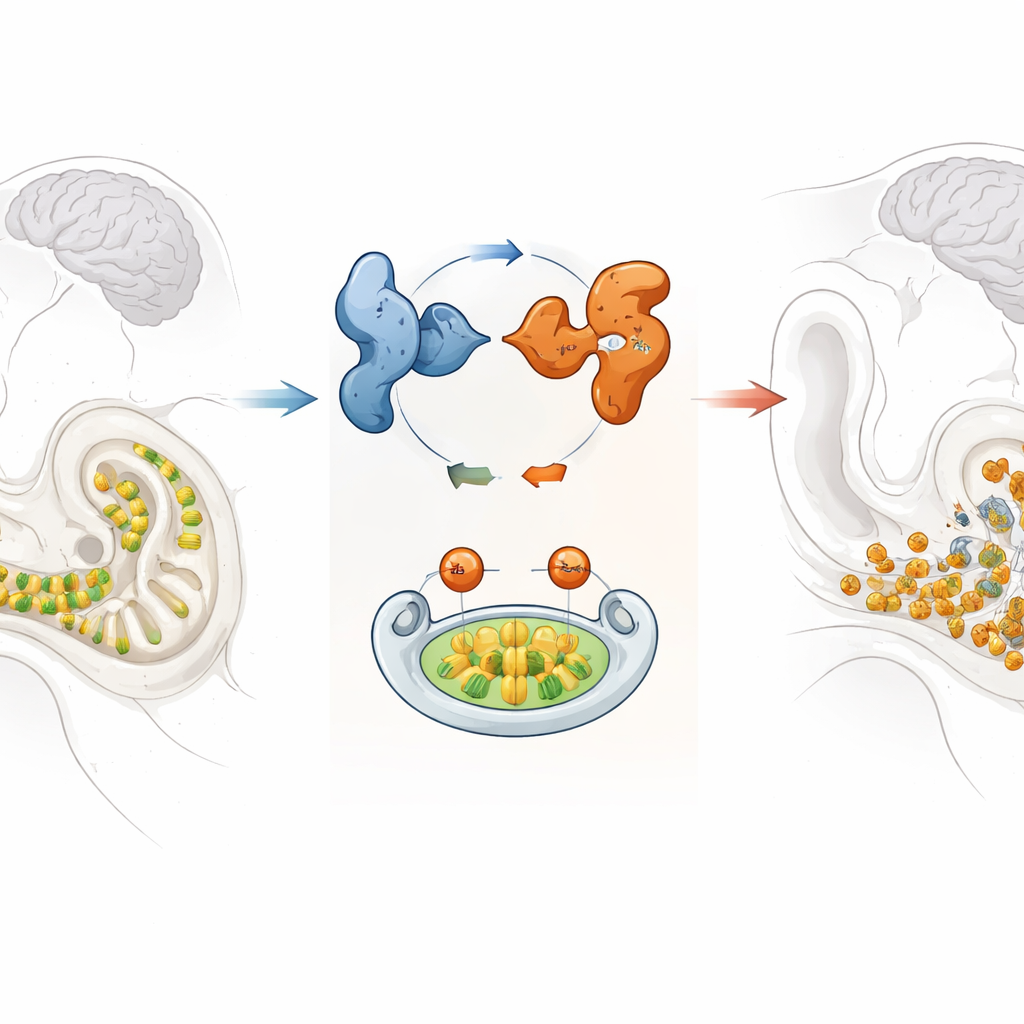
Delikatny czujnik dźwięku w uchu wewnętrznym
W skręconym ślimaku ucha wewnętrznego znajdują się rzędy komórek rzęsowych, które przekształcają mikrowibracje w sygnały elektryczne zrozumiałe dla mózgu. Gdy te komórki zginą, nie odrastają, dlatego utrzymanie ich w dobrej kondycji jest kluczowe dla słyszenia przez całe życie. Badacze skupili się na GPRASP2, genie wcześniej wykrytym jako zmieniony w rodzinie z zespołową, sprzężoną z chromosomem X utratą słuchu, co oznacza, że schorzenie dotyka głównie mężczyzn i może towarzyszyć mu dodatkowy zestaw objawów. Chociaż wiadomo było, że GPRASP2 jest aktywny w mózgu i uchu wewnętrznym, jego dokładna rola w słyszeniu pozostawała niejasna.
Co się dzieje, gdy gen jest nieobecny
Aby naśladować stan ludzki, zespół zastosował edycję genów CRISPR do stworzenia myszy pozbawionych działającej kopii Gprasp2. Zwierzęta te wykazały wyraźną utratę słuchu w szerokim zakresie częstotliwości przy badaniach czułymi zapisami elektrycznymi z nerwu słuchowego. Ich reakcje na nagłe głośne dźwięki były stłumione, natomiast równowaga i zdolności motoryczne były w większości normalne, co wskazuje na specyficzny problem ze słuchem, a nie ogólne zaburzenie ruchowe. Co ciekawe, myszy wykazywały także zachowania przypominające depresję w kilku standardowych testach, sugerując, że ten gen łączy słuch i nastrój przez swoje działania zarówno w uchu, jak i w mózgu.
Uszkodzenia wewnątrz ślimaka
Po zbadaniu uszu wewnętrznych myszy pozbawionych Gprasp2 naukowcy stwierdzili brak lub przemieszczenie wielu zewnętrznych komórek rzęsowych, a pozostałe komórki często miały zdeformowane wiązki drobnych projekcji, które normalnie działają jak stroiki. Zaobserwowano także zmiany w strii waskularis, wysoce aktywnej tkance utrzymującej specjalny płyn i środowisko elektryczne niezbędne do słyszenia. Na poziomie mikroskopowym markery śmierci komórkowej i stresu oksydacyjnego były podwyższone w zewnętrznych komórkach rzęsowych oraz pobliskich komórkach nerwowych, co wskazuje, że te struktury były silnie atakowane przez reaktywne cząsteczki i miały zwiększoną skłonność do obumierania.
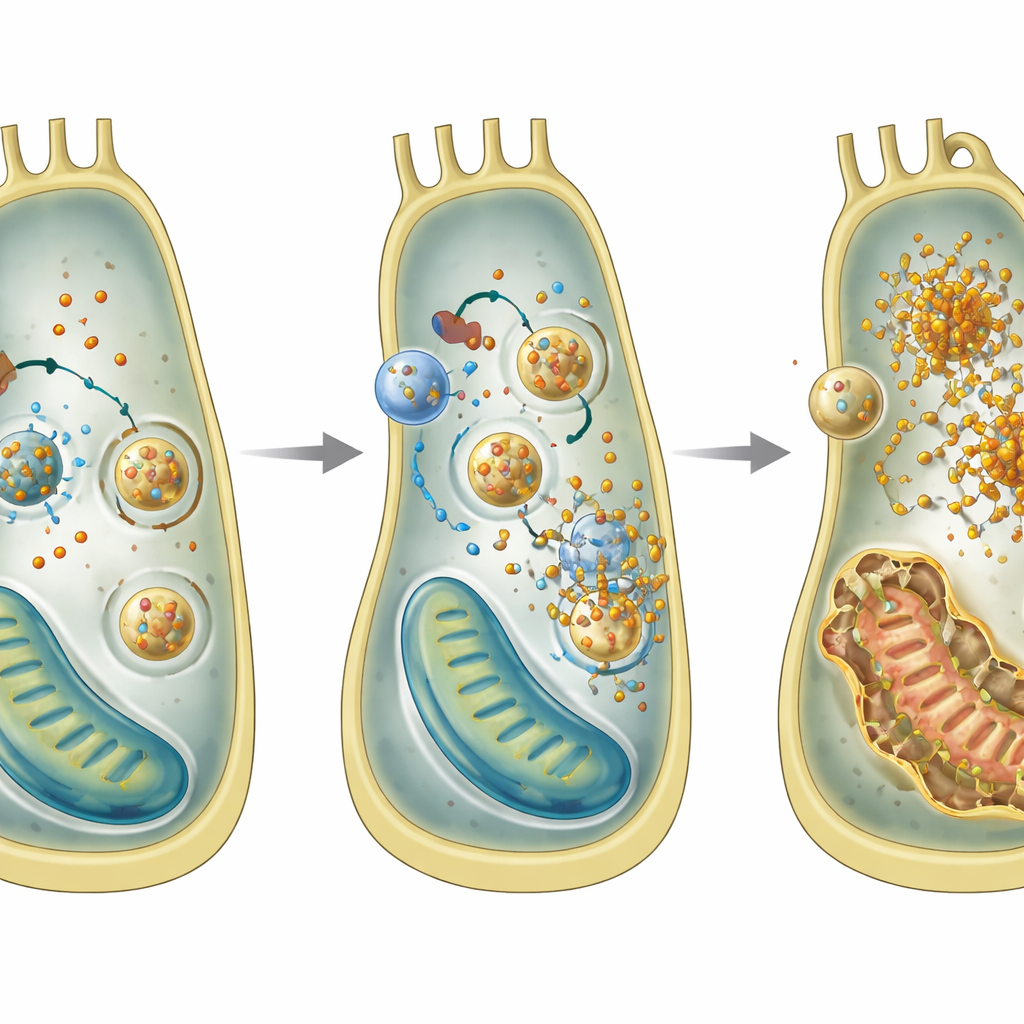
Przeciążenie żelazem i wymknięty recykling
Zagłębiając się dalej, zespół użył linii komórkowej z ucha wewnętrznego, by zbadać, co szwankuje w pojedynczych komórkach pozbawionych GPRASP2. Odkryli wzorzec charakterystyczny dla formy śmierci komórkowej zwanej ferroptozą, napędzanej przez żelazo i peroksydację lipidów. Komórki bez Gprasp2 gromadziły więcej żelaza dwuwartościowego, produkowały więcej reaktywnych form tlenu, miały niższe poziomy przeciwutleniającej glutationu i wykazywały uszkodzenia mitochondriów. Analizy genów i białek wskazywały na nasiloną ferritinofagię — proces, w którym cząsteczki magazynujące żelazo trafiają do kompartamentów recyklingu i są rozkładane, uwalniając dodatkowe żelazo do komórki. Zablokowanie tego kroku recyklingu zmniejszało nagromadzenie żelaza, wspierając koncepcję, że nadmierna ferritinofagia jest kluczowa dla uszkodzeń.
Kluczowe białko partnerujące, które pilnuje żelaza
Następnie badacze zapytali, jak GPRASP2 kontroluje ten system gospodarowania żelazem. Mapując białka wchodzące w interakcje z GPRASP2, zidentyfikowali NCAM1 — cząsteczkę adhezji komórkowej znaną przede wszystkim z ról w uczeniu się, pamięci i nastroju. Pokazali, że GPRASP2 wiąże się fizycznie z NCAM1, a utrata GPRASP2 powoduje spadek poziomów NCAM1 w komórkach rzęsowych i w hodowlanych komórkach słuchowych. Niższe poziomy NCAM1 były powiązane ze zwiększoną ferritinofagią i przeciążeniem żelazem. Przywrócenie NCAM1 w komórkach pozbawionych Gprasp2 obniżyło poziomy żelaza i stłumiło kluczowych regulatorów ferritinofagii, mimo że ogólna autofia pozostała aktywna. Sugeruje to, że GPRASP2 precyzyjnie dostraja specyficzną ścieżkę recyklingu żelaza przez NCAM1, zamiast włączać lub wyłączać cały system recyklingu.
Co to oznacza dla słuchu i nie tylko
Mówiąc wprost, praca ta pokazuje, że GPRASP2 pełni rolę menedżera bezpieczeństwa dla żelaza w komórkach rzęsowych ślimaka. Gdy GPRASP2 jest obecny, współpracuje z NCAM1, by zapobiegać nadmiernemu uwalnianiu zmagazynowanego żelaza do wnętrza komórki, utrzymując pod kontrolą uszkodzenia oksydacyjne. Gdy gen jest zaburzony, gospodarka żelazem wymyka się równowadze, komórki „rdzewieją” od wewnątrz, kluczowe komórki rzęsowe obumierają, prowadząc do utraty słuchu. Ponieważ GPRASP2 i NCAM1 funkcjonują także w mózgu, ta sama ścieżka może pomagać wyjaśnić zmiany nastroju obserwowane u niektórych pacjentów. Zrozumienie tego trybu awarii zależnej od żelaza daje wyraźny cel dla przyszłych leków lub terapii genowych mających na celu zachowanie słuchu u osób z zaburzeniami związanymi z GPRASP2 lub podobnymi genetycznymi defektami.
Cytowanie: Lu, Y., Sheng, F., Yao, J. et al. Abnormal iron homeostasis mediates cochlear hair cell impairment and hearing loss in Gprasp2-deficient mice. Commun Biol 9, 425 (2026). https://doi.org/10.1038/s42003-026-09679-8
Słowa kluczowe: dziedziczna utrata słuchu, komórki rzęsowe ślimaka, homeostaza żelaza, ferroptoza, GPRASP2