Clear Sky Science · pl
Praktyczny przewodnik po ukierunkowanych technologiach pojedynczokomórkowego sekwencjonowania RNA
Dlaczego warto przyglądać się pojedynczym komórkom
Każda komórka w organizmie zawiera tę samą DNA, a mimo to różne komórki zachowują się bardzo odmiennie. Osiągają to przez włączanie lub wyłączanie konkretnych genów oraz przez subtelne modyfikacje cząsteczek RNA. Współczesne techniki pojedynczokomórkowego sekwencjonowania RNA potrafią odczytać, które RNA są obecne w tysiącach komórek jednocześnie, ale aktualnie przepuszczają większość przekazu. Niniejszy przegląd wyjaśnia, gdzie współczesne metody tracą informacje i jak nowe metody „ukierunkowane” są rozwijane, by przybliżyć najważniejsze fragmenty cząsteczek RNA dla badań, diagnostyki i projektowania terapii.
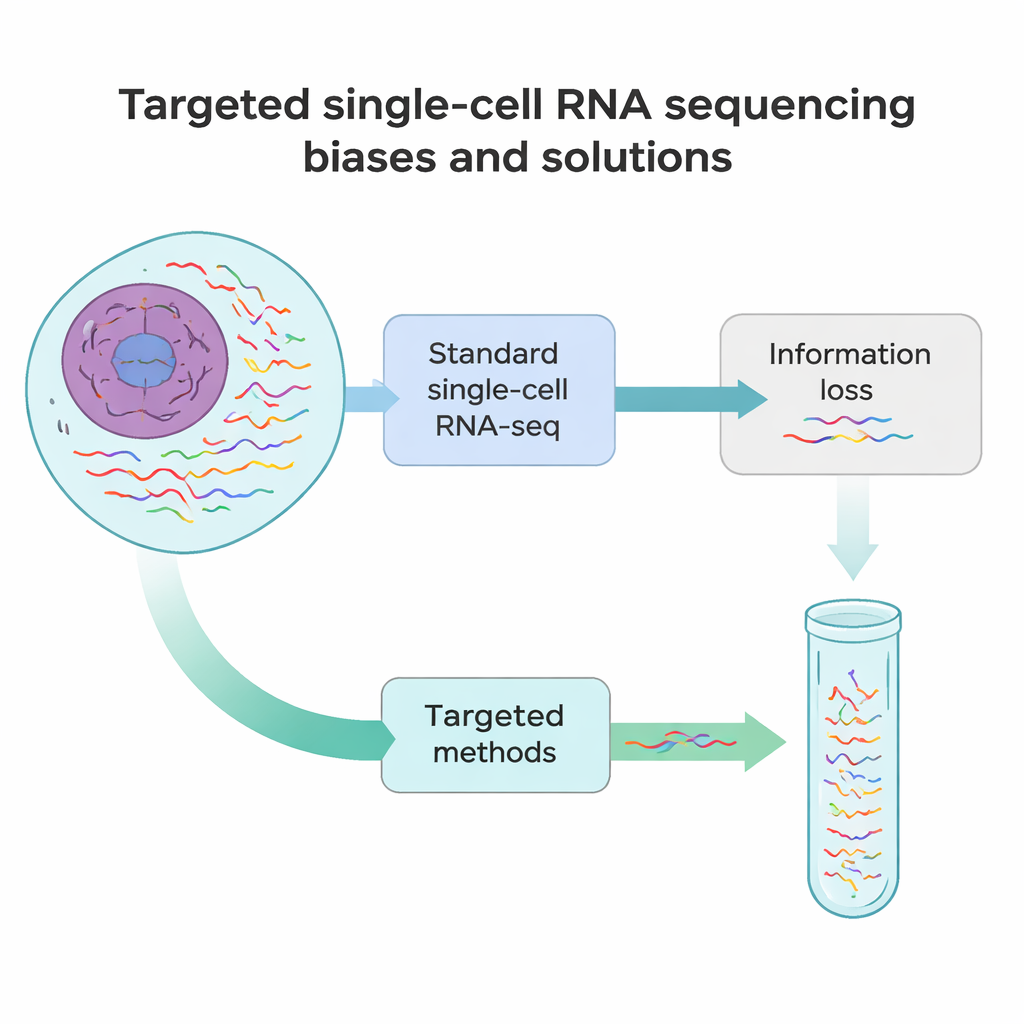
Gdzie współczesne metody zawodzą
Standardowe pojedynczokomórkowe sekwencjonowanie RNA działa trochę jak szybkie zdjęcie każdego komunikatu zamiast pełnometrażowego filmiku. W większości eksperymentów wykrywane jest tylko około 10–40% wszystkich RNA w komórce, i odczytywane są jedynie ich początki lub końce. Oznacza to, że wiele rzadkich, lecz istotnych RNA — takich jak markery definiujące tożsamość komórki czy warianty genów niosące mutacje chorobotwórcze — może zostać łatwo przeoczonych. Dodatkowo kilka etapów technicznych, od rozdzielania tkanek na pojedyncze komórki po konwersję RNA na DNA i amplifikację, wprowadza systematyczne uprzedzenia. Niektóre RNA są przycinane wcześnie, inne są nadreprezentowane, a jeszcze inne znikają całkowicie z danych.
Dlaczego wewnętrzne szczegóły RNA mają znaczenie
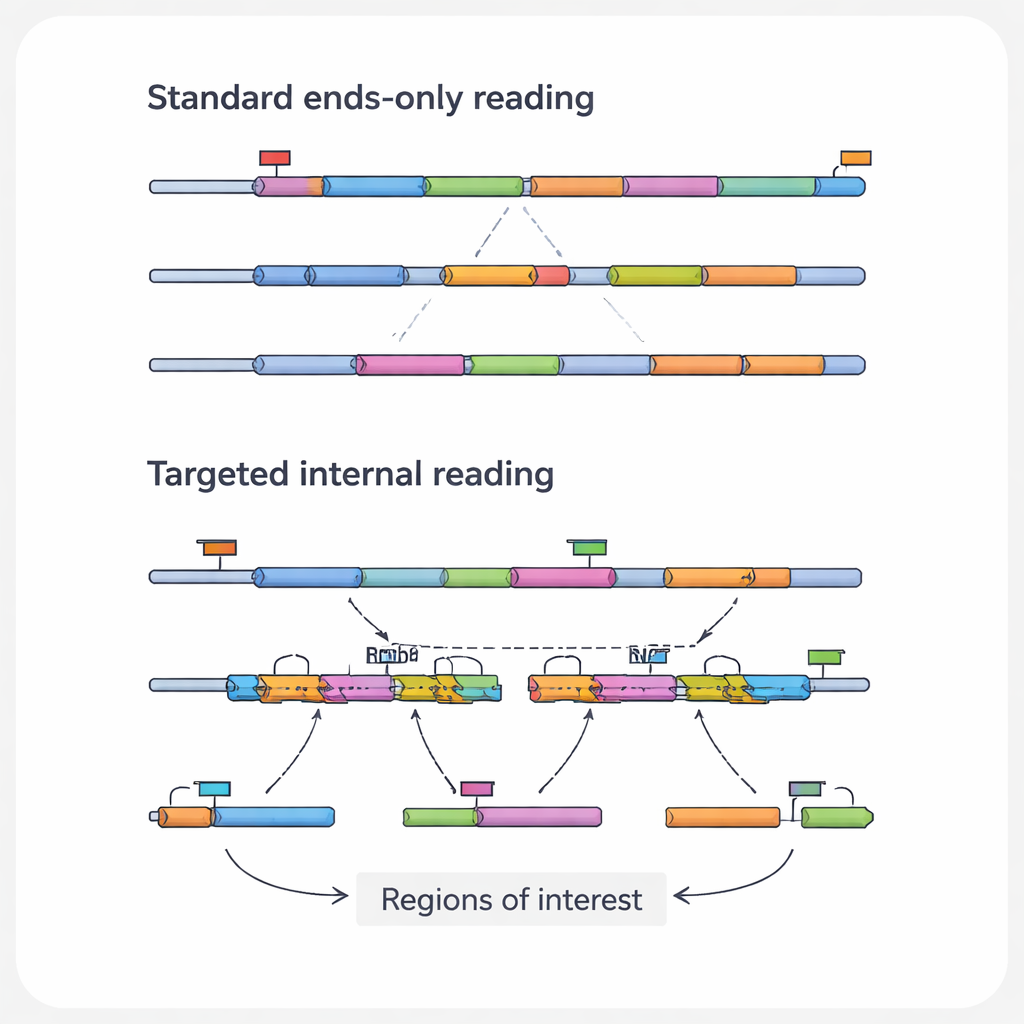
Najnowsze informacje o znaczeniu medycznym w cząsteczce RNA często znajdują się w jej wewnętrznych regionach, a nie na końcach widocznych dla standardowych metod. Wewnętrzne fragmenty mogą zawierać mutacje punktowe napędzające nowotworzenie, punkty fuzji, gdzie dwa geny zostały nienormalnie połączone, lub miejsca splicingu tworzące różne warianty białek z tego samego genu. Mogą też zachowywać ślady działania narzędzi do edycji genów, takich jak CRISPR. Autorzy nazywają te konkretnie istotne cechy „obszarami zainteresowania”, a RNA je niosące „transkryptami zainteresowania”. Ponieważ popularne platformy wysokoprzepustowe głównie odczytują końcówki RNA, rutynowo pomijają te kluczowe szczegóły, szczególnie w przypadku długich lub niskoobfitych transkryptów.
Nowe sposoby skierowania światła
Aby pokonać te martwe pola, badacze opracowali zestaw ukierunkowanych podejść do pojedynczokomórkowego sekwencjonowania RNA. Zamiast próbować odczytać każde RNA jednakowo, metody te celowo wzbogacają wybrane transkrypty lub regiony. Niektóre strategie przeprojektowują kulki chwytające, tak aby wiązały wewnętrzne sekwencje RNA, a nie tylko ogon poli(A), przyciągając wybrane wiadomości do biblioteki już na pierwszym etapie. Inne dodają niestandardowe startery, które zaczynają kopię od wnętrza, albo dodatkowe etapy PCR, które specyficznie amplifikują krótką listę genów z istniejącej biblioteki. Jeszcze inne wykorzystują sondy DNA hybrydyzujące z docelowymi RNA lub ich kopiami, a następnie wyłapują je, często przy użyciu prostych znaczników chemicznych. Każda kategoria wiąże się z kompromisem między czułością, liczbą komórek, liczbą celów i kosztem, ale wszystkie dążą do tego samego celu: odzyskać więcej znaczących szczegółów z tej samej lub mniejszej liczby odczytów sekwencyjnych.
Zastosowania od wirusów po guzy
Metody ukierunkowane już przekształcają kilka dziedzin biologii i medycyny. W infekcjach pozwalają wreszcie uchwycić wirusowe lub bakteryjne RNA, które nie mają ogonków poli(A), na które liczą standardowe protokoły, ujawniając, w których komórkach gospodarza się znajdują i jak zmieniają aktywność genów gospodarza. W onkologii ukierunkowane sekwencjonowanie pojedynczych komórek potrafi wskazać, które typy komórek niosą konkretne mutacje lub geny fuzyjne i powiązać je ze zmienionymi programami genowymi, pomagając wyjaśnić, dlaczego niektóre komórki stają się oporne na terapię. Inne metody koncentrują się na alternatywnym splicingu, ujawniając, które typy komórek używają jakich izoform, albo na rzadkich populacjach komórek i subtelnych markerach, które w przeciwnym razie pozostałyby poniżej progu detekcji. W pulowanych ekranach CRISPR lepsze wychwytywanie RNA przewodników pozwala naukowcom powiązać każdą perturbację genetyczną z jej precyzyjną odpowiedzią komórkową.
Wybór właściwego narzędzia i co dalej
Skoro istnieje teraz rozbudowane narzędziownia ukierunkowanych podejść, autorzy proponują drzewo decyzyjne, które ma pomóc badaczom wybrać metodę. Kluczowe pytania obejmują: czy potrzebne jest pełne profilowanie transkryptomu, ile genów lub regionów należy ukierunkować, jak daleko te regiony leżą od końców RNA oraz ile komórek można przetworzyć. Patrząc w przyszłość, autorzy uważają, że największe zyski przyniosą ulepszenia w samych pierwszych etapach wychwytu, rozwój pomysłowych strategii opartych na sondach oraz łączenie ukierunkowania z pojawiającymi się platformami długiego odczytu i bezpośredniego sekwencjonowania RNA. Dopóki nie stanie się praktyczne odczytywanie każdego RNA w każdej komórce od końca do końca, ukierunkowane pojedynczokomórkowe sekwencjonowanie RNA pozostanie niezbędne do ujrzenia tych części komórkowego przekazu, które mają największe znaczenie dla biologii i chorób.
Cytowanie: Moro, G., Brunner, E. & Basler, K. A practical guide to targeted single-cell RNA sequencing technologies. Commun Biol 9, 250 (2026). https://doi.org/10.1038/s42003-026-09675-y
Słowa kluczowe: sekwencjonowanie RNA pojedynczych komórek, sekwencjonowanie ukierunkowane, transkryptomika, mutacje nowotworowe, transkryptomika przestrzenna