Clear Sky Science · pl
Aktywacja kodowanego przez cytomegalowirus receptora sprzężonego z białkiem G UL33 przez wrodzony peptyd N‑końcowy
Jak powszechny wirus przeprogramowuje nasze komórki
Ludzki cytomegalowirus (HCMV) cicho zakaża większość ludzi na świecie i zazwyczaj pozostaje bezobjawowy. Jednak u noworodków, biorców przeszczepów i osób z osłabionym układem odpornościowym może powodować poważne choroby. Badanie to ujawnia w skali molekularnej, jak jeden wirusowy białko zwane UL33 działa jak wbudowany przełącznik, który nieustannie skłania zainfekowane komórki do sprzyjania wirusowi. Zrozumienie tego ukrytego przełącznika pomaga wyjaśnić, jak HCMV utrzymuje się przez całe życie i wskazuje nowe sposoby unieszkodliwienia go bez zakłócania normalnej sygnalizacji komórek.
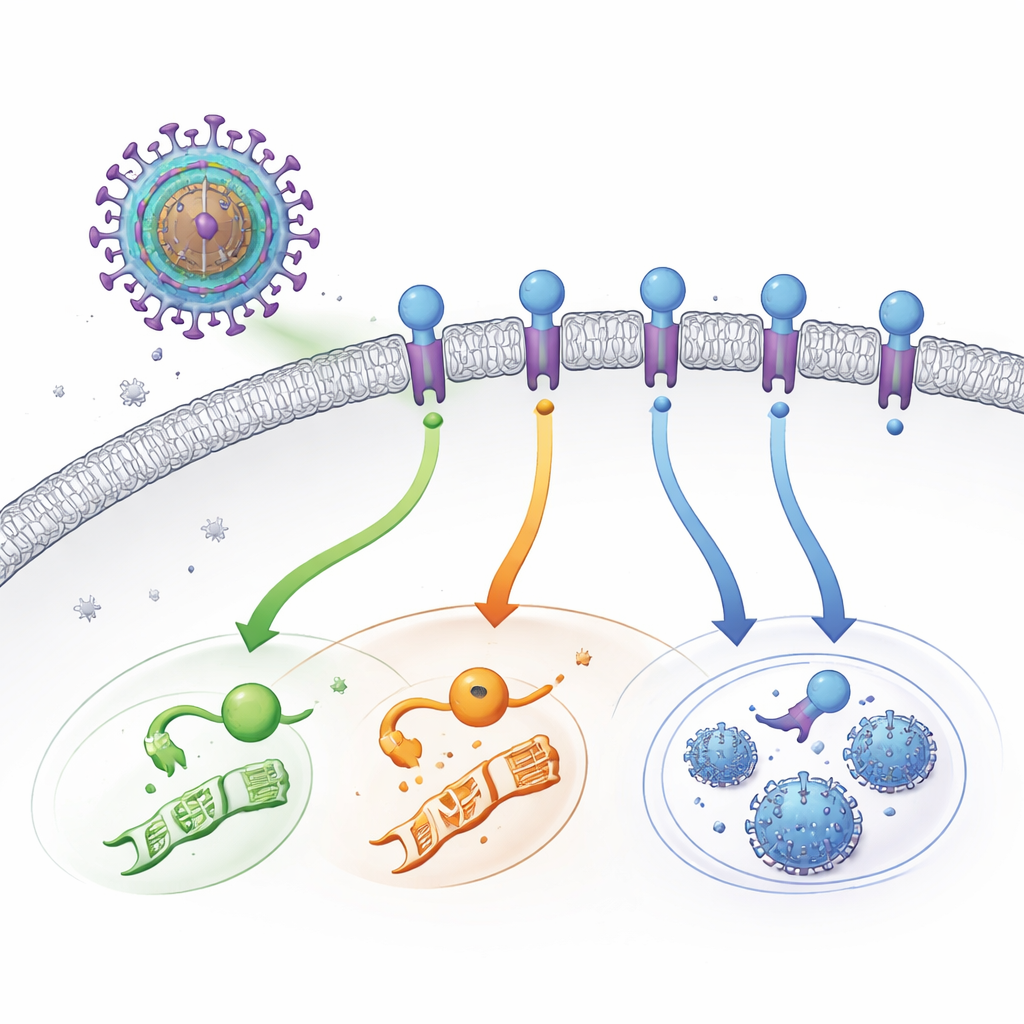
Podstępny wirusowy przełącznik na powierzchni komórki
HCMV nosi własne wersje receptorów powierzchni komórkowej — białek, które normalnie wykrywają hormony lub sygnały odpornościowe. UL33 jest jednym z tych wirusowych receptorów. W przeciwieństwie do typowych receptorów, które czekają na zewnętrzny sygnał, UL33 jest „zawsze włączony”. Po umieszczeniu w błonie zewnętrznej zainfekowanej komórki może jednocześnie podłączyć się do kilku głównych szlaków komunikacyjnych komórki. Szlaki te kontrolują procesy takie jak aktywność genów, metabolizm oraz decyzję o pozostaniu w stanie utajenia lub produkcji nowych wirionów. Przez lata naukowcy wiedzieli, że UL33 jest aktywny, ale nie wiedzieli, co go uruchamia, zwłaszcza że nigdy nie znaleziono zewnętrznej cząsteczki aktywującej (ligandu).
Samorzutnik: receptor, który przynosi własny klucz
Wykorzystując zaawansowaną krioelektronową mikroskopię (cryo‑EM), autorzy uchwycili trójwymiarowe migawki UL33 związanej z jednym z partnerów sygnalizacyjnych komórki, białkiem G o nazwie Gs. Obrazy pokazują, że sam początek białka UL33 — jego krótki ogon N‑końcowy — składa się z powrotem do kieszeni na samym receptorze, niczym klucz pozostawiony na stałe w zamku. Ten „przytwierdzony” ogon umiejscawia się w małej bocznej kieszeni, która w pokrewnych ludzkich receptorach normalnie przyjmowałaby część białka sygnalizacyjnego zwanego chemokiną. Zajmując tę kieszeń od wewnątrz, UL33 blokuje wiązanie zewnętrznych chemokin, co tłumaczy, dlaczego zachowuje się jak receptor „sierota”, nieodpowiadający na zwykłe sygnały gospodarza.
Krytyczne atomy w wirusowym wyłączniku
Aby potwierdzić, że ten wbudowany ogon rzeczywiście jest wyzwalaczem, zespół systematycznie modyfikował pojedyncze elementy budulcowe UL33 w komórkach ludzkich. Skoncentrowali się na pierwszych kilku aminokwasach ogona oraz na odpowiadających im miejscach wewnątrz kieszeni, które je chwytają. Gdy zamieniali te kluczowe reszty na bardziej obojętne lub usuwali jedną z nich całkowicie, zdolność UL33 do przekazywania sygnału spadała niemal do zera — mimo że zmodyfikowane receptory nadal docierały do powierzchni komórki w normalnych ilościach. Innymi słowy, białko było obecne, lecz nieme. Pokazuje to, że ogon nie jest jedynie elementem strukturalnym; jest niezbędnym, samaktywującym się elementem, który utrzymuje UL33 w stanie aktywnym.
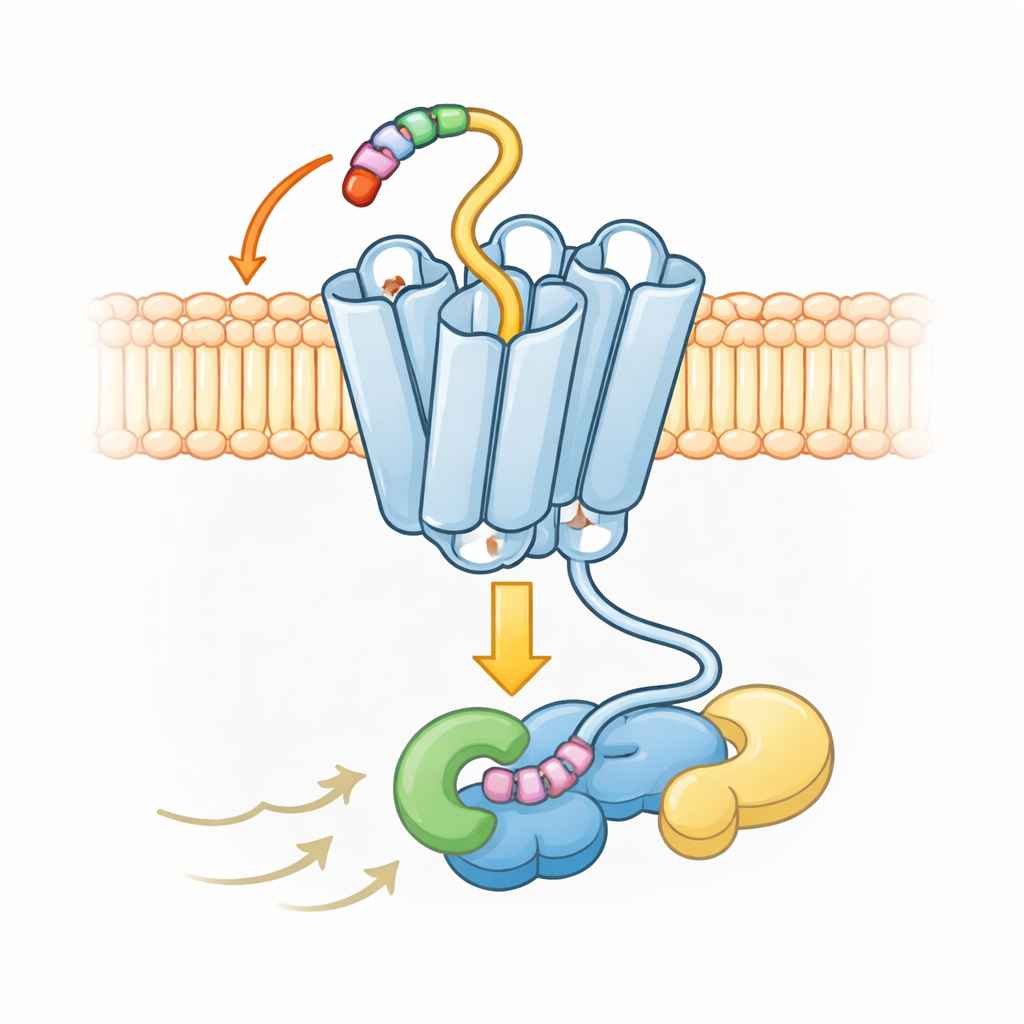
Nietypowy kształt dla szerokiej, lecz kontrolowanej sygnalizacji
Mapy strukturalne ujawniają również, że UL33 przyjmuje nieco inną aktywną konformację w porównaniu z typowymi ludzkimi receptorami. W większości receptorów z tej rodziny jedna z siedmiu helis położonych bliżej wnętrza komórki wychyla się znacząco na zewnątrz po aktywacji, otwierając dużą jamę dla dokowania białek G. W UL33 ta helisa pozostaje znacznie bliżej środka, tworząc ciaśniejsze dopasowanie. Mimo to UL33 potrafi wchodzić w interakcje z kilkoma rodzajami białek G — Gs, Gq i Gi — przez precyzyjne kontakty z końcówką białka G, która wsuwa się do receptora. Kontakty te faworyzują pewne białka G i wykluczają inne, takie jak grupa G12/13, co pozwala wirusowi stronniczo modulować odpowiedzi komórkowe bez wywoływania niekontrolowanej sygnalizacji.
Nowe słabe punkty starego wirusa
Łącząc obrazowanie strukturalne z testami funkcjonalnymi, badanie kreśli jasny obraz: UL33 jest samorozpoczynającym receptorom wirusowym, którego własny ogon działa jako trwale przytwierdzony aktywator. Ta konstrukcja pozwala HCMV łagodnie, ale trwale dostrajać sygnalizację komórkową gospodarza, by wspierać replikację wirusa i jego reaktywację, zwłaszcza poprzez wzmacnianie szlaków uruchamiających geny wirusowe. Jednocześnie praca ujawnia słabe punkty, które można by wykorzystać farmakologicznie, na przykład wąski tunel prowadzący do kieszeni, w której wiąże się ogon. Cząsteczki zaprojektowane tak, by klinować się w tym regionie albo wypchnąć ogon, mogłyby uciszyć aktywność UL33 i zmniejszyć szkody wyrządzane przez wirusa, oszczędzając przy tym normalne receptory organizmu. Dla pacjentów zagrożonych przez HCMV celowanie w ten wirusowy „główny przełącznik” może w przyszłości zaoferować precyzyjniejszy sposób kontrolowania wirusa.
Cytowanie: Drzazga, A.K., Suzuki, S., Wouters, C. et al. Activation of cytomegalovirus-encoded G protein-coupled receptor UL33 by an innate N-terminal peptide. Commun Biol 9, 415 (2026). https://doi.org/10.1038/s42003-026-09660-5
Słowa kluczowe: cytomegalowirus, wirusowy GPCR, sygnalizacja komórkowa, struktura cryo-EM, celowanie leków