Clear Sky Science · pl
Badanie reakcji biofilmów Salmonella na leczenie antybiotykami za pomocą optycznej fototermalnej spektroskopii w podczerwieni
Dlaczego lepkie bakterie mają znaczenie
Wiele patogennych bakterii woli żyć w ciasno upakowanych społecznościach zwanych biofilmami, gdzie komórki przyczepiają się do siebie i do powierzchni w organizmie lub na urządzeniach medycznych. W tych śliskich „miastach” mikroby mogą ignorować antybiotyki, które normalnie by je zabiły. W tym badaniu przedstawiono nowy sposób oglądania wnętrza biofilmów z dużą precyzją, ujawniając, które komórki są aktywnie rosnące i jak reagują po dodaniu silnych leków. Zrozumienie tych niewidocznych wzorców aktywności może pomóc lekarzom zaprojektować terapie, które w końcu przełamią uporczywe mechanizmy obronne biofilmów.
Ukryte życie wewnątrz bakteryjnych miast
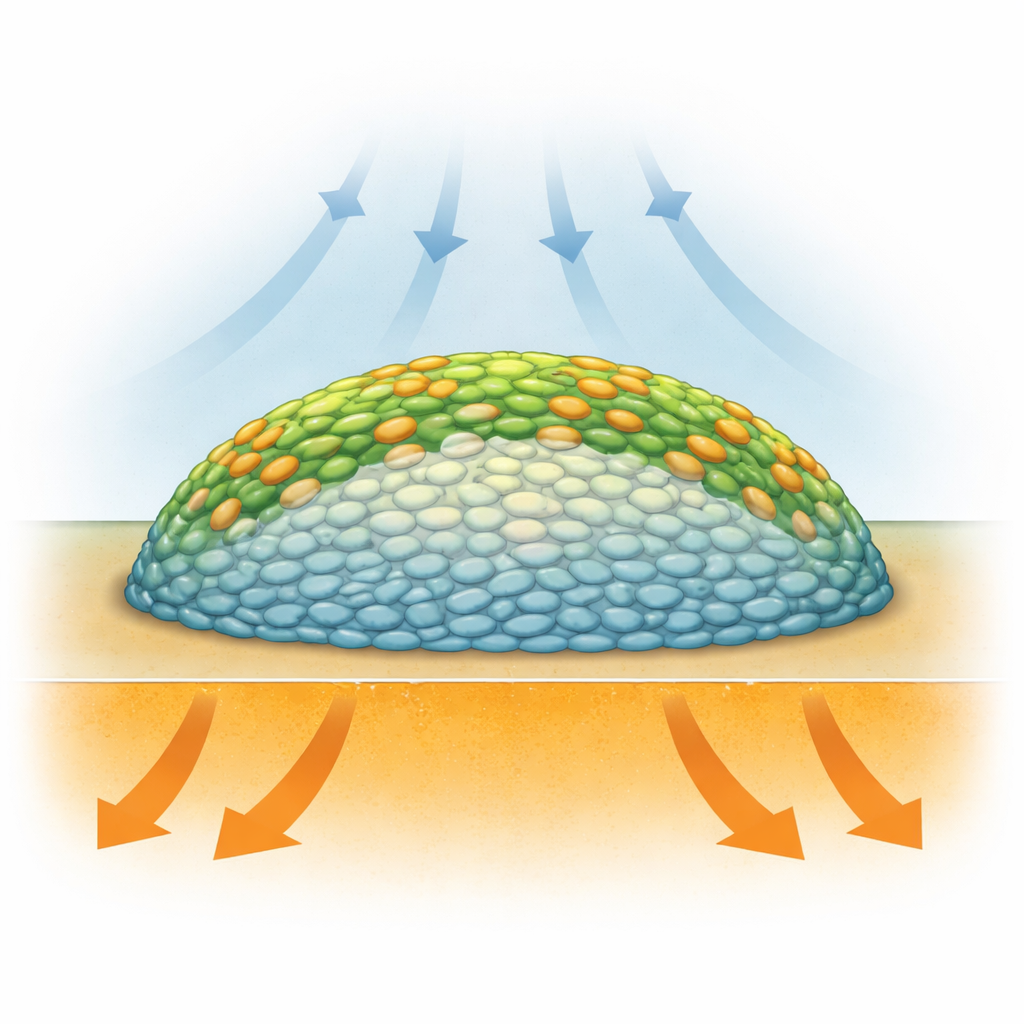
Biofilmy to nie przypadkowe grudki zarazków: to warstwowe struktury, w których bakterie żyją w bardzo różnych warunkach zależnie od miejsca. Komórki na zewnątrz mają lepszy dostęp do tlenu z powietrza, podczas gdy te pogrzebane w środku cierpią na jego brak i mogą spowalniać metabolizm lub przechodzić w stan uśpienia. Poprzednie metody, takie jak mikroskopia fluorescencyjna, potrafiły pokazać strukturę, ale często wymagały dodania barwników lub znaczników genetycznych, które mogły zakłócać biologię, i nie mierzyły bezpośrednio, co komórki robią chemicznie. Naukowcy potrzebowali sposobu, by „zobaczyć” chemię żywych biofilmów warstwa po warstwie, bez ich rozrywania lub silnej ingerencji.
Widzieć chemię niewidzialnym światłem
Zespół sięgnął po technikę zwaną optyczną fototermalną spektroskopią w podczerwieni (O-PTIR), która używa impulsów niewidzialnego światła podczerwonego i widzialnego lasera do wykrywania drobnych drgań w cząsteczkach. Te drgania działają jak odciski palców kluczowych składników komórkowych, takich jak białka, lipidy i DNA. Aby śledzić metabolizm — aktywne wykorzystanie substancji odżywczych — karmili biofilmy Salmonella Typhimurium specjalną formą cukru, w której atomy węgla były nieco cięższe niż zwykle (stabilny izotop znany jako węgiel-13). Kiedy komórki intensywnie rosną i syntetyzują nowe białka, wbudowują te cięższe atomy w swoje struktury, co powoduje subtelne, ale wykrywalne przesunięcia w sygnale w podczerwieni. Poprzez kriopreparowanie biofilmu i skanowanie cienkich przekrojów badacze stworzyli mapy chemiczne pokazujące, gdzie w biofilmie ten ciężki węgiel został włączony.
Strefy aktywności i ciche jądra
Obrazowanie w podczerwieni nieleczonych biofilmów Salmonella ujawniło uderzający wzorzec: zewnętrzne rejony i warstwy powierzchniowe wykazywały silne włączenie ciężkiego węgla, podczas gdy duże centralne jądro pokazywało go bardzo niewiele. Innymi słowy, biofilm zachowywał się jak pierścień aktywnych komórek otaczający spokojne wnętrze. Analiza statystyczna widm w podczerwieni potwierdziła, że sygnały związane z drganiami protein przesuwały się bardziej w warstwach zewnętrznych niż w centrum, co wskazywało na większą produkcję białek na obrzeżach. Wyniki te wspierają pogląd, że dostępność tlenu, największa w pobliżu powierzchni, jest głównym czynnikiem napędzającym metaboliczne „strefy gorące” w tym modelu kolonii, mimo że składniki odżywcze napływają od dołu. Badanie dostarczyło jednego z najczystszych, najwyższej rozdzielczości obrazów tego, jak metabolizm jest warstwowany wewnątrz biofilmu.
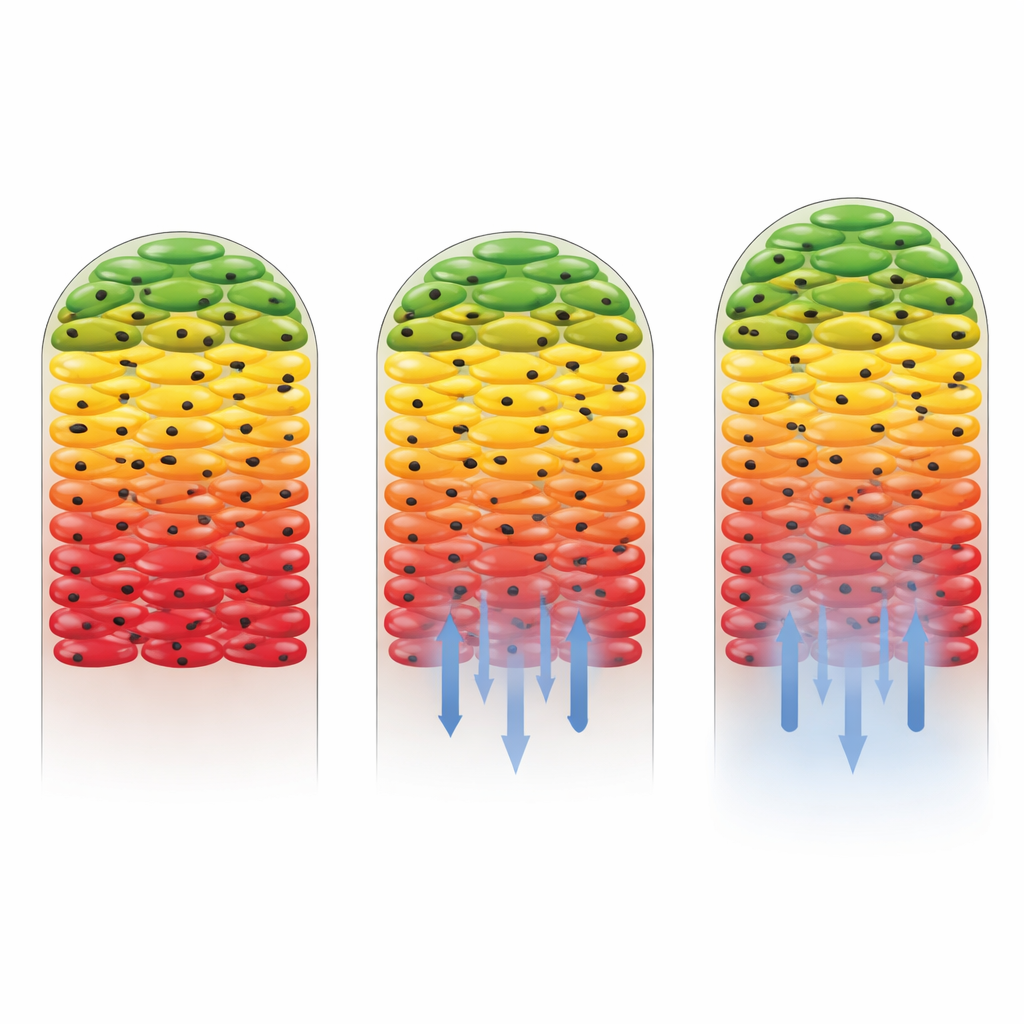
Jak różne antybiotyki przekształcają aktywność biofilmu
Następnie badacze zapytali, co się dzieje po wprowadzeniu antybiotyków. Użyli dwóch leków: kanamycyny, na którą szczep Salmonella był wrażliwy, oraz gentamycyny, na którą szczep został genetycznie uczyniony w dużej mierze niewrażliwym. W obecności gentamycyny ogólny wzorzec aktywnych warstw zewnętrznych i cichego jądra prawie się nie zmienił, co świadczy, że oporne komórki nadal rosły i włączały ciężki węgiel w dużej części biofilmu. W przeciwieństwie do tego kanamycyna drastycznie zmniejszyła aktywność metaboliczną, szczególnie blisko dna biofilmu, gdzie stężenie leku było najwyższe. Tylko cienki pas komórek najdalszych od źródła antybiotyku nadal wykazywał oznaki pobierania węgla. To ujawniło nie tylko skuteczność leku, lecz także że sama struktura biofilmu pomagała chronić część komórek przez osłabianie leku w miarę jego dyfuzji do wnętrza.
Nowe okna do leczenia trudnych zakażeń
Z perspektywy ogólnej kluczowe przesłanie jest takie, że ta praca oferuje potężny „chemiczny mikroskop”, pozwalający obserwować, jak społeczności bakteryjne żyją i przetrwają leczenie w trzech wymiarach. Łącząc niedestrukcyjną metodę obrazowania w podczerwieni z bezpieczną formą ciężkiego węgla, badacze mogli precyzyjnie wskazać, gdzie bakterie aktywnie rosną i jak ta aktywność zmienia się pod wpływem różnych antybiotyków. Ich wyniki potwierdzają, że biofilmy chronią mieszankę zajętych i niemal uśpionych komórek, i że skuteczne leki nadal mogą być osłabione przez fizyczną barierę biofilmu. W przyszłości to podejście mogłoby być użyte do testowania nowych terapii, badania, jak różne gatunki współpracują lub dzielą się opornością w mieszanych biofilmach, i ostatecznie pomóc zaprojektować mądrzejsze strategie oczyszczania przewlekłych zakażeń.
Cytowanie: Smaje, D., Zhu, X., Hinton, J.C.D. et al. Investigating Salmonella biofilm responses to antibiotic treatment using optical photothermal infrared spectroscopy. Commun Biol 9, 405 (2026). https://doi.org/10.1038/s42003-026-09655-2
Słowa kluczowe: biofilmy, Salmonella, oporność na antybiotyki, obrazowanie w podczerwieni, śledzenie izotopów stabilnych