Clear Sky Science · pl
Wybór modelu w przedklinicznych badaniach leków z kwasów nukleinowych
Przekształcanie genów w leki
Leki oparte na kwasach nukleinowych to nowy rodzaj medykamentów, które nie działają poprzez blokowanie białek, jak większość leków, lecz sięgają krok wcześniej — do poziomu naszych komunikatów genetycznych. Ten przegląd wyjaśnia, jak naukowcy dobierają odpowiednie modele laboratoryjne i zwierzęce do testowania tych leków celujących w RNA, zanim trafią do pacjentów. Czytelnik niebędący specjalistą może się tym zainteresować, ponieważ mądre wybory modeli mogą przyspieszyć rozwój bezpieczniejszych i skuteczniejszych terapii chorób genetycznych, w tym rzadkich schorzeń dziecięcych oraz częstszych przypadków, jak choroby serca.
Co wyróżnia te leki genetyczne?
Leki z kwasów nukleinowych (NAT) obejmują krótkie łańcuchy zwane oligonukleotydami antysensownymi (ASO) oraz małe interferencyjne RNA (siRNA). Zamiast polegać na kształcie i chemii celów białkowych, te leki rozpoznają swoje cele przez zasady parowania zasad — to samo dopasowanie A‑T i G‑C, które leży u podstaw DNA. Dzięki temu są programowalne: znając sekwencję RNA, którą chcemy zmienić, często można szybko zaprojektować wiele kandydatów bez wieloletnich prac chemicznych. Trudność nie polega już na pytaniu „Czy potrafimy stworzyć aktywny związek?”, lecz „Jak zmierzyć, czy rzeczywiście działa w realistycznym kontekście biologicznym?”. Ponieważ nawet pojedyncza różnica w literze sekwencji może zadecydować o aktywności, wybór odpowiednich systemów testowych staje się kluczowy.
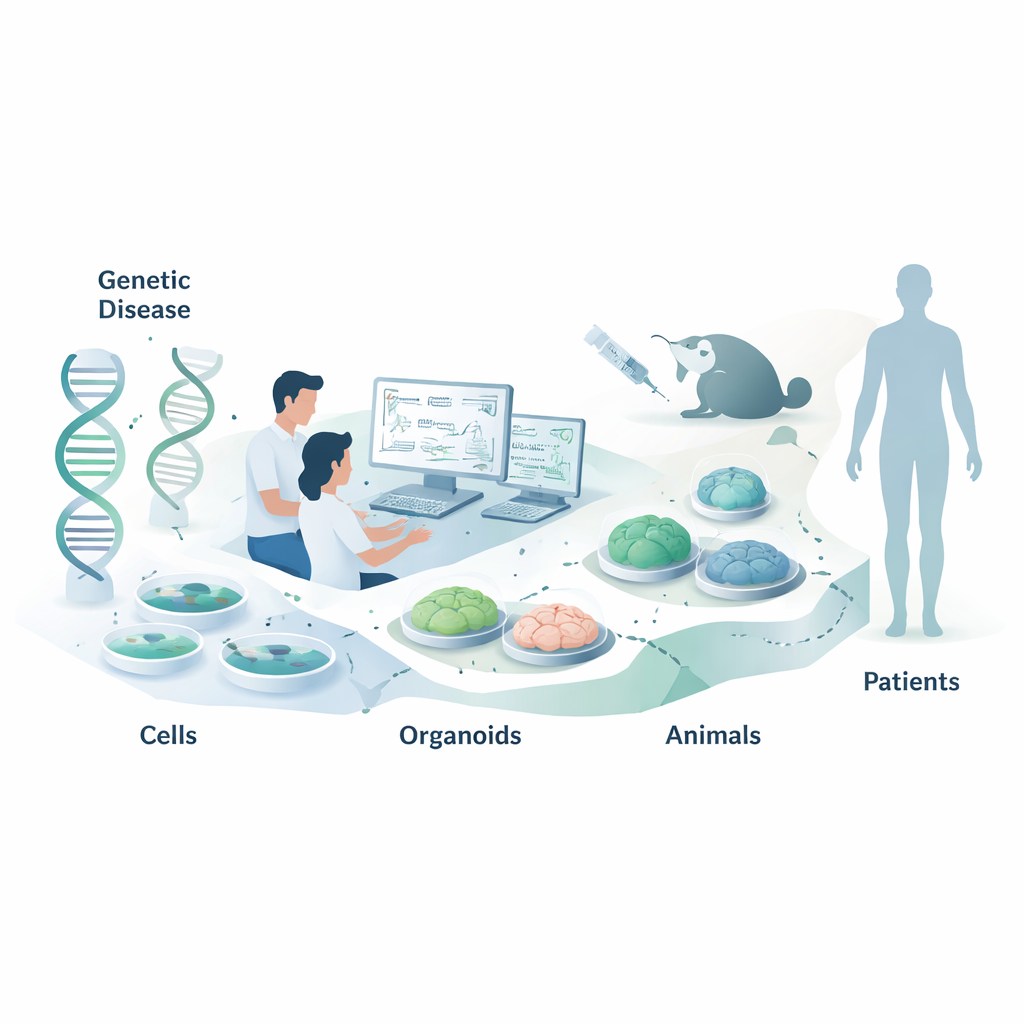
Proste testy komórkowe: szybkie, ale niepełne
Pierwszym etapem dla większości NAT są panele stosunkowo łatwych do hodowli linii komórkowych, takich jak komórki HeLa czy HEK293, które naturalnie exprimują docelowe RNA. Badacze dodają duże biblioteki kandydatów ASO lub siRNA, a następnie mierzą, jak bardzo spada poziom docelowego RNA i białka, stosując techniki takie jak PCR czy Western blot. Pracują też z komórkami pochodzącymi od pacjentów, które lepiej odwzorowują indywidualne tło genetyczne i pozwalają testować leki „selektywne allelicznie”, wyciszające tylko wadliwą kopię genu. Gdy naturalny gen nie jest wygodnie eksprymowany, naukowcy czasem wprowadzają sztuczne minigeny lub plazmidy raportujące, które świecą, gdy RNA zostanie przecięte lub poprawnie składane. Systemy te są potężne do szybkiego porównywania wielu projektów, ale mogą pomijać istotne szczegóły, takie jak naturalna struktura RNA czy przetwarzanie specyficzne dla typu komórki, dlatego wyniki trzeba potwierdzać w bardziej realistycznych kontekstach.
Od napraw molekularnych do rzeczywistego zachowania komórek
Wiele NAT nie ma na celu jedynie zniszczenia wadliwego RNA, lecz jego naprawę poprzez modyfikację składania (splicingu), procesu łączenia fragmentów komunikatu genowego. Starannie zaprojektowane ASO mogą spowodować pominięcie szkodliwego eksonu, przywrócić brakujący fragment lub zapobiec włączeniu „pseudoeksonu”, który łamie kod. Aby sprawdzić, czy takie zmiany rzeczywiście poprawiają funkcję komórki, badacze idą dalej niż proste pomiary poziomów RNA i białka. W komórkach pochodzących od pacjentów testują, czy aktywność enzymu wraca, czy transport jonów w komórkach płuc normalizuje się lub czy szlaki sygnałowe w komórkach układu odpornościowego reagują prawidłowo. Coraz częściej wykorzystują trójwymiarowe organoidy — mini‑tkanki hodowane ze komórek macierzystych pacjentów — które potrafią naśladować rytm serca, aktywność sieci mózgowych lub inne złożone zachowania. Te modele 3D są bliższe prawdziwym narządom, ale są trudniejsze, wolniejsze i droższe w prowadzeniu, więc zespoły muszą równoważyć realizm z przepustowością.
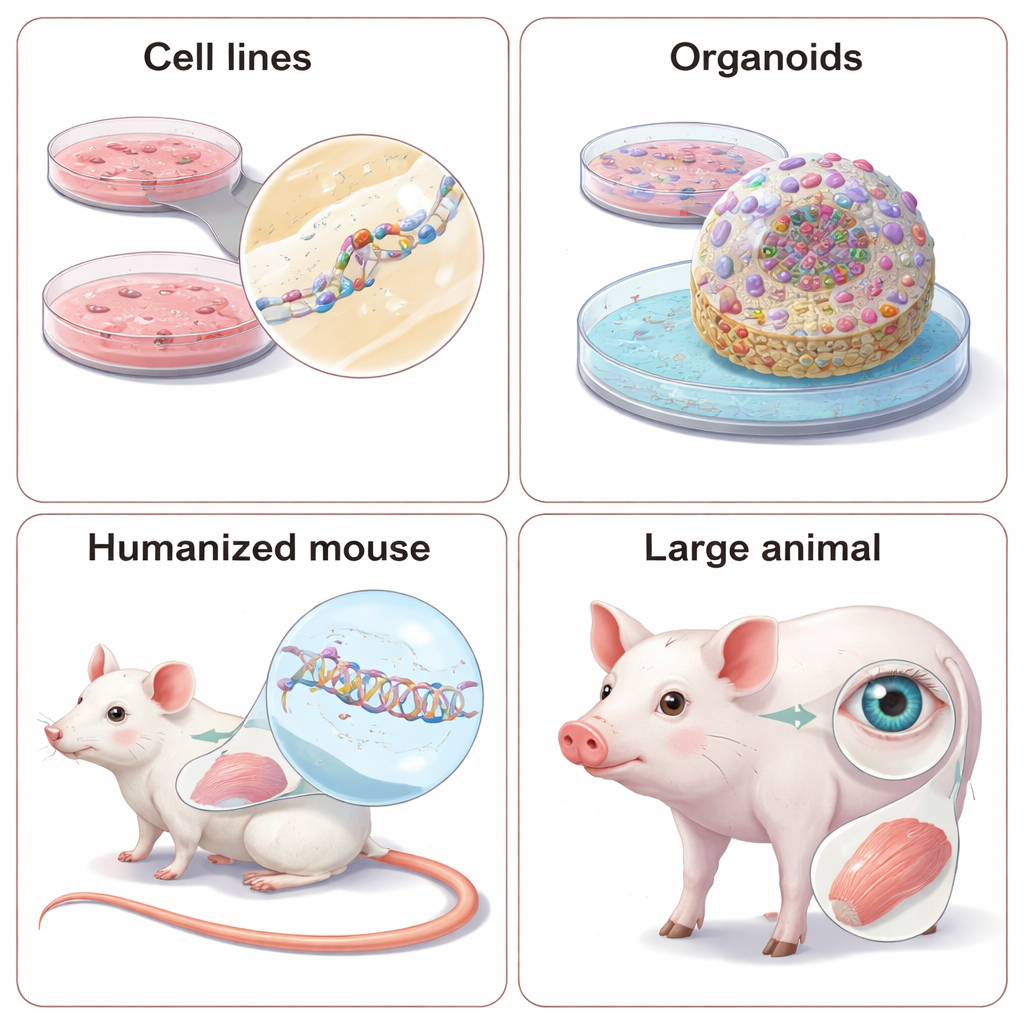
Dlaczego zwierzęta wciąż mają znaczenie — i jak je uhumanizować
Niektórych cech chorób, takich jak metabolizm całego organizmu, interakcje między narządami czy zachowanie, nie da się uchwycić w naczyniach hodowlanych. W takich przypadkach NAT testuje się na żywych zwierzętach. Ponieważ te leki zależą od dokładnej sekwencji RNA, naukowcy stoją przed wyborem: zaprojektować „zastępcze” leki dopasowane do wersji genu u zwierzęcia lub przeprojektować zwierzę tak, by nosiło ludzkie sekwencje genetyczne. Zastępcze ASO i siRNA mogą pokazać, czy obniżenie poziomu genu poprawia objawy w dobrze ugruntowanych modelach mysich, ale nie idealnie odwzorowują lek ukierunkowany na człowieka. Modele uhumanizowane — myszy lub nawet mini‑świnie z fragmentami lub całymi kopiami ludzkich genów — pozwalają testować rzeczywistego kandydata klinicznego, lecz wymagają znacznego czasu i kosztów, a subtelne różnice w regulacji genów między gatunkami wciąż mogą prowadzić do niespodzianek. Przegląd podkreśla też rosnące użycie dużych zwierząt, szczególnie w chorobach oczu i mięśni, gdzie anatomia bardziej przypomina ludzką.
W kierunku przyszłości: mądrzejsze modele i mniej zgadywania
Autorzy konkludują, że nie ma jednego „najlepszego” modelu dla leków z kwasów nukleinowych; zamiast tego każdy projekt wymaga dostosowanej ścieżki, która zaczyna się od szybkich, prostych testów i przechodzi do bardziej złożonych, bardziej odpowiednich dla człowieka systemów. W miarę jak regulatorzy i fundatorzy naciskają na ograniczenie użycia zwierząt, zaawansowane organoidy, urządzenia organ‑on‑a‑chip i modele komputerowe mają przejąć większą część pracy, zwłaszcza w połączeniu z narzędziami uczenia maszynowego, które przewidują, które sekwencje i chemie sprawdzą się najlepiej. Ostatecznie, rozumiejąc mocne strony i ślepe punkty każdego modelu — oraz dzieląc się najlepszymi praktykami i danymi w całej dziedzinie — badacze mogą bardziej wiarygodnie przekształcać programowalne pomysły genetyczne w bezpieczne, skuteczne leki dla pacjentów.
Cytowanie: Oliver, P.L., Hill, A.C. Model selection in preclinical nucleic acid therapeutics research. Commun Biol 9, 200 (2026). https://doi.org/10.1038/s42003-026-09650-7
Słowa kluczowe: leki z kwasów nukleinowych, oligonukleotydy antysensowne, siRNA, modele przedkliniczne, terapia genowa