Clear Sky Science · pl
Wnt11 pośredniczy w interakcji fibroblast–mięśnie gładkie, promując włóknienie pęcherza neurogennego u szczurów
Gdy nerwy zawodzą, pęcherz bliznuje
Wiele osób z urazami rdzenia kręgowego, stwardnieniem rozsianym lub chorobą Parkinsona rozwija „pęcherz neurogenny”, w którym uszkodzone nerwy nie potrafią już właściwie kontrolować magazynowania i wydalania moczu. Z czasem ściana pęcherza może stawać się gruba i sztywna wskutek tkanki przypominającej bliznę, co zagraża zdrowiu nerek i jakości życia. Badanie przeprowadzone na szczurach ujawnia kluczowego molekularnego sprawcę tego bliznowacenia i sugeruje nowe sposoby spowalniania lub nawet zapobiegania temu uszkodzeniu.
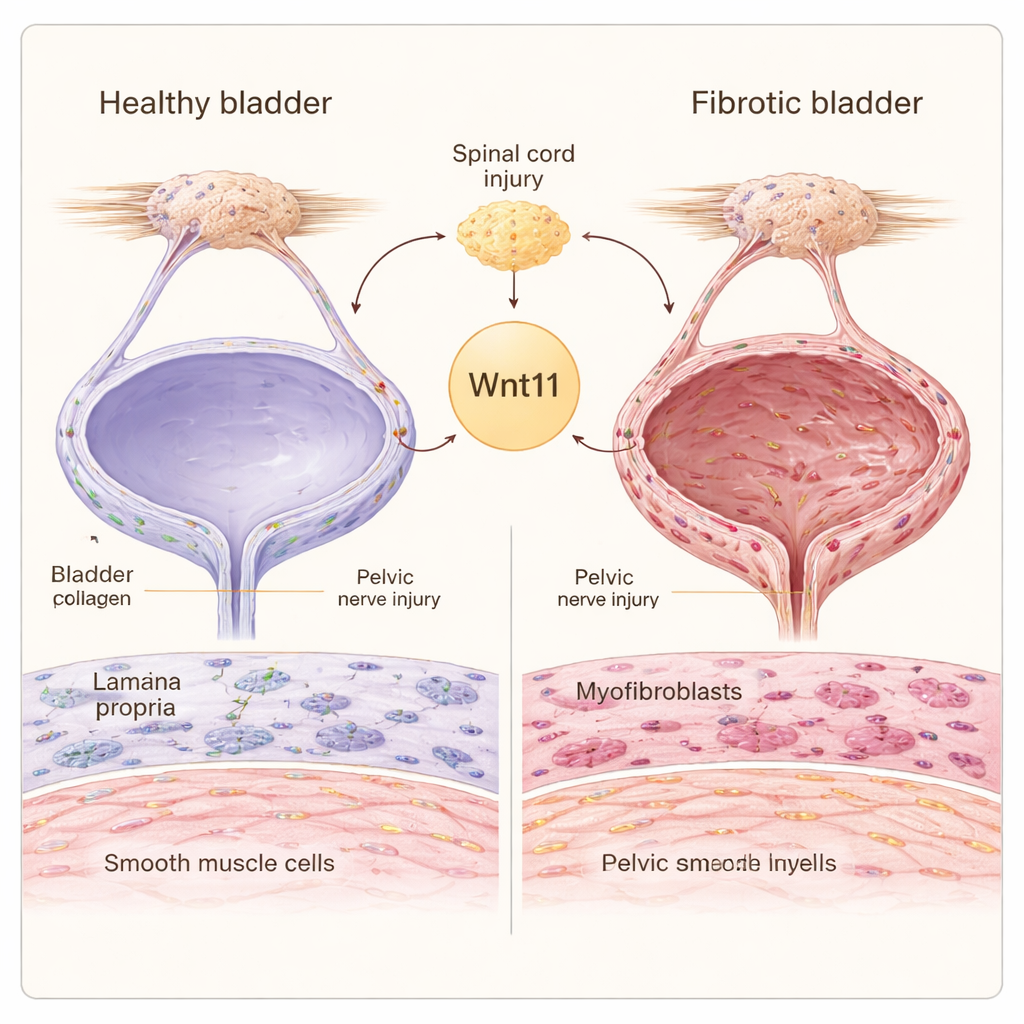
Ukryty koszt uszkodzenia nerwów
Gdy nerwy unerwiające pęcherz zostają uszkodzone, czy to w rdzeniu kręgowym, czy w okolicy miednicy, narząd musi pracować ciężej, by radzić sobie z moczem. Ściana pęcherza zawiera dwa główne typy komórek wspierających: fibroblasty, które wytwarzają materiał rusztowania wokół komórek, oraz komórki mięśni gładkich, które się kurczą, by wypchnąć mocz. W pęcherzu neurogennym fibroblasty mogą przechodzić w wysoko aktywne „mięśniopodobne fibroblasty” (myofibroblasty), które produkują nadmiar kolagenu, podczas gdy komórki mięśni gładkich zmieniają się ze smukłego, kurczliwego stanu w bardziej masywny, syntetyczny fenotyp. Razem te zmiany odkładają sztywną tkankę bliznowatą, która ogranicza zdolność pęcherza do rozciągania się i opróżniania.
Cząsteczka sygnałowa wchodząca na scenę
Naukowcy skupili się na rodzinie białek komunikacji międzykomórkowej zwanych ligandami Wnt, które są znane z regulacji wzrostu tkanek i bliznowacenia w innych narządach. Przesiewowo badając pęcherze szczurów z uszkodzeniem nerwów, stwierdzili, że jeden członek tej rodziny, Wnt11, był konsekwentnie i silnie podwyższony w pęcherzach włókniejących wywołanych zarówno urazem rdzenia kręgowego, jak i zmiażdżeniem nerwu miednicznego. Poziomy Wnt11 wzrastały zarówno w fibroblastach, jak i komórkach mięśni gładkich, a ilość Wnt11 korelowała z nasileniem dysfunkcji pęcherza. Gdy normalne komórki pęcherza hodowane w warunkach in vitro były wystawione na działanie kolejnego pro-bliznowaciejącego czynnika, TGF-β1, również zwiększały produkcję Wnt11, co sugeruje istnienie sprzężenia zwrotnego między tymi dwoma sygnałami.
Od chemicznego komunikatu do trwałej blizny
Aby sprawdzić, czy Wnt11 jest jedynie biernym obserwatorem, czy aktywnym sprawcą, zespół dodał dodatkowe białko Wnt11 do szczurów z uszkodzeniem nerwów, a także zablokował wydzielanie Wnt lekiem LGK974. Nadmiar Wnt11 powiększał pęcherze, pogarszał profile ciśnienia podczas napełniania i opróżniania, pogrubiał warstwę mięśniową i zwiększał depozycję kolagenu. Zablokowanie wydzielania Wnt przyniosło efekt odwrotny, łagodząc problemy z oddawaniem moczu i redukując tkankę bliznowatą. W izolowanych komórkach Wnt11 przesuwał fibroblasty w kierunku statusu myofibroblastu i skłaniał komórki mięśni gładkich ku syntetycznemu, sprzyjającemu włóknieniu fenotypowi. Wyciszenie samego genu Wnt11 tłumiło te zmiany, co jasno wykazało, że Wnt11 jest centralnym przyspieszaczem przebudowy pęcherza.
Jak komórki odszyfrowują sygnał włóknienia
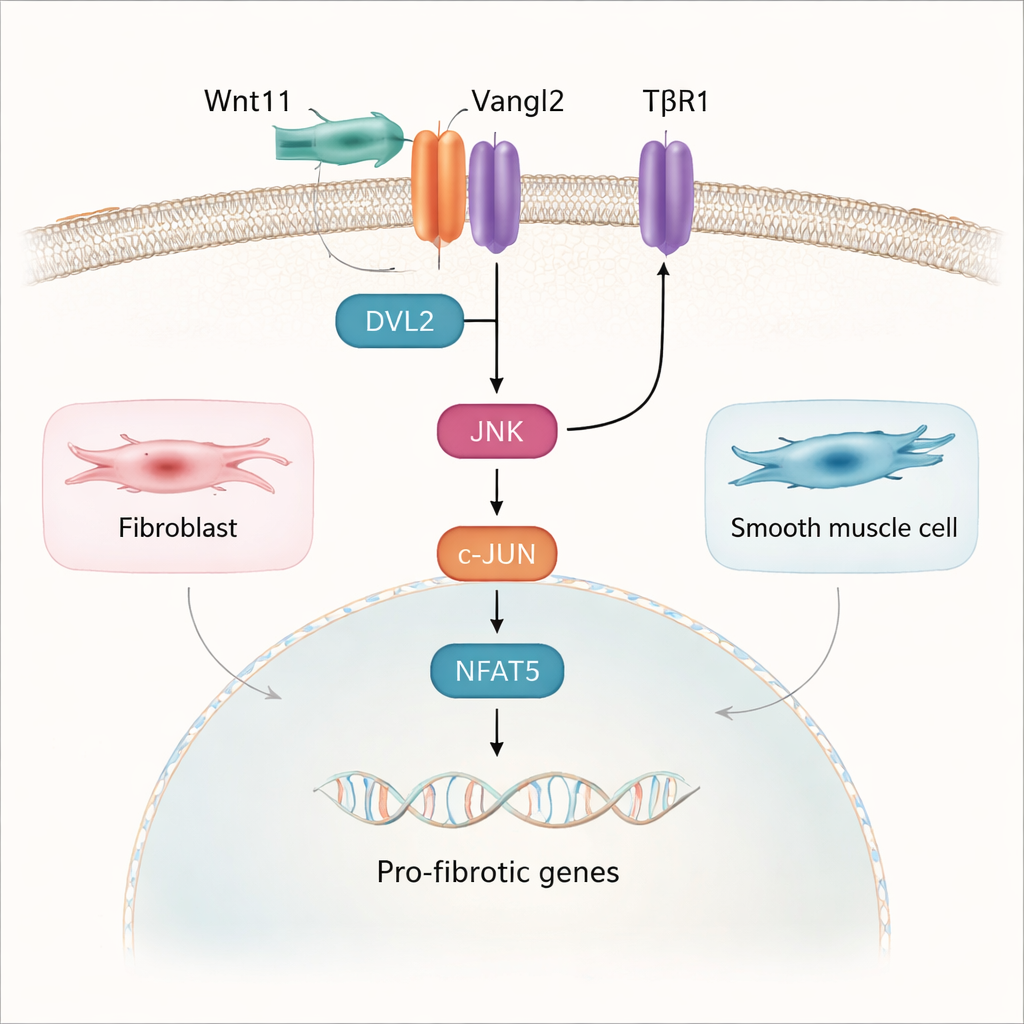
Zagłębiając się głębiej, badanie odtworzyło ścieżkę od Wnt11 na powierzchni komórki do zmian genowych w jądrze. Stwierdzono, że Wnt11 wiąże receptor Vangl2 na fibroblastach i komórkach mięśni gładkich pęcherza. To partnerstwo nie korzystało z klasycznej drogi Wnt obejmującej białko β-kateninę; zamiast tego aktywowało inną kaskadę zwaną ścieżką polarności komórek planarnej (PCP). Tutaj Wnt11 i Vangl2 rekrutują białko adaptorowe DVL2, które następnie uruchamia enzym JNK. JNK z kolei aktywuje czynniki transkrypcyjne c-JUN i NFAT5, które przemieszczają się do jądra i pomagają włączać geny pro-włóknieniowe. Droga TGF-β1, dobrze znany kierowca bliznowacenia, konwergowała fizycznie i funkcjonalnie z tą ścieżką Wnt11–Vangl2–JNK, tak że oba sygnały wzmacniały się nawzajem zarówno przy błonie komórkowej, jak i w jądrze.
W kierunku bardziej miękkich, zdrowszych pęcherzy
Ponieważ Wnt11 i TGF-β1 współdziałają, aby utwardzać pęcherz, zespół przetestował leki blokujące kluczowe etapy obu tych szlaków. U szczurów z pęcherzem neurogennym najlepsze wyniki dała łączona inhibicja receptora TβR1 dla TGF-β oraz enzymu JNK: mniejsze pęcherze, cieńsze ściany mięśniowe, mniej kolagenu i poprawione magazynowanie oraz opróżnianie moczu w porównaniu z leczeniem jednym lekiem. Dla osoby bez specjalistycznej wiedzy główne przesłanie jest takie, że specyficzny sygnał wywołany uszkodzeniem nerwów, Wnt11, pomaga przekształcać normalne komórki podporowe i mięśniowe w komórki tworzące blizny. Przerwanie tego sygnału, zwłaszcza w połączeniu z klasycznymi blokerami TGF-β, mogłoby stanowić podstawę przyszłych terapii ukierunkowanych nie tylko na łagodzenie objawów, ale na zachowanie struktury i funkcji pęcherza u osób z pęcherzem neurogennym.
Cytowanie: Ge, Q., Zhang, J., Fan, Z. et al. Wnt11 mediates fibroblast–smooth muscle cell interaction to promote neurogenic bladder fibrosis in rats. Commun Biol 9, 194 (2026). https://doi.org/10.1038/s42003-026-09647-2
Słowa kluczowe: pęcherz neurogenny, włóknienie, Wnt11, komórki mięśni gładkich, sygnalizacja TGF-β