Clear Sky Science · pl
Równoległe szlaki zależne od Tbr2 regulują rozwój odmiennych podtypów ipRGC
Jak nasze oczy mierzą czas i formę
Ponad tworzeniem obrazów, nasze oczy cicho regulują zegar biologiczny, kontrolują szerokość źrenic i pomagają oceniać ogólny poziom jasności. Niewielka populacja specjalnych komórek nerwowych siatkówki, zwanych wewnętrznie fotoczułymi komórkami zwojowymi siatkówki (ipRGC), wykonuje znaczną część tej pracy. Odpowiadają na światło przy użyciu barwnika zwanego melanopsyną i przesyłają sygnały głęboko do mózgu. W tym badaniu postawiono podstawowe pytanie o duże konsekwencje: w jaki sposób jedna wczesna populacja rozwijających się komórek nerwowych rozdziela się na kilka odrębnych typów ipRGC, z których każdy jest okablowany do innego zadania?
Jeden główny przełącznik, wiele typów komórek światłoczułych
W siatkówce myszy wszystkie sześć znanych podtypów ipRGC wywodzi się z wczesnej populacji komórek zwojowych, które włączają gen Tbr2. Gen ten działa jak główny przełącznik, uruchamiając programy potrzebne do powstania ipRGC i do utrzymania aktywności genu melanopsyny, Opn4. Sam jeden przełącznik nie wyjaśnia jednak, jak powstaje sześć różnych odmian ipRGC, każda o unikatowych kształtach, reakcjach na światło i celach w mózgu. Autorzy użyli sekwencjonowania RNA rozwijających się siatkówek myszy, aby poszukać genów, których aktywność zależy od Tbr2. Spośród niewielkiej grupy kandydatów wyróżniły się dwa: Irx1 i Tbx20, oba znane jako regulatory tożsamości komórek w innych częściach organizmu. 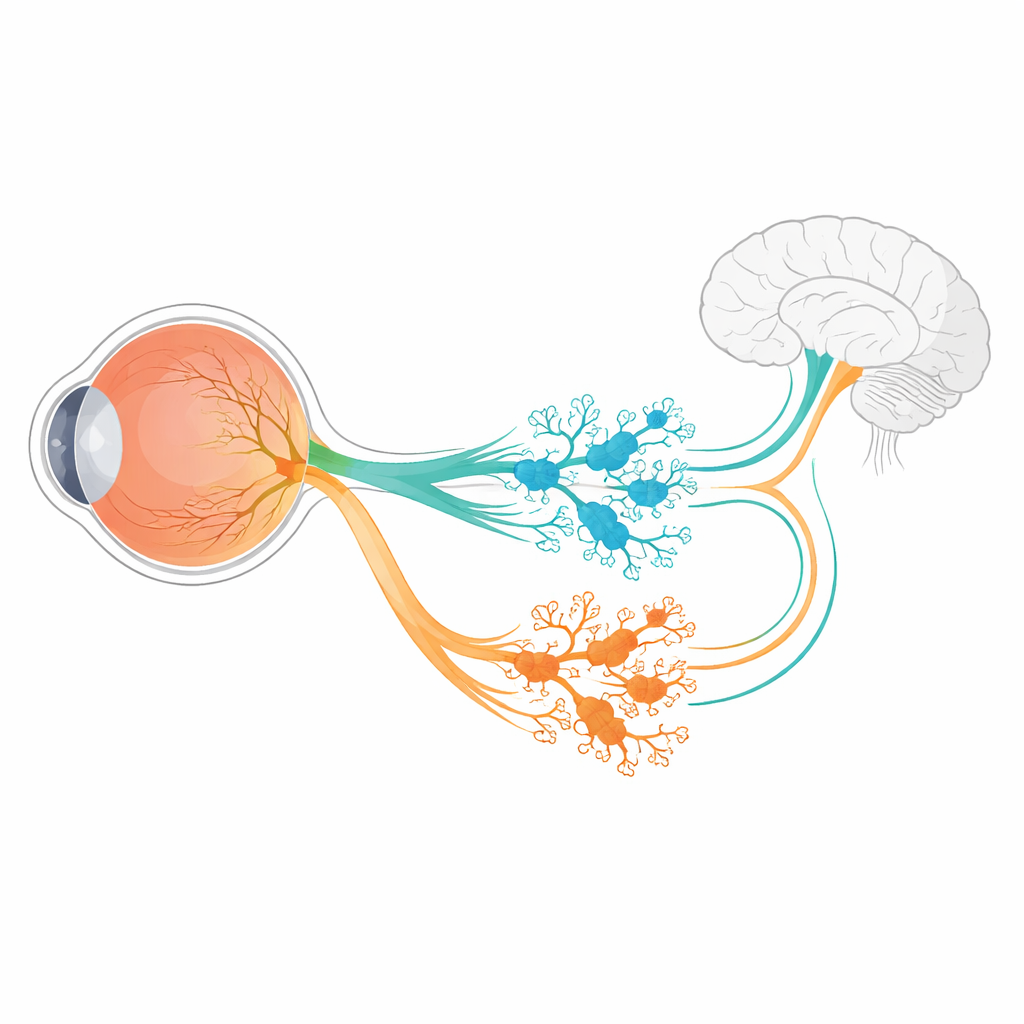
Dwie rozgałęziające się ścieżki w obrębie siatkówki
Wykorzystując nowo zmodyfikowane linie myszy, które znakują komórki produkujące Irx1 i Tbx20 markerami fluorescencyjnymi lub enzymatycznymi, badacze śledzili, gdzie i kiedy te czynniki są uruchamiane. Stwierdzili, że Irx1 i Tbx20 pojawiają się w nakładających się grupach młodych komórek zwojowych siatkówki około połowy okresu płodowego, lecz szybko rozdzielają się na niemal całkowicie odrębne zestawy w dorosłości. Irx1 występuje głównie w trzech typach ipRGC oznaczonych jako M3, M4 i M5, podczas gdy Tbx20 koncentruje się w komórkach M1, M2 i M6, z jedynie niewielkim nakładaniem się w niektórych komórkach M3 i M5. Szczegółowe obrazowanie, rejestracje elektryczne i śledzenie projekcji do mózgu wykazały, że każdy z tych czynników oznacza odrębną populację ipRGC o charakterystycznych rozmieszczeniach dendrytów, reakcjach na światło oraz wzorcach projekcji do konkretnych regionów mózgu zaangażowanych w ustawianie zegara, odruchy i przetwarzanie wzrokowe.
Przełączniki regulujące czułość na światło i przeżywalność komórek
Zespół następnie sprawdził, co się dzieje po usunięciu każdego z czynników. Gdy Irx1 został wyłączony w rozwijającej się siatkówce, liczba i podstawowa struktura ipRGC oznaczonych Irx1 pozostała w dużej mierze nienaruszona, ale poziomy melanopsyny znacznie spadły. Innymi słowy, Irx1 okazał się niezbędny do pełnego uruchomienia programu świetlnego Opn4 w komórkach M3, M4 i M5, ale nie był konieczny do samego utworzenia tych komórek. Tbx20 zachowywał się inaczej. Usunięcie Tbx20 nie tylko obniżyło ekspresję Opn4, lecz także zmniejszyło liczbę komórek pozytywnych na Tbx20 mniej więcej o połowę, a w późniejszym okresie ograniczyło przeżywalność tych komórek. Wskazuje to, że Tbx20 pomaga zarówno w budowie, jak i utrzymaniu konkretnych podtypów ipRGC, zwłaszcza M1, M2 i M6, a także wspiera ich melanopsynową czułość na światło. 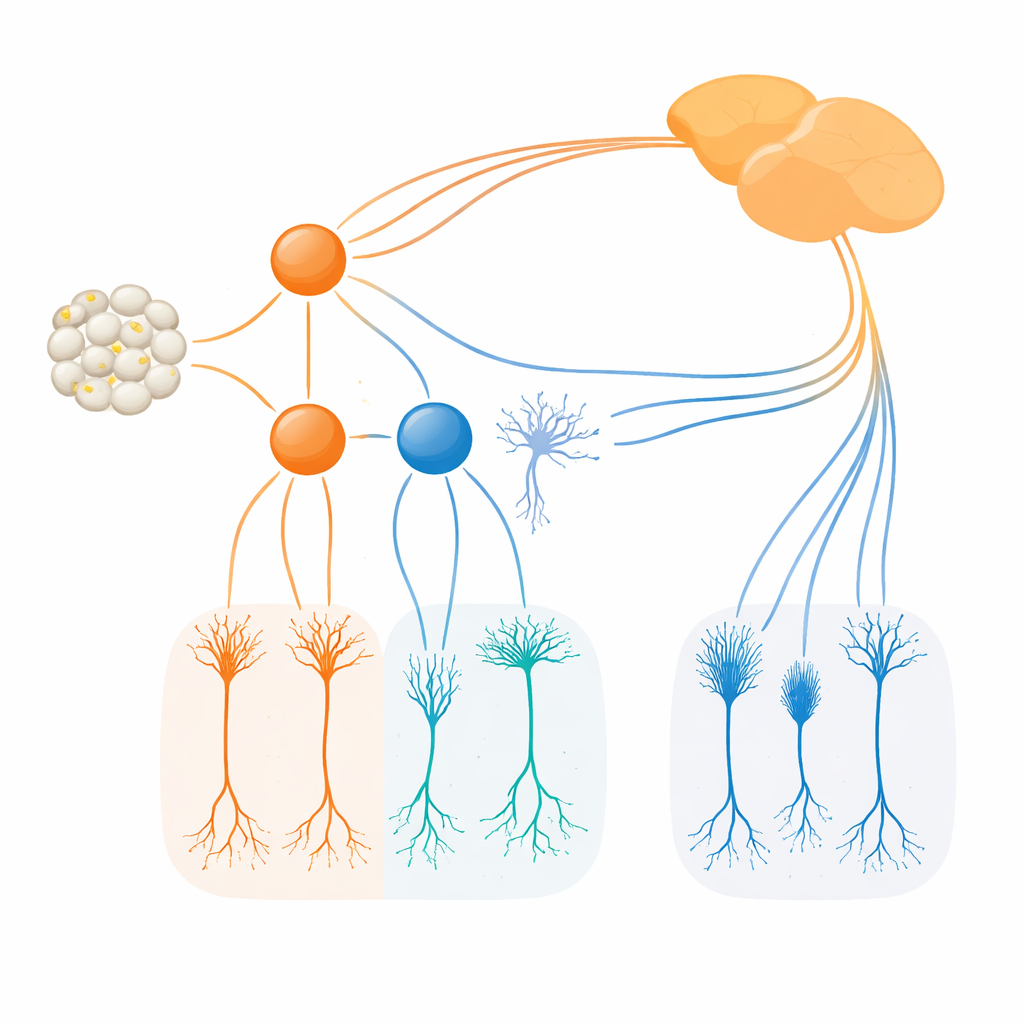
Wyznaczanie momentu rozdzielenia na odrębne rodziny komórek
Poprzez krótkotrwałe aktywowanie reporterów genetycznych w precyzyjnych dniach embrionalnych, autorzy mogli „ostemplować czasowo” komórki, które wyrażały Irx1 lub Tbx20, i śledzić ich losy aż do dorosłości. Eksperymenty wykazały, że komórki oznaczone przez Tbx20 zobowiązują się do swoich ostatecznych tożsamości ipRGC nieco wcześniej niż komórki oznaczone przez Irx1, a większość decyzji zapada tuż przed narodzinami. W krótkim oknie czasowym oba czynniki mogą współistnieć w niektórych komórkach, a myszy z podwójnym wyłączeniem obu genów wykazały znacznie silniejszą utratę ipRGC pozytywnych na melanopsynę niż w pojedynczych mutantach. Sugeruje to, że oba szlaki współdziałają przemijająco, a następnie rozchodzą się, kierując różne podzbiory ipRGC odrębnymi torami rozwojowymi.
Co to oznacza dla zrozumienia wzroku i zdrowia
Dla osoby niebędącej specjalistą główny przekaz jest taki, że jeden wczesny gen, Tbr2, nie działa samodzielnie. Zamiast tego wpływa na dwa równoległe szlaki kontrolne, jeden skupiony wokół Irx1, drugi wokół Tbx20. Te ścieżki decydują, jakiego rodzaju ipRGC stanie się młoda komórka, dopracowują, jak silnie odbiera światło, i określają, czy połączy się z regionami mózgu odpowiadającymi za regulację zegara biologicznego, odruchy źrenicy czy inne role wzrokowe. Praca ta oferuje jaśniejszy schemat połączeń tego, jak zbudowane są nasze wewnętrzne „liczniki światła”, i wskazuje konkretne etapy genetyczne, które mogą mieć znaczenie, gdy te komórki zostaną utracone lub źle funkcjonują — z potencjalnym znaczeniem dla zaburzeń snu, sezonowych zmian nastroju oraz chorób uszkadzających siatkówkę.
Cytowanie: Kiyama, T., Chen, CK., Altay, H.Y. et al. Tbr2-dependent parallel pathways regulate the development of distinct ipRGC subtypes. Commun Biol 9, 347 (2026). https://doi.org/10.1038/s42003-026-09645-4
Słowa kluczowe: komórki zwojowe siatkówki, melanopsyna, rozwój neurologiczny, rytmy dobowe, czynniki transkrypcyjne