Clear Sky Science · pl
Analiza strukturalna ujawnia, że cząsteczki wody pośredniczą w autouaktywowaniu GPR99
Dlaczego ten receptor ma znaczenie dla zapalenia
Nasze drogi oddechowe i inne tkanki nieustannie wyczuwają chemiczne sygnały, które wskazują na infekcję lub podrażnienie. Jednym z takich sensorów jest białko GPR99, które znajduje się na powierzchni komórek i wyłania się jako istotny przełącznik w chorobach zapalnych, takich jak astma czy polipy nosa. W tym badaniu wyjaśniono, w skali atomowej, jak GPR99 może włączać się samoistnie nawet bez zewnętrznego liganda — oraz jak drobne skupiska cząsteczek wody ułatwiają ten proces — dostarczając wskazówek przy projektowaniu nowych leków przeciwzapalnych.
Wbudowany przełącznik w sensorze komórkowym
GPR99 należy do dużej rodziny białek błonowych, które przekazują informacje z zewnątrz komórki do jej wnętrza, często zmieniając konformację i rekrutując partnerów białkowych zwanych białkami G. W przeciwieństwie do większości takich receptorów, GPR99 wykazuje nadzwyczajną aktywność nawet wtedy, gdy nie jest związany żaden ligand. Autorzy pokazują, że elastyczna pętla po zewnętrznej stronie receptora, znana jako druga pętla zewnątrzkomórkowa, działa jak wewnętrzny klucz: wkłada się do zwykłej kieszeni wiążącej, imitując sygnał aktywujący i samodzielnie włączając receptor.
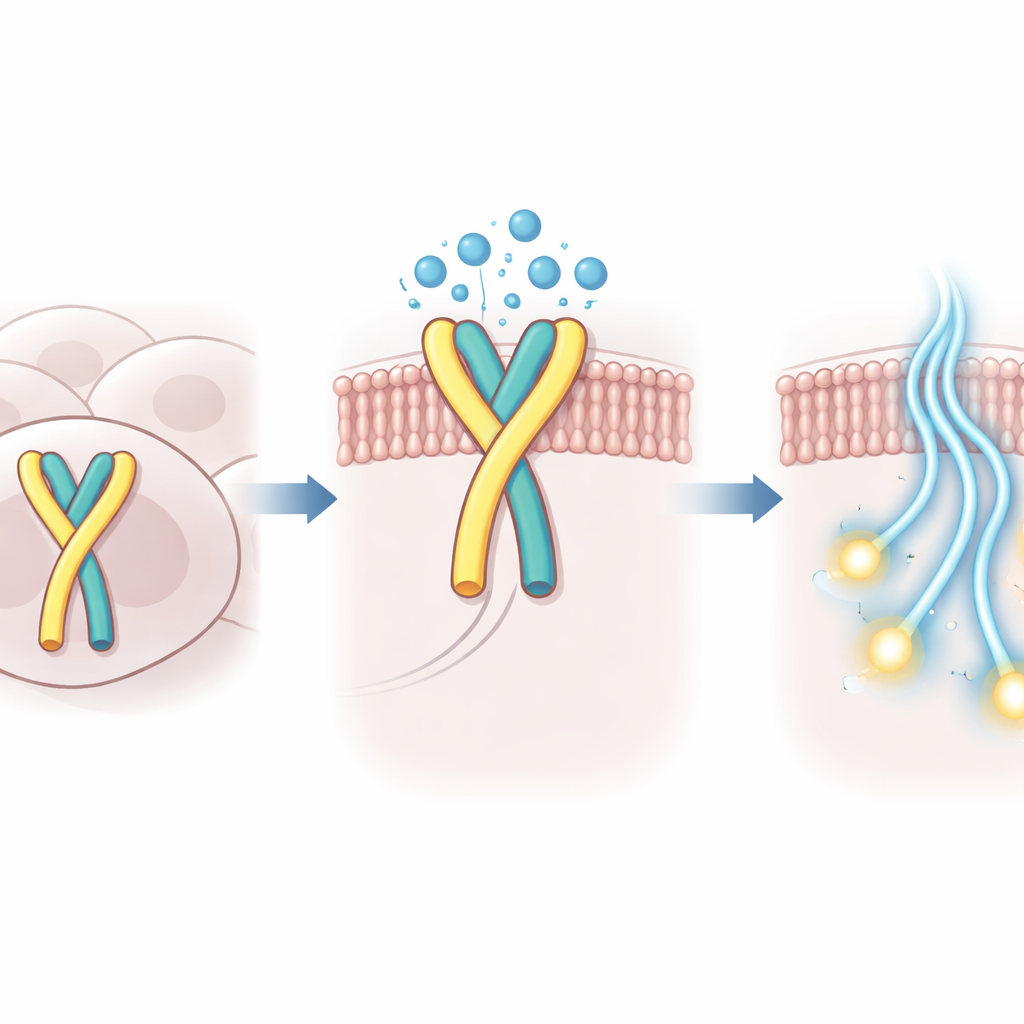
Jak woda pomaga utrzymać przełącznik na miejscu
Wykorzystując wysokorozdzielczą krioelektronową mikroskopię, badacze uchwycili trójwymiarową strukturę ludzkiego GPR99 związana z białkiem G w stanie autouaktywnym. W kieszeni wiążącej, gdzie zwykle lokowałyby się zewnętrzne cząsteczki, zaobserwowali nie tylko wsuniętą pętlę, lecz także małe skupisko uporządkowanych cząsteczek wody. Te molekuły wody tworzą polarny mostek między pętlą a otaczającym białkiem, kompensując płytsze wsunięcie pętli i stabilizując aktywną konformację receptoru. Gdy kluczowe aminokwasy w pętli lub w sąsiedniej kieszeni były zmieniane tak, że te kontakty pośredniczone przez wodę osłabły, w komórkowych testach aktywność wbudowana GPR99 gwałtownie spadała.
Przearanżowanie wewnętrznych mechanizmów dla stałego sygnalizowania
Zespół porównał strukturę autouaktywną z innymi członkami rodziny, w tym z blisko spokrewnionym receptorem wiążącym produkt metaboliczny — bursztynian — oraz z aktywną formą GPR99 związaną z metabolitem 2‑oksyglutaranem. Stwierdzili, że GPR99 w braku zewnętrznego liganda jest już w pełni gotowy w aktywnej konformacji: kilka zachowanych „mikroprzełączników” w jego helikalnym rdzeniu przyjmuje kształty zwykle obserwowane dopiero po pobudzeniu receptorów. Krytyczne pozycje, które zwykle pomagają utrzymać receptor w stanie wyłączonym, zostały zastąpione lub przearanżowane w GPR99, rozluźniając wewnętrzne ograniczenia i sprzyjając otwartej konfiguracji, która przyjmuje partnera białkowego G.
Przekazywanie sygnału do wnętrza komórki
Po wewnętrznej stronie błony struktura pokazuje, jak GPR99 chwyta białko G typu Gq, które przekazuje jego sygnał. Helikalny ogon białka G wsuwa się w kawernę otwartą przez odchylenie jednej z helis GPR99, tworząc sieć kontaktów polarnych i hydrofobowych z wewnętrznymi pętlami i ogonem receptora. Mutacje zakłócające to miejsce interakcji także osłabiają sygnalizację, potwierdzając, że autouaktywnienie wywołane przez zewnętrzną pętlę i skupisko wody jest skutecznie sprzężone z partnerami wewnątrzkomórkowymi. Razem te strukturalne migawki łączą zmiany na zewnętrznej powierzchni receptora z falami sygnalizacji wapniowej, które wywołuje wewnątrz komórek.
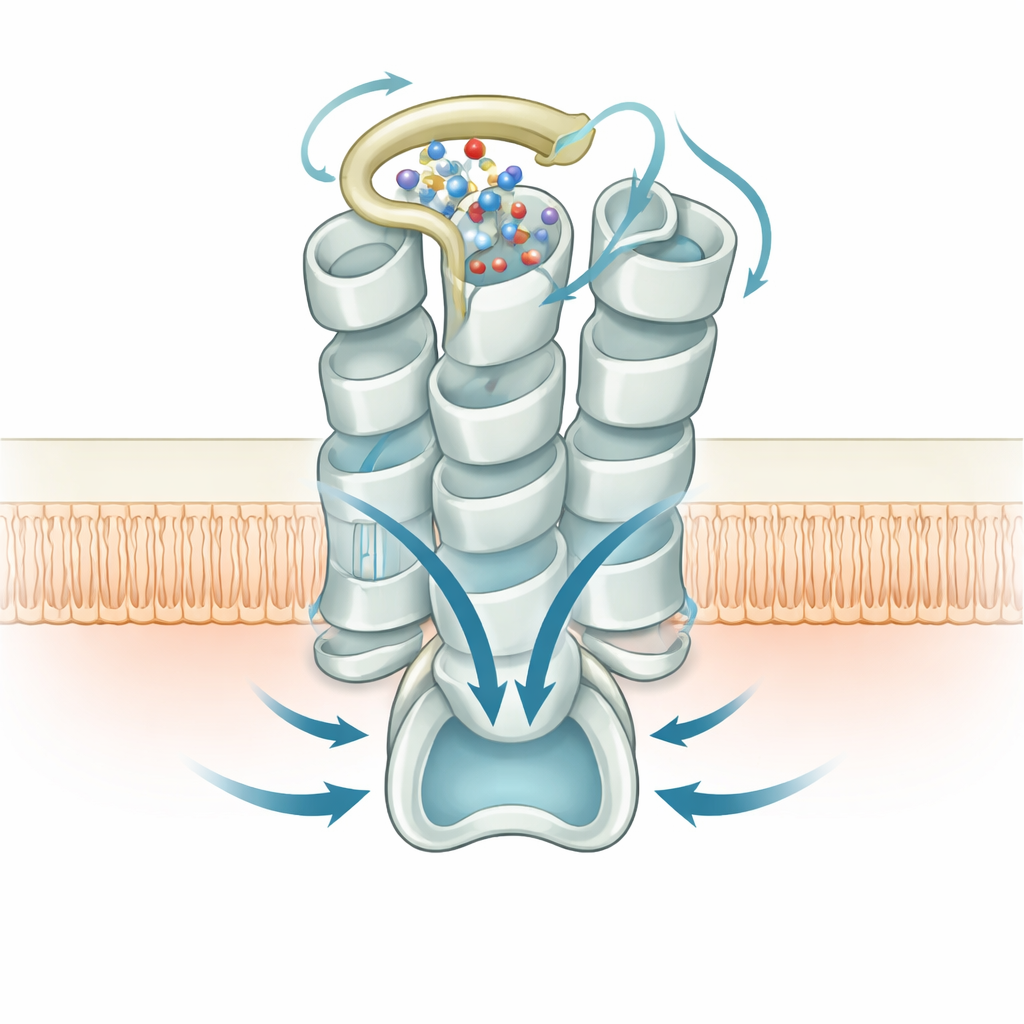
Implikacje dla oddychania i nie tylko
Autorzy sugerują, że wbudowana aktywność GPR99, wzmocniona przez strukturalne molekuły wody, może utrzymywać tkanki dróg oddechowych w trybie „gotowości” — przygotowane do uwalniania śluzu i uruchomienia odpowiedzi immunologicznej, gdy pojawią się zapalne lipidy lub zmiany metaboliczne. Ponieważ GPR99 jest wysoce aktywny nawet bez zewnętrznych sygnałów, a jego aktywacja opiera się na specyficznym układzie pętla‑woda, te strukturalne poznania oferują konkretne cele dla projektantów leków. Małe molekuły, które zaburzą ten wewnętrzny przełącznik lub sieć wodną, mogłyby stłumić nadmierne zapalenie, podczas gdy związki dopracowujące tę interakcję mogą wykorzystać wrażliwość GPR99 dla korzyści terapeutycznych.
Cytowanie: Xiao, M., Bao, X., Guo, Y. et al. Structural analysis reveals that water molecules mediate self-activation of GPR99. Commun Biol 9, 342 (2026). https://doi.org/10.1038/s42003-026-09644-5
Słowa kluczowe: GPR99, aktywacja GPCR, biologia strukturalna, zapalenie, sygnalizacja pośredniczona przez wodę