Clear Sky Science · pl
Mechanizm strukturalny przeciwciała przeciw MHC-I blokującego hamujące receptory komórek NK w odporności przeciwnowotworowej
Uwalnianie cichych zabójców nowotworów w organizmie
Nasz układ odpornościowy dysponuje potężnymi strażnikami zwanymi komórkami natural killer (NK), które potrafią rozpoznawać i niszczyć komórki nowotworowe oraz zakażone wirusem. Jednak guzy często uczą się je uciszać. Artykuł ten ujawnia, na poziomie atomowym, jak specjalnie zaprojektowane przeciwciało może zdjąć ten „przycisk wyciszenia”, ponownie pobudzając komórki NK do skuteczniejszej walki z nowotworem. Praca łączy zaawansowaną biologię strukturalną z eksperymentami na myszach, pokazując, jak jedno przeciwciało może uzupełniać istniejące immunoterapie przeciwnowotworowe.
Identyfikatory immunologiczne na powierzchni naszych komórek
Każda komórka w naszym organizmie prezentuje na powierzchni molekularne „identyfikatory” zwane cząsteczkami MHC klasy I. Te znaczniki pomagają komórkom odpornościowym odróżniać prawidłowe tkanki od niebezpiecznych komórek, które przekształciły się w nowotworowe lub zostały zakażone wirusem. Komórki NK nieustannie skanują te znaczniki. Gdy wykryją normalne wzorce, hamujące receptory na komórkach NK wysyłają sygnał uspokajający, który zapobiega atakowi. Guzy często utrzymują widoczne te znaczniki, wykorzystując je jako ochronną tarczę: dopóki płynie sygnał hamujący, komórki NK powstrzymują się od ataku, a rak może się rozwijać.
Przeciwciało chwytające tarczę
Naukowcy zbadali przeciwciało monoklonalne o nazwie B1.23.2, które silnie wiąże wiele wariantów ludzkich MHC klasy I na komórkach nowotworowych. Wykorzystując krioelektronową mikroskopię i krystalografię rentgenowską, odwzorowali dokładnie, jak przeciwciało osadza się na powierzchni MHC. B1.23.2 zaczepia się na konserwowanej grzędzie cząsteczki MHC — helisie α2 — nie dotykając łańcucha lekkiego partnera i tylko słabo reagując z prezentowanym peptydem. Oznacza to, że przeciwciało może rozpoznawać szerokie spektrum ludzkich cząsteczek MHC-A, -B i -C z bardzo wysokim powinowactwem, będąc jednocześnie stosunkowo niewrażliwym na konkretne krótkie fragmenty białkowe prezentowane przez MHC.
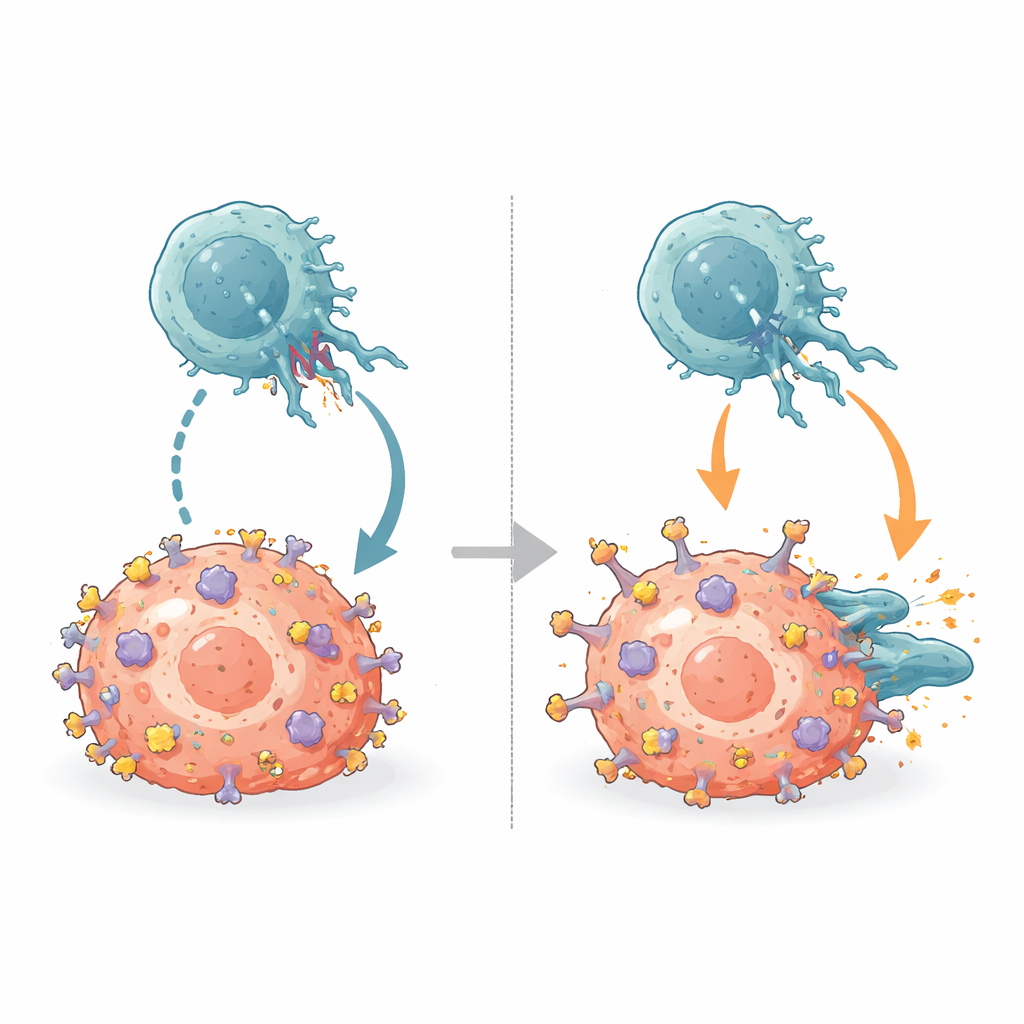
Wypieranie hamulców immunologicznych
Komórki NK noszą hamujące receptory zwane KIR, które normalnie osadzają się na tej samej grzędzie α2 MHC. Poprzez dopasowanie struktur przeciwciało–MHC do znanych struktur KIR–MHC, zespół wykazał, że B1.23.2 fizycznie zajmuje dokładnie ten fragment MHC, którego KIR potrzebują do przyłączenia. Miejsce wiązania przeciwciała i odciski KIR nakładają się tak rozlegle, że oba nie mogą się jednocześnie przyłączyć. B1.23.2 wiąże się również mocniej z MHC niż robią to KIR, co oznacza, że wygrywa to molekularne przeciąganie liny. W rezultacie, gdy przeciwciało pokrywa cząsteczki MHC na komórkach nowotworowych, receptory KIR na komórkach NK nie mogą już przekazywać swoich hamujących sygnałów, przesuwając równowagę w stronę aktywacji komórek NK.
Dopasowanie i szeroki zasięg działania
Choć B1.23.2 głównie celuje w konserwowaną powierzchnię MHC, autorzy stwierdzili, że drobne różnice w peptydzie związanym z MHC mogą subtelnie modulować siłę wiązania przeciwciała. Poprzez systematyczną zamianę pojedynczego miejsca aminokwasowego w peptydzie pokazali umiarkowane zmiany wiązania — generalnie w granicach około dziesięciokrotności — bez utraty ogólnego rozpoznania. Zbadali też, dlaczego niektóre powszechne typy MHC, takie jak HLA-A*02:01, unikają wiązania. Przeszczepiając kluczowe reszty kontaktowe z reagującego wariantu MHC do HLA-A*02:01, zespół skonstruował wersje, które przeciwciało potrafiło teraz rozpoznać, potwierdzając precyzyjnie, które pozycje tworzą krytyczną powierzchnię dokującą. Te wnioski sugerują, że przyszłe warianty przeciwciał mogłyby zostać zaprojektowane tak, by obejmować jeszcze więcej typów MHC lub selektywnie unikać niektórych z nich.
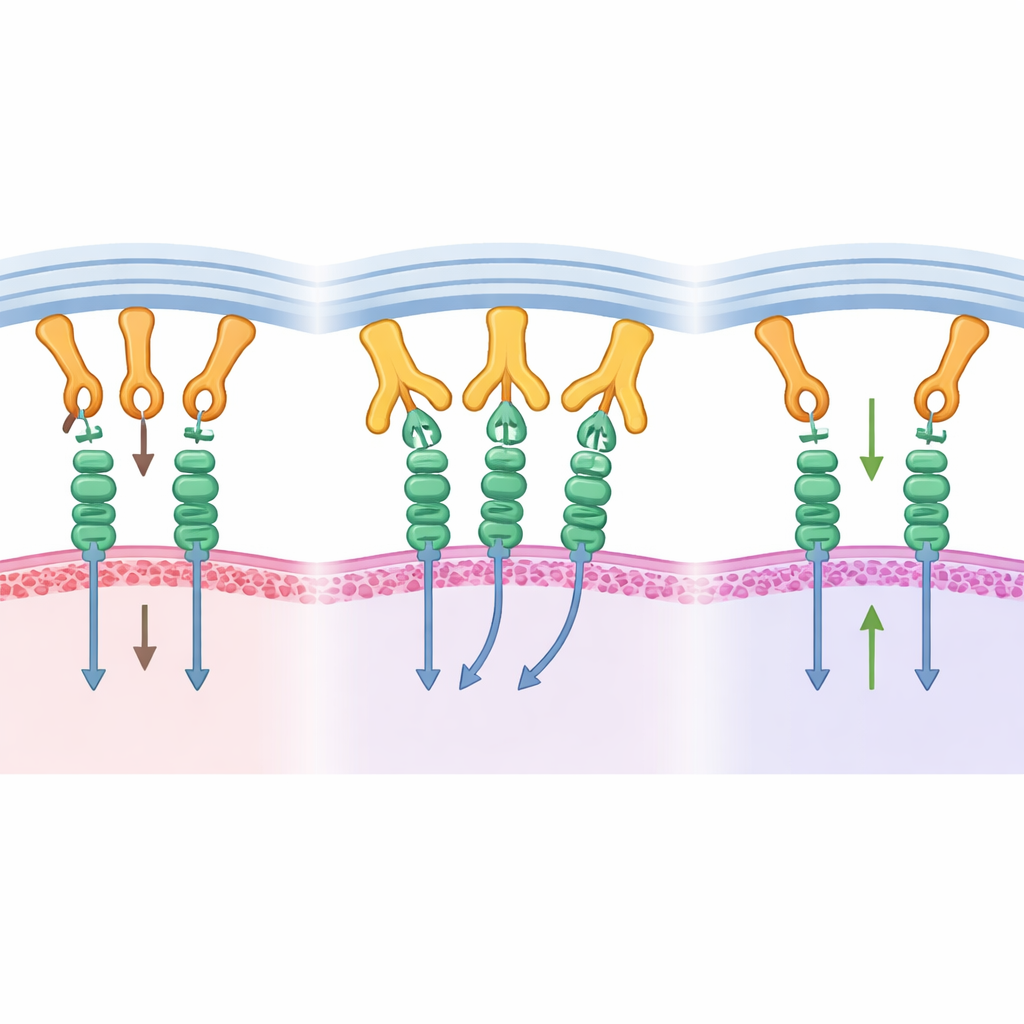
Przekuwanie wglądu strukturalnego w kontrolę guza
Czy to molekularne blokowanie rzeczywiście pomaga zwalczać guzy? Aby to sprawdzić, badacze użyli humanizowanego modelu mysiego niosącego ludzki rak trzustki. Zmodyfikowali formę B1.23.2 tak, by nie sygnalizowała przez własny ogon Fc, więc wszelkie efekty pochodziły głównie z blokowania interakcji MHC–KIR. Gdy myszy otrzymały przeciwciało wraz z ludzkimi komórkami NK, guzy rosły znacznie wolniej. Komórki NK wykazywały zwiększoną proliferację, wyższą aktywność szlaków wzrostu i sygnalizacyjnych oraz większą produkcję molekuł zapalnych związanych z zabijaniem komórek nowotworowych. W obrębie guzów komórki NK prezentowały więcej receptorów aktywujących, co jest zgodne z uwolnieniem ich spod stałego napływu sygnałów hamujących.
Co to może znaczyć dla przyszłych terapii przeciwnowotworowych
Mówiąc prosto, badanie pokazuje, jak pojedyncze przeciwciało może wślizgnąć się między komórki nowotworowe a hamulce układu odpornościowego, zatrzymując sygnał „nie atakuj”, który zwykle usypia komórki NK. Mapując interakcję w rozdzielczości atomowej i potwierdzając jej efekty u zwierząt, praca daje plan działania dla nowej klasy terapii: przeciwciał wiążących znaczniki identyfikacyjne guza, a nie same receptory odpornościowe. Takie środki mogłyby być łączone z istniejącymi inhibitorami punktów kontrolnych lub terapiami komórkowymi, aby zmobilizować zarówno komórki NK, jak i T, dając układowi odpornościowemu kolejny kierunek ataku przeciw trudnym do leczenia nowotworom.
Cytowanie: Jiang, J., Panda, A.K., Natarajan, K. et al. Structural mechanism of anti-MHC-I antibody blocking of inhibitory NK cell receptors in tumor immunity. Commun Biol 9, 350 (2026). https://doi.org/10.1038/s42003-026-09641-8
Słowa kluczowe: komórki natural killer, klasa I MHC, immunoterapia nowotworów, przeciwciała monoklonalne, receptory hamujące