Clear Sky Science · pl
LukS-PV celujący w C5aR hamuje EMT w raku wątrobowokomórkowym poprzez oś BCL6/HDAC6/HSPD1
Przekształcenie broni bakteryjnej w środek przeciwnowotworowy
Rak wątrobowokomórkowy, najczęstsza postać raka wątroby, często bywa śmiertelny, ponieważ rozprzestrzenia się z wątroby do innych narządów. Artykuł bada niespodziewanego sprzymierzeńca w walce z tym rozprzestrzenianiem: białko LukS-PV, będące składnikiem toksyny wytwarzanej przez bakterie Staphylococcus aureus. Badacze wykazują, że to białko przyłącza się do specyficznego receptora na komórkach raka wątroby i zamiast szkodzić tkankom prawidłowym, wyłącza kluczowe etapy umożliwiające komórkom nowotworowym odłączenie się, migrację i tworzenie nowych guzów.
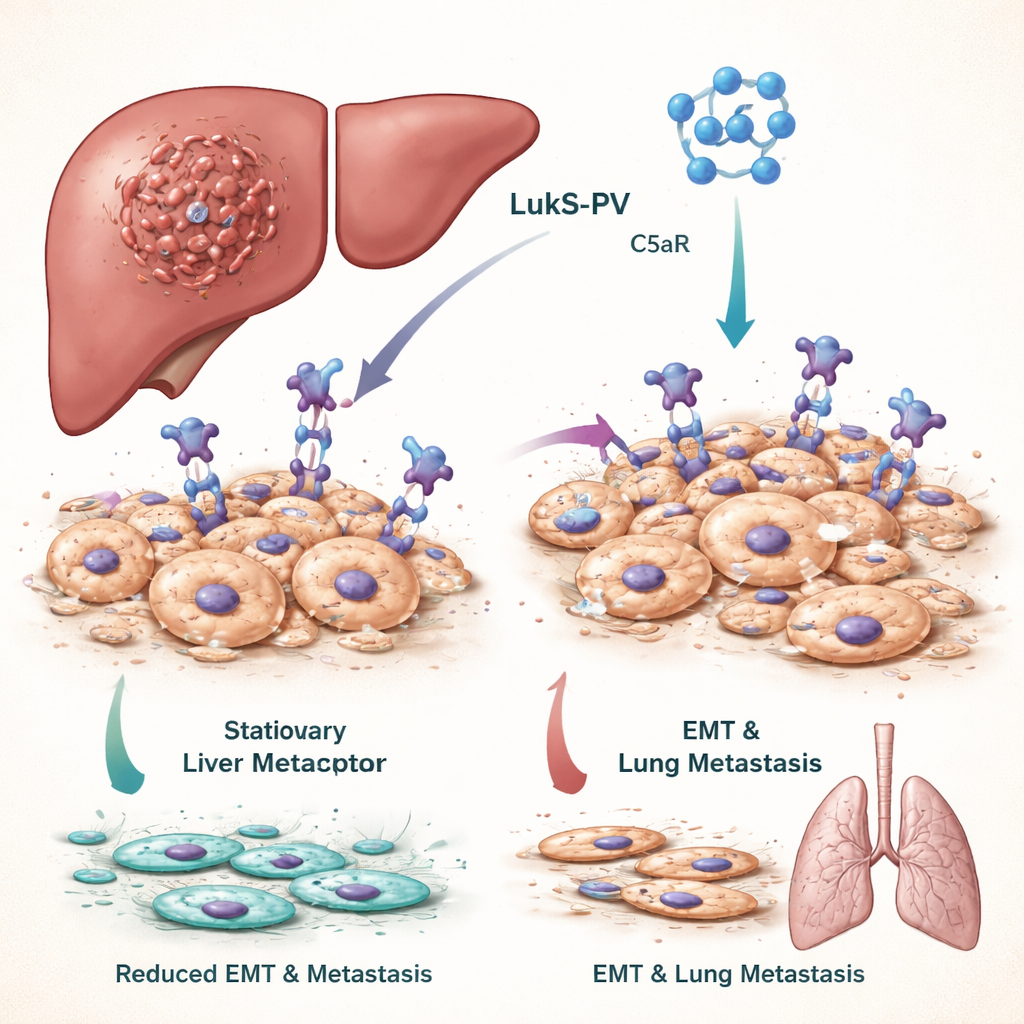
Dlaczego zatrzymanie „zmiany kształtu” komórek jest ważne
Aby rak wątroby się rozsiewał, komórki guza muszą przejść dramatyczną zmianę kształtu i zachowania zwaną przejściem nabłonkowo-mezenchymalnym (EMT). W EMT ciasno upakowane komórki, które normalnie pozostają na miejscu, stają się bardziej plastyczne, ruchliwe i inwazyjne, co pozwala im wnikać do naczyń krwionośnych i kolonizować odległe narządy, takie jak płuca. U pacjentów, których guzy wykazują silną aktywność EMT, rokowanie jest zwykle gorsze. Zespół skupił się na szlaku sygnałowym napędzanym przez cząsteczkę C5a i jej receptor C5aR, który jest nadmiernie obecny na wielu komórkach nowotworowych i wiadomo, że sprzyja EMT i przerzutom.
Składnik toksyny, który celuje w nowotworowy sygnał
Panton–Valentine leukocidin, toksyna Staphylococcus aureus, zawiera składnik LukS-PV, który naturalnie rozpoznaje i wiąże C5aR. Wcześniejsze prace autorów wykazały, że rekombinowana, niezawierająca aktywności tworzenia porów wersja LukS-PV potrafi hamować wzrost kilku nowotworów bez oczywistej toksyczności u zwierząt. W tym badaniu traktowali linie komórkowe raka wątroby LukS-PV i zaobserwowali, że komórki stają się mniej migrujące i inwazyjne. Testy molekularne ujawniły, że markery komórek stacjonarnych, „dobrze zachowujących się”, wzrosły, podczas gdy markery komórek agresywnych i ruchliwych spadły. U myszy wstrzykniętych komórkami raka wątroby leczenie LukS-PV doprowadziło do znacznie mniejszej liczby guzków w płucach, co wskazuje na ograniczenie przerzutów.
Blokowanie reakcji łańcuchowej wewnątrz komórek guza
Badając mechanizm głębiej, naukowcy odkryli kaskadę białek kontrolnych wewnątrz komórek nowotworowych, którą LukS-PV zaburza. Najpierw LukS-PV wiąże się z C5aR na powierzchni komórki i skutecznie blokuje pro-przerzutowy sygnał z C5a. Tłumienie tego sygnału obniża poziom białka BCL6, czynnika transkrypcyjnego, który zwykle włącza określone geny w jądrze. Jednym z celów BCL6 jest HDAC6, enzym usuwający małe chemiczne znaczniki zwane grupami acetylowymi z innych białek. Gdy BCL6 jest obfity, poziomy HDAC6 rosną, a komórka staje się bardziej podatna na EMT i migrację. Zakłócenie sygnalizacji C5aR przez LukS-PV zmniejsza BCL6, co z kolei obniża produkcję HDAC6 i spowalnia ten pro-przerzutowy program.
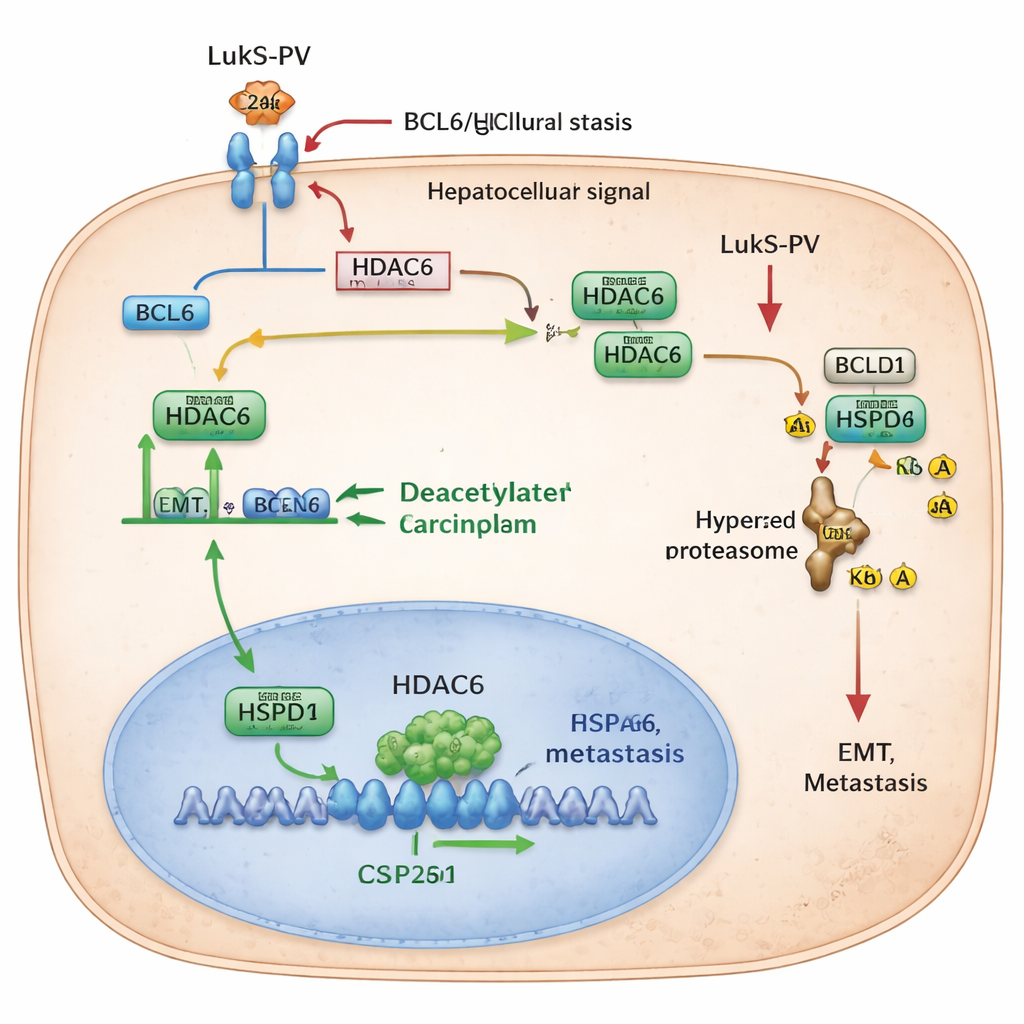
Oznaczanie chaperonu do zniszczenia
Zespół zidentyfikował następnie kluczowego partnera HDAC6 - HSPD1, znane też jako HSP60, białko „opiekun” (chaperon), które pomaga innym białkom poprawnie się fałdować i utrzymywać stabilność. W raku wątroby poziomy HSPD1 są wyższe niż w okolicznej tkance zdrowej i powiązane z gorszym przeżyciem pacjentów. Badacze odkryli, że HDAC6 fizycznie oddziałuje z HSPD1 i usuwa z niego grupy acetylowe w dwóch konkretnych miejscach. Gdy te znaczniki acetylowe zostają usunięte, HSPD1 staje się bardziej stabilny i wspiera EMT oraz przerzuty. Kiedy HDAC6 jest zredukowany — czy to genetycznie, czy w wyniku leczenia LukS-PV — HSPD1 ulega hiperacetylacji. Taka forma jest rozpoznawana przez komórkowe mechanizmy utylizacji, oznaczana ubikwityną i degradowana. W miarę spadku poziomów HSPD1 komórki nowotworowe tracą część zdolności do migracji, inwazji i kolonizacji płuc.
Od złożonych szlaków do prostego wniosku
Dla osoby niezaznajomionej ze szczegółami, przekaz jest taki: autorzy zmapowali efekt domina wewnątrz komórek raka wątroby — receptor powierzchniowy (C5aR) zwiększa poziom białka regulatorowego (BCL6), które podwyższa enzym (HDAC6), chroniący chaperon (HSPD1) przed degradacją. Razem te elementy pomagają komórkom nowotworowym zmieniać kształt, przemieszczać się i rozsiewać. LukS-PV, bakteryjne białko zaadoptowane w laboratorium, przerywa tę sekwencję już na powierzchni komórki, prowadząc ostatecznie do rozpadu HSPD1 i zahamowania przerzutów. Choć prace są wciąż na etapie eksperymentalnym, wyniki sugerują, że leki wzorowane na LukS-PV — albo celujące w BCL6, HDAC6 lub HSPD1 — mogą dać nowe możliwości powstrzymywania rozsiewu guzów wątroby i poprawy rokowania pacjentów.
Cytowanie: Ding, P., Shi, L., Xu, X. et al. LukS-PV targeting C5aR inhibits EMT in hepatocellular carcinoma via the BCL6/HDAC6/HSPD1 axis. Commun Biol 9, 314 (2026). https://doi.org/10.1038/s42003-026-09640-9
Słowa kluczowe: rak wątrobowokomórkowy, przerzuty, przejście nabłonkowo-mezenchymalne, HDAC6, terapia toksynami bakteryjnymi