Clear Sky Science · pl
PTBP1 wspiera spermatogenezę myszy, ułatwiając organizację cytoszkieletu poprzez szlak mTORC2–PKCα w komórkach Sertoliego
Dlaczego to badanie ma znaczenie dla płodności mężczyzn
Niezdolność do poczęcia u mężczyzn często wydaje się zagadkowa, ale w istocie zależy od precyzyjnej współpracy między tworzącymi się plemnikami a „opiekunkami”, które je wspierają. To badanie zagłębia się w jednego z ukrytych molekularnych pomocników w tych komórkach opiekuńczych i pokazuje, jak jego niewydolność może zatrzymać produkcję plemników. Zrozumienie tej ukrytej warstwy kontroli może wskazać drogę do nowych diagnostyk lub terapii dla niektórych form niepłodności męskiej.
Komórki wspierające, które umożliwiają powstawanie plemników
Plemniki powstają wewnątrz długich, skręconych kanalików w jądrach zwanych kanalikami nasiennymi. Wyściełające te kanaliki komórki Sertoliego to wyspecjalizowany typ komórek wspierających, które otulają rozwijające się komórki germinalne, odżywiają je i prowadzą w miarę ich podziałów i dojrzewania do postaci plemników. Komórki Sertoliego budują także ochronną barierę zwaną barierą krew–jądro, oddzielającą komórki we wczesnych stadiach rozwoju od układu odpornościowego. Do wykonywania tych funkcji potrzebują wewnętrznego rusztowania z filamentów aktynowych i mikrotubul, które nieustannie się przebudowuje, gdy fale komórek germinalnych przemieszczają się w kanalikach. Jeśli to rusztowanie zostanie zakłócone, bariera przecieka, a dojrzewające komórki germinalne mogą się odczepić lub obumrzeć, zagrażając płodności.
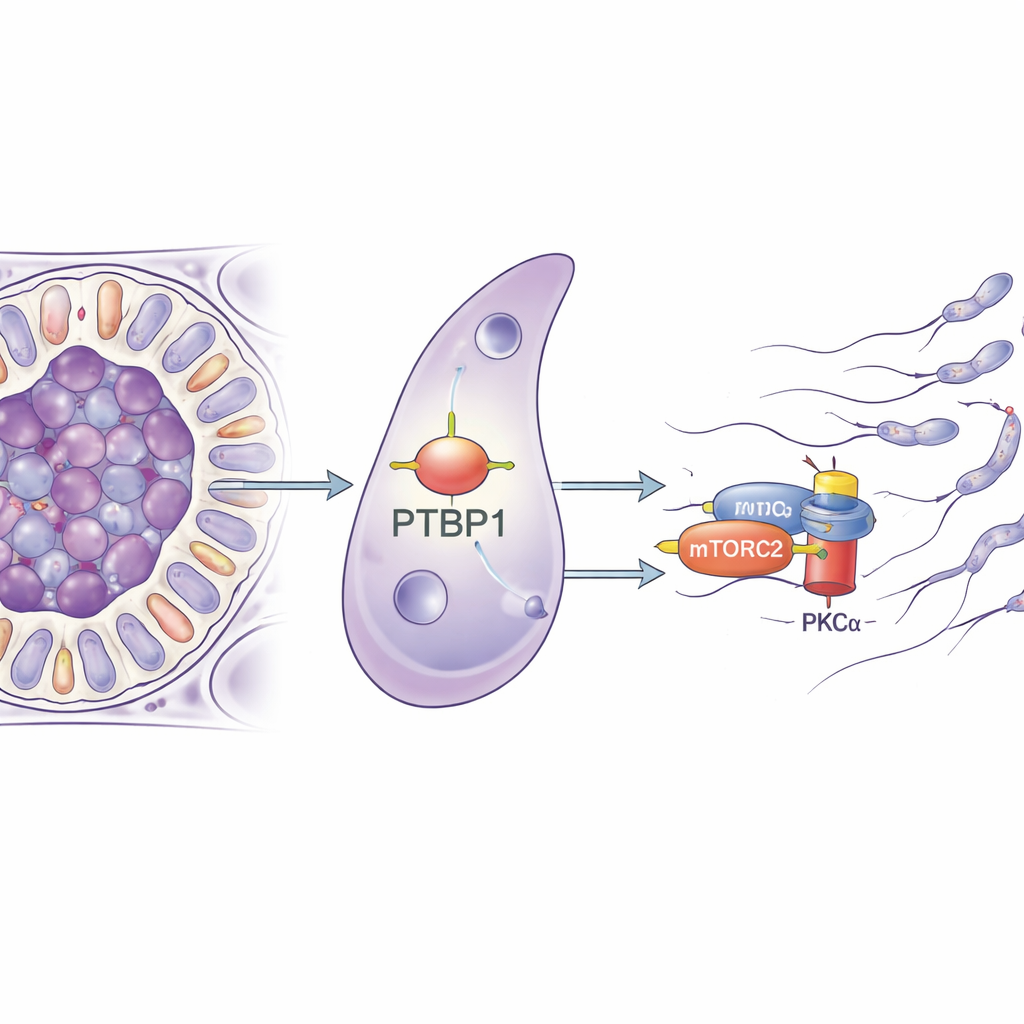
Maleńki menedżer RNA o wielkiej roli
Naukowcy skupili się na białku zwanym PTBP1, znanym przede wszystkim z roli w zarządzaniu cząsteczkami RNA w komórkach — decydowaniu o sposobie składania transkryptów, stabilności komunikatów i skuteczności przetwarzania na białko. PTBP1 jest obfite zarówno w komórkach germinalnych, jak i w komórkach Sertoliego; wcześniejsze badania wykazały, że usunięcie go z komórek germinalnych utrudnia produkcję plemników. W tym badaniu zespół specyficznie usunął PTBP1 jedynie z komórek Sertoliego u myszy. Początkowo młode myszy wydawały się normalne, ale w miarę dojrzewania płciowego ich jądra kurczyły się, liczba plemników w najądrzu gwałtownie spadła, a żaden z samców nie mógł spłodzić potomstwa — co ujawniło całkowitą utratę płodności.
Gdy wewnętrzne rusztowanie komórkowe się rozpada
Badania mikroskopowe jąder tych myszy pokazały, że spermatogeneza zatrzymała się w połowie drogi. W wielu kanalikach pojawiały się puste przestrzenie, nieprawidłowe skupiska zrośniętych jąder komórek germinalnych oraz niedobór w pełni wydłużonych plemników. Jądra komórek Sertoliego, które normalnie przylegają do zewnętrznej ściany kanalików, często były przesunięte w kierunku środka, co sugeruje, że komórki te tracą przyczepność do otaczającej struktury. Barwienia kluczowych składników połączeń komórkowych i białek strukturalnych potwierdziły osłabienie bariery krew–jądro oraz zastąpienie zwykłych zwartych pęków filamentów aktynowych przez zdezorganizowane, nadmiernie intensywne włókna rozciągające się od podstawy ku środkowi kanalika. Molekuła znacznikowa, która normalnie pozostaje po „krwistej” stronie bariery, zamiast tego przeciekała głęboko do kanalików, bezpośrednio dowodząc uszkodzenia bariery.
Śledzenie awarii do węzła sygnalizacyjnego
Aby zrozumieć, jak białko wiążące RNA mogło prowadzić do takichProblemów mechanicznych, zespół wyizolował komórki Sertoliego i przeanalizował, które geny zmieniają swoją aktywność po utracie PTBP1. Wiele zmienionych genów uczestniczyło w kontroli cytoszkieletu i adhezji międzykomórkowej, wskazując na szeroki defekt przebudowy. Naukowcy następnie wyłapali cząsteczki RNA fizycznie wiążące PTBP1 i odkryli, że PTBP1 przyłącza się do transkryptu Rictor, będącego kluczowym elementem kompleksu sygnalizacyjnego mTORC2. Ten kompleks z kolei aktywuje enzym PKCα, który kształtuje filamenty aktynowe. W komórkach Sertoliego pozbawionych PTBP1 spadła ilość białka RICTOR, a PKCα było znacznie mniej aktywne, mimo że poziom RNA Rictor zmienił się nieznacznie. Silnie sugeruje to, że PTBP1 pomaga komórkom Sertoliego wytwarzać wystarczającą ilość białka RICTOR z jego komunikatu RNA, utrzymując tym samym aktywność szlaku mTORC2–PKCα.
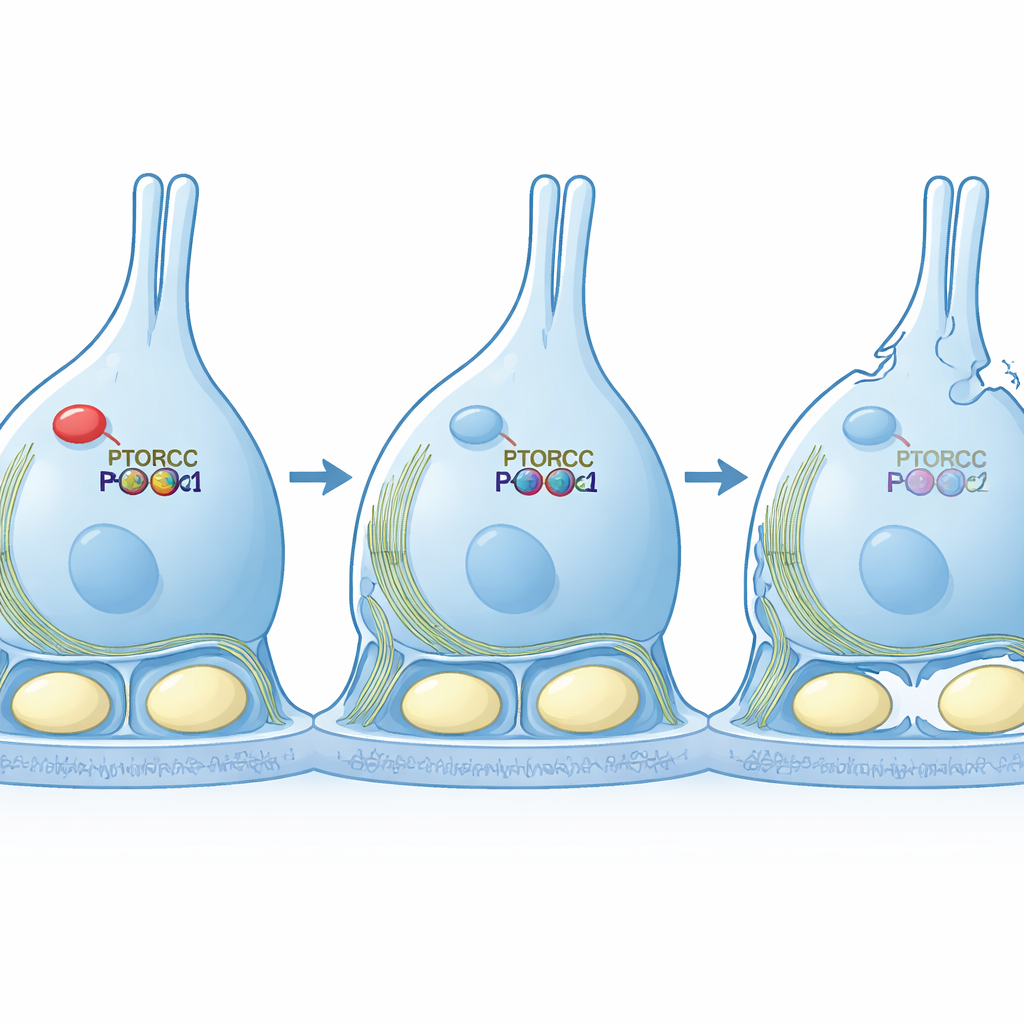
Przywracanie rusztowania przez odbudowę sygnalu
Zespół przeszedł następnie do modeli hodowli komórkowej, by przetestować związek przyczynowy. Gdy zredukowali PTBP1 w linii komórek podobnych do Sertoliego, komórki wydłużały się w cienkie formy i wykazywały rozbite sieci aktynowe — cechy osłabionej sygnalizacji mTORC2. Co ważne, gdy zmusili te komórki do produkcji trwale aktywnej wersji PKCα, odzyskały one normalny, zwarty kształt i bardziej uporządkowaną strukturę aktyny, mimo że poziom RICTOR pozostał niski. Eksperyment ratunkowy pokazuje, że główną rolą PTBP1 w tym kontekście jest utrzymanie wystarczająco silnego szlaku mTORC2–PKCα, by zorganizować wewnętrzne rusztowanie komórki.
Co to znaczy dla zrozumienia niepłodności
W prostych słowach, praca ta ujawnia łańcuch zależności w jądrze: PTBP1 pomaga komórkom Sertoliego zbudować kluczowy węzeł sygnałowy; ten węzeł organizuje ich wewnętrzny cytoszkielet; a nienaruszony cytoszkielet pozwala im utrzymać i chronić rozwijające się plemniki. Przerwij łańcuch na poziomie PTBP1, a komórki Sertoliego tracą strukturę, bariera ochronna zawodzi, a rozwój plemników się załamuje, prowadząc do męskiej niepłodności. Choć badania przeprowadzono na myszach, te same cząsteczki występują u ludzi, co rodzi możliwość, że subtelne zaburzenia kontroli RNA w komórkach Sertoliego mogą leżeć u podstaw niektórych niewyjaśnionych przypadków niepłodności męskiej i oferuje nowy zestaw molekularnych celów do dalszych badań.
Cytowanie: Ozawa, M., Taguchi, J., Mori, H. et al. PTBP1 supports mouse spermatogenesis by facilitating cytoskeletal organization through the mTORC2–PKCα pathway in Sertoli cells. Commun Biol 9, 341 (2026). https://doi.org/10.1038/s42003-026-09636-5
Słowa kluczowe: płodność męska, komórki Sertoliego, spermatogeneza, cytoszkielet, białka wiążące RNA