Clear Sky Science · pl
Ujemna regulacja szlaku NF-κB przez ligazę ubikwitynową Nedd4-1(NE)
Dlaczego wyłączanie stanu zapalnego ma znaczenie
Nasz układ odpornościowy polega na szybkich impulsach zapalnych, aby zwalczać infekcje i goić urazy, ale te same mechanizmy mogą uszkadzać tkanki i sprzyjać rozwojowi nowotworów, jeśli pozostaną włączone na zbyt długo. W artykule opisano, jak komórki ludzkie i innych naczelnych unikają tego zagrożenia dzięki nowo scharakteryzowanemu wbudowanemu „hamulcowi”, który wycisza jedno z kluczowych systemów alarmowych organizmu, gdy jego zadanie zostanie wykonane.
Centralny przełącznik alarmowy w naszych komórkach
W centrum tej historii stoi NF-κB, rodzina białek działających jak główny przełącznik dla setek genów zaangażowanych w stan zapalny, przeżycie komórek i odporność. Gdy komórki wykrywają sygnały stresowe, takie jak cząsteczka zapalna TNFα, łańcuch zdarzeń uwalnia NF-κB z jego „opiekunów” białkowych w płynie komórkowym i pozwala mu przenieść się do jądra, gdzie włącza geny prozapalne i promujące przeżycie. Ponieważ ten szlak jest tak silny, komórki muszą precyzyjnie regulować zarówno jego aktywację, jak i wygaszanie. Niezdolność do jego wyłączenia wiązana jest z przewlekłymi chorobami zapalnymi i wieloma nowotworami.
Hamulcowy mechanizm charakterystyczny dla naczelnych
Naukowcy skupili się na Nedd4-1, członku dużej rodziny enzymów, które znakują inne białka małą cząsteczką zwaną ubikwityną. Ten znacznik często kieruje białka na degradację lub przemieszczenie wewnątrz komórki, przekształcając sieci sygnałowe. Wcześniej odkryty wariant splicingu Nedd4-1, nazwany Nedd4-1(NE), występuje tylko u naczelnych i ma długi dodatkowy odcinek na początku, który zmienia jego lokalizację w komórce i to, co rozpoznaje. W przeciwieństwie do standardowej formy Nedd4-1, która poprzez innych partnerów może wzmacniać aktywność NF‑κB, zespół wykazał, że Nedd4-1(NE) działa odwrotnie: tłumi sygnalizację NF‑κB, szczególnie po długotrwałej ekspozycji na TNFα.
Dwa mechanizmy trzymania NF-κB w ryzach
Aby wyjaśnić mechanizm działania tego hamulca, autorzy zastosowali znakowanie proksymalne i metody wyłapywania białek, by zobaczyć, które cząsteczki fizycznie wiążą się z Nedd4-1(NE). Zidentyfikowali kluczowe składniki szlaku NF‑κB, w tym kinazę IKKβ i prekursor białka NF‑κB1 (zwany też p105). Dalsze eksperymenty pokazały, że Nedd4-1(NE) przyłącza ubikwitynę do IKKβ, prowadząc do jego degradacji. Przy niższym poziomie IKKβ jego zwykły cel, IκBα, nie jest już tak efektywnie fosforylowany i niszczony. W rezultacie IκBα pozostaje bardziej stabilny i utrzymuje aktywną podjednostkę NF‑κB, p50, związane w cytosolu, zapobiegając jej wejściu do jądra i uruchomieniu genów zapalnych.
Adaptor kierujący przekazaniem do hamulca
Nedd4-1(NE) działa także dalej w dół szlaku, ograniczając poziomy samego NF‑κB1. W tym przypadku enzym nie działa samodzielnie: współpracuje z innym białkiem znakującym ubikwityną zwanym KPC1. KPC1 pomaga przetwarzać prekursor NF‑κB1, p105, do aktywnej formy p50 i występuje w przedziałach komórkowych znanych jako późne endosomy, gdzie też znajduje się Nedd4-1(NE). Zespół wykazał, że Nedd4-1(NE) może ubikwitynować KPC1 i że zmodyfikowany KPC1 działa jako adaptor, rekrutując NF‑κB1 do Nedd4-1(NE) na późnych endosomach. Kompleks trójelementowy sprzyja destabilizacji zarówno p105, jak i p50, ponownie zmniejszając pulę NF‑κB, która może dotrzeć do jądra.
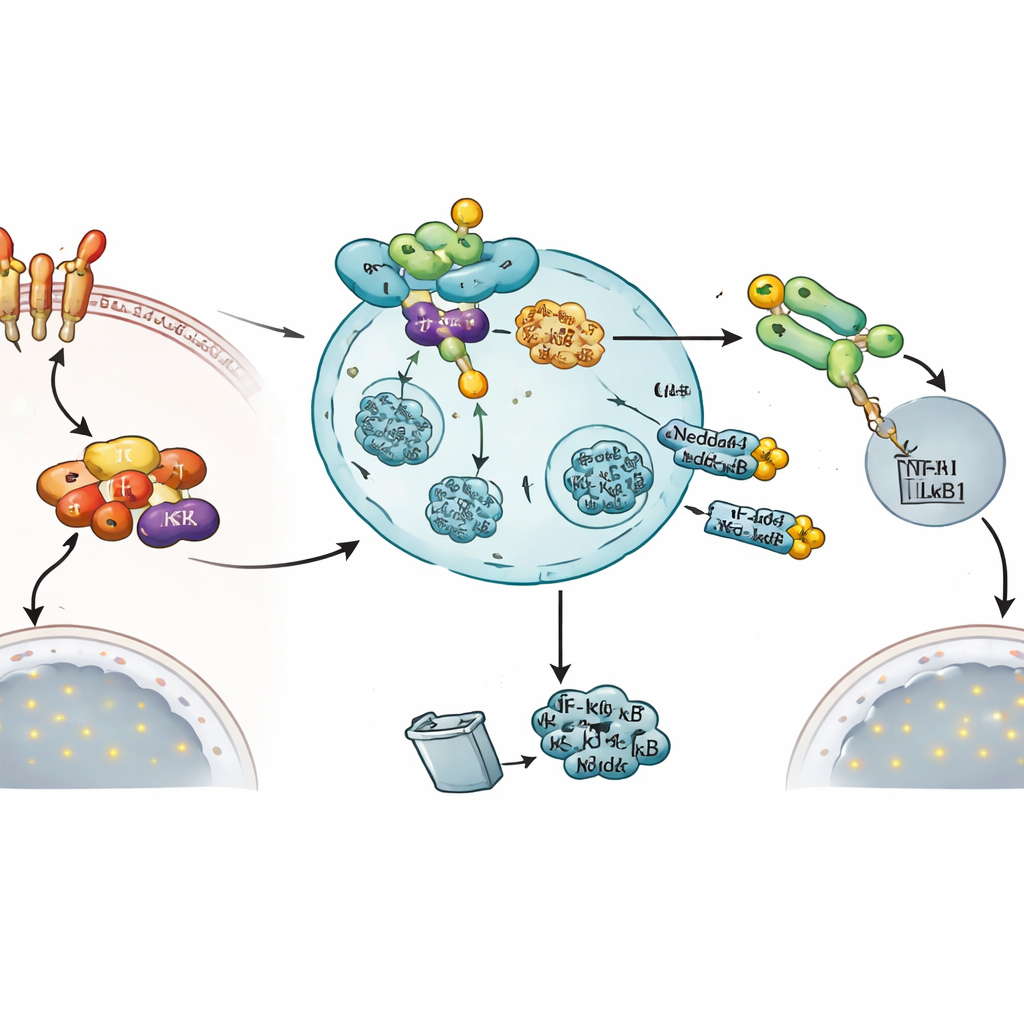
Wbudowana pętla ujemnego sprzężenia zwrotnego kończąca sygnał
Co istotne, sam sygnał aktywujący NF‑κB wydaje się również indukować ten hamulec. Po traktowaniu komórek TNFα poziomy mRNA dla Nedd4-1(NE) gwałtownie wzrastały, podczas gdy standardna forma Nedd4-1 nie ulegała zmianie. Odczyty funkcjonalne potwierdziły, że Nedd4-1(NE) działa jak zawór wyłączający: zwiększenie aktywnego Nedd4-1(NE) zmniejszało przemieszczanie NF‑κB1 do jądra, obniżało aktywność genu raportowego reagującego na NF‑κB i zmniejszało ekspresję regulowanego przez NF‑κB genu zapalnego TNFAIP3. Razem wyniki te opisują ujemne sprzężenie zwrotne, w którym aktywacja szlaku NF‑κB ostatecznie zwiększa poziom Nedd4-1(NE), który następnie celuje w dwa krytyczne węzły — IKKβ i NF‑κB1 — aby przywrócić odpowiedź zapalną do normy.
Co to oznacza dla zdrowia i chorób
Dla ogólnej publiczności kluczowa wiadomość jest taka, że nasze komórki wprowadziły dodatkowy, specyficzny dla naczelnych mechanizm bezpieczeństwa, który zapobiega wymykaniu się sygnalizacji zapalnej spod kontroli. Poprzez selektywne znakowanie i ograniczanie kluczowych składników systemu NF‑κB, Nedd4-1(NE) pomaga zakończyć odpowiedź na TNFα i może przyczyniać się do długoterminowej równowagi immunologicznej. Zrozumienie tego wbudowanego hamulca może otworzyć nowe drogi leczenia chorób, w których NF‑κB jest przewlekle nadaktywne, takich jak zaburzenia autoimmunologiczne i niektóre nowotwory, sugerując sposoby na naśladowanie lub wzmacnianie tego naturalnego procesu wygaszania.
Cytowanie: Persaud, A., Kefalas, G., Shteiman, A. et al. Negative regulation of the NF-κB pathway by the ubiquitin ligase Nedd4-1(NE). Commun Biol 9, 374 (2026). https://doi.org/10.1038/s42003-026-09634-7
Słowa kluczowe: sygnalizacja NF-kB, stan zapalny, ligaza ubikwitynowa, Nedd4-1(NE), TNF alfa