Clear Sky Science · pl
Notch3 reguluje fenotypową plastyczność perycytów w raku jelita grubego
Dlaczego naczynia krwionośne wokół guzów mają znaczenie
Rak jelita grubego jest jednym z najczęstszych i najbardziej śmiertelnych nowotworów na świecie, lecz większość terapii skierowana jest bezpośrednio na komórki nowotworowe i często pomija otaczający je system wsparcia, który ułatwia wzrost guza. W artykule skupiono się na mniej znanej grupie komórek wspomagających, zwanych perycytami, które otaczają drobne naczynia krwionośne. Odkrywając, jak przełącznik sygnałowy o nazwie Notch3 zmienia zachowanie perycytów, autorzy pokazują, jak unaczynienie guza może być skierowane ku nieszczelnym, chaotycznym naczyniom sprzyjającym nowotworowi albo ku bardziej prawidłowym naczyniom, które mogą spowalniać chorobę i poprawiać skuteczność leczenia. 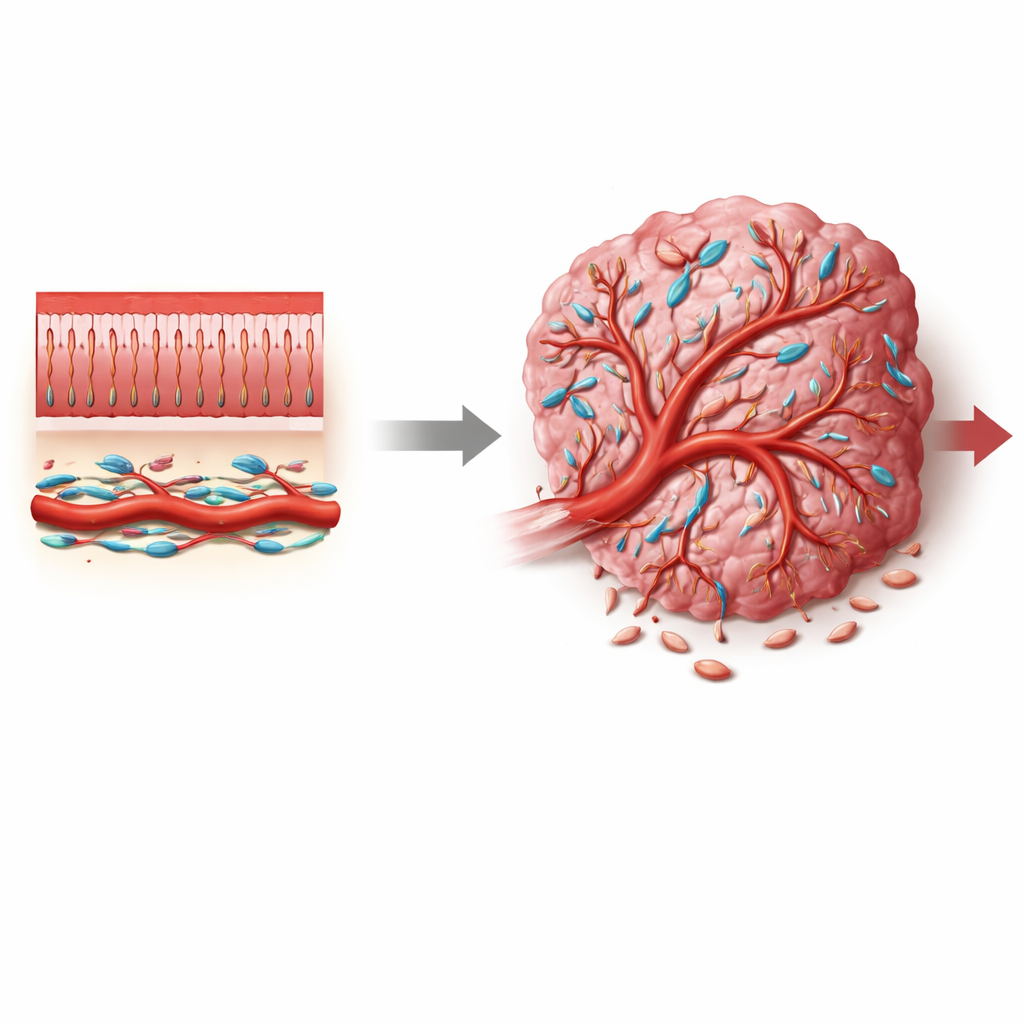
Ukryci pomocnicy wokół naczyń guza
Naczynia krwionośne to więcej niż puste rurki. W zdrowych tkankach małe naczynia są ściśle otoczone przez perycyty — wyspecjalizowane komórki stabilizujące ściany naczyń, regulujące przepływ krwi i ograniczające przeciekanie. W guzach jednak perycyty często wyglądają i zachowują się inaczej: mogą odłączać się, namnażać lub zmieniać swoją tożsamość, przyczyniając się do nieprawidłowej, nieszczelnej sieci naczyniowej typowej dla nowotworów. W rakach jelita grubego, gdzie mikrośrodowisko jest gęsto zaludnione przez fibroblasty, komórki odpornościowe i komórki naczyniowe, nie było jasne, skąd pochodzą perycyty związane z guzem, jakie stany przyjmują i które sygnały molekularne skłaniają je do ról sprzyjających nowotworowi.
Śledzenie perycytów podczas formowania się guzów
Aby obserwować perycyty w czasie, badacze wykorzystali modele myszy z rakiem jelita grubego powiązanym z zapaleniem, w których mogli genetycznie „oznaczać” konkretne typy komórek i śledzić ich losy. Wykazali, że perycyty obecne w guzach w dużej mierze pochodzą z normalnych, rezydujących w tkance perycytów, które rozszerzają się i proliferują w miarę rozwoju nowotworu, zamiast napływać z odległych źródeł, takich jak szpik kostny. Dzięki zaawansowanemu sekwencjonowaniu RNA pojedynczych komórek skatalogowali dziesiątki tysięcy komórek zrębu z mysich guzów i zdrowego jelita grubego i stwierdzili, że perycyty są znacząco wzbogacone w mikrośrodowisku guza. Zidentyfikowali też podobną ekspansję perycytów w kilku zestawach danych dotyczących ludzkiego raka jelita grubego, co podkreśla, że zjawisko to nie jest specyficzne tylko dla myszy.
Przełącznik molekularny zmieniający zachowanie perycytów
Zespół następnie zapytał, które sygnały kształtują zachowanie perycytów w guzach i odkrył, że Notch3 — receptor umożliwiający komórkom komunikację z sąsiadami — jest szczególnie aktywny w perycytach guzów. Analiza komputerowa komunikacji międzykomórkowej sugerowała, że perycyty zarówno wysyłają, jak i odbierają sygnały związane z Notch, zwłaszcza poprzez partnerów na komórkach naczyniowych. Sztuczne włączenie Notch3 w perycytach spowodowało, że te komórki proliferowały bardziej, ale wykazywały niższą ekspresję białek kurczliwych typowo związanych ze stabilizacją naczyń. Naczynia krwionośne w tych mysich modelach stały się większe, bardziej nieszczelne i wyścielone większą liczbą proliferujących komórek śródbłonka, co wskazuje na mniej stabilne unaczynienie. Przeciwnie, usunięcie Notch3 zmniejszyło proliferację komórek śródbłonka, skurczyło rozmiar naczyń i obniżyło przeciekanie, sugerując przesunięcie w kierunku bardziej znormalizowanych naczyń bez dramatycznej zmiany liczby lub wczesnego rozmiaru guzów. 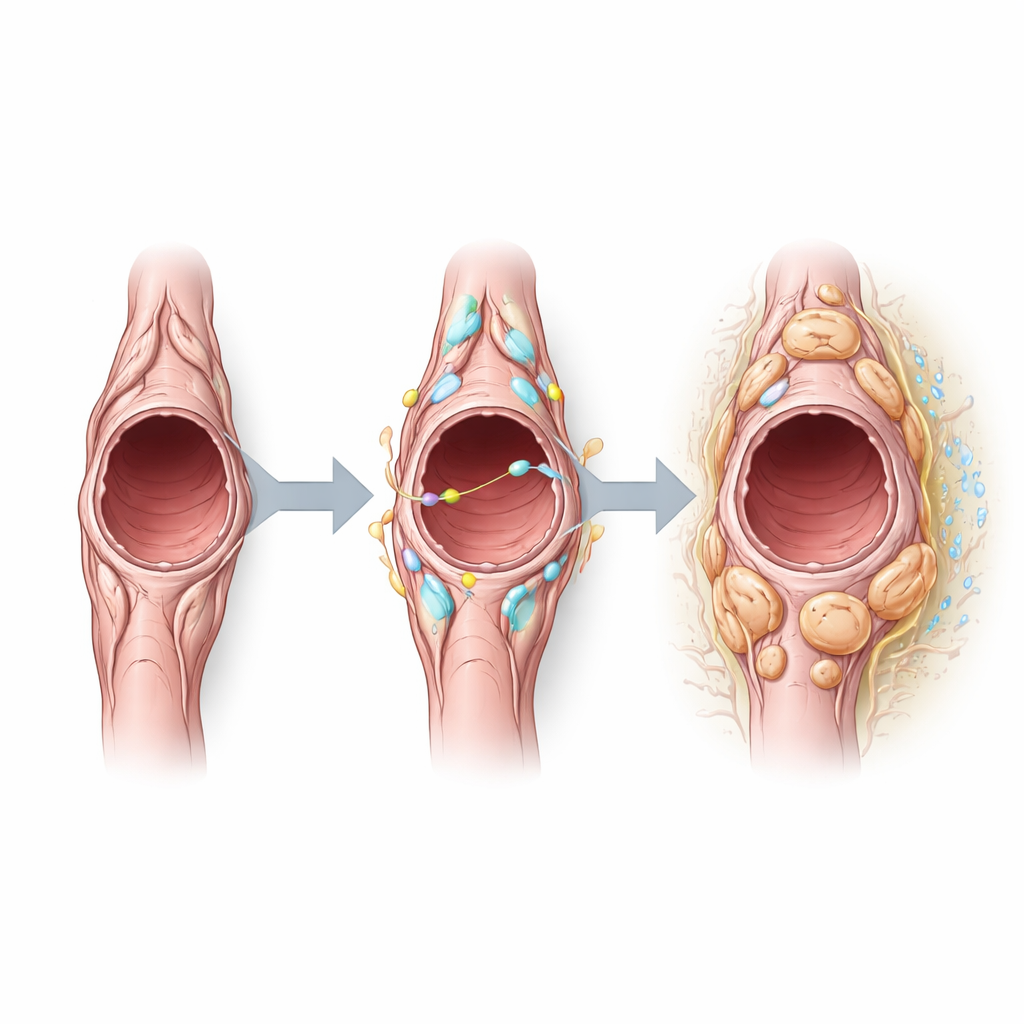
Wiele oblicz perycytów wewnątrz guzów
Ponad prostymi zmianami włącz/wyłącz, badanie ujawniło, że perycyty guzów występują w kilku odrębnych stanach. Niektóre podgrupy wykazywały cechy silnie kurczliwych komórek, inne produkowały duże ilości macierzy zewnątrzkomórkowej, niektóre przejawiały cechy zapalne, a pewien podzbiór nawet nosił sygnatury zwykle obserwowane w komórkach śródbłonka. Aktywność Notch3 nie była równomiernie rozłożona: była wzbogacona w populacji „syntetycznych” perycytów produkujących macierz i niska w bardziej kurczliwym podzbiorze. Analizy trajektorii sugerowały, że perycyty mogą przemieszczać się ze stanu kurczliwego w kierunku stanu syntetycznego i proliferacyjnego w miarę wzrostu aktywności Notch3. Gdy autorzy zbadali dane z ludzkiego raka jelita grubego, znaleźli porównywalne spektrum stanów perycytów i ponownie zaobserwowali wyższą aktywność genu docelowego Notch3 w perycytach związanych z guzem i proliferujących, co odzwierciedla wyniki z myszy.
Przemiana chaosu naczyń w okazję terapeutyczną
Podsumowując, praca przedstawia Notch3 jako kluczowy regulator, który stroi tożsamość perycytów, a przez nie — strukturę i funkcję naczyń krwionośnych guza. Wysoka aktywność Notch3 popycha perycyty w kierunku stanu proliferacyjnego i mniej kurczliwego, powiązanego z powiększonymi, nieszczelnymi naczyniami sprzyjającymi progresji nowotworu. Niska aktywność Notch3 wiąże się z bardziej kurczliwymi perycytami, spokojniejszymi komórkami śródbłonka i bardziej znormalizowanym unaczynieniem, które może hamować wzrost guza i poprawiać dostarczanie leków. Celowanie w Notch3 specyficznie w perycytach może w przyszłości pozwolić skierować naczynia guza z chaosu ku stabilności, oferując nowy wariant terapii zaawansowanego raka jelita grubego w połączeniu z istniejącymi lekami.
Cytowanie: Chalkidi, N., Stavropoulou, A., Arvaniti, VZ. et al. Notch3 regulates pericyte phenotypic plasticity in colorectal cancer. Commun Biol 9, 343 (2026). https://doi.org/10.1038/s42003-026-09629-4
Słowa kluczowe: rak jelita grubego, mikrośrodowisko guza, perycyty, sygnalizacja Notch3, naczynia krwionośne guza