Clear Sky Science · pl
Endotelialny TRIM47 reguluje integralność bariery krew–mózg i funkcje poznawcze poprzez szlak sygnałowy KEAP1/NRF2 u myszy
Dlaczego ochrona drobnych naczyń mózgu ma znaczenie
Choroba małych naczyń mózgowych to cichy sprawca kłopotów w mózgu. Uszkadza najmniejsze naczynia krwionośne, zwiększa ryzyko udaru i stopniowo osłabia pamięć oraz zdolności myślowe, a mimo to lekarzom nadal brakuje terapii likwidujących jej zasadnicze przyczyny biologiczne. W tym badaniu przyjrzano się jednemu białku, TRIM47, występującemu w komórkach wyściełających naczynia mózgowe, aby postawić proste, lecz istotne pytanie: czy pomaga utrzymać ochronną barierę krew–mózg oraz czy ma to znaczenie dla funkcji poznawczych?
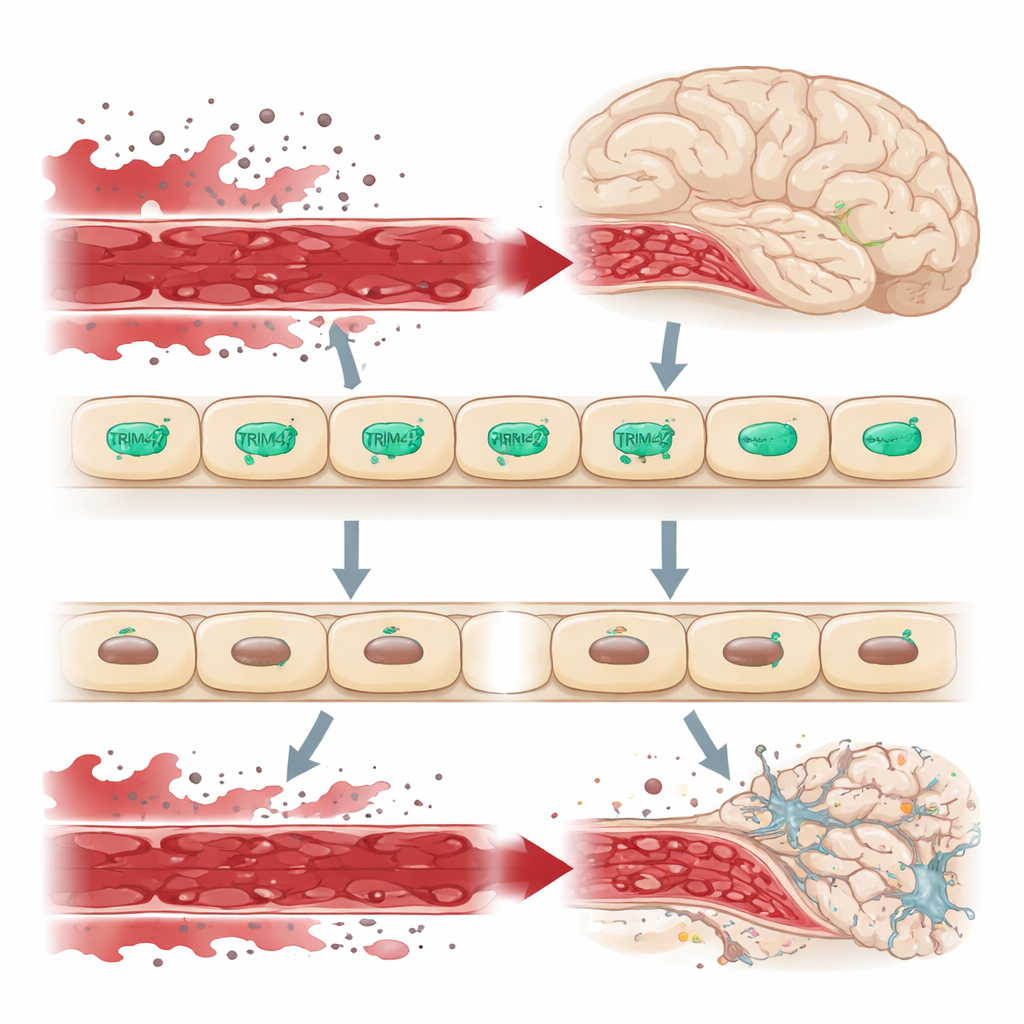
Stróż na granicy mózgu
Mózg jest osłonięty przed krążeniem reszty ciała przez barierę krew–mózg — szczelne wyściółki komórek śródbłonka, które ściśle kontrolują, co może przedostać się do tkanki mózgowej. Jeśli ta bariera przecieka, szkodliwe cząsteczki z krwi przenikają do mózgu, obciążając neurony i komórki wspierające oraz przyczyniając się do schorzeń takich jak demencja. Badania genetyczne na dużych populacjach ludzkich wskazały fragment DNA zawierający gen TRIM47 jako region związany z ryzykiem choroby małych naczyń mózgowych. TRIM47 jest szczególnie aktywny w komórkach śródbłonka mózgowego, co sugeruje, że może pełnić ważną rolę w ochronie tej bariery.
W jaki sposób TRIM47 uzbraja komórki przeciw stresowi oksydacyjnemu
Autorzy najpierw badali ludzkie komórki śródbłonka mózgowego hodowane w laboratorium i obniżyli poziomy TRIM47 za pomocą interferencji RNA. To wywołało szerokie zmiany w aktywności genów, a najsilniej dotknięta sieć koncentrowała się wokół NRF2 — głównego regulatora komórkowych mechanizmów antyoksydacyjnych. W warunkach prawidłowych NRF2 jest hamowany przez białko KEAP1, które kieruje je do degradacji. Zespół wykazał, że TRIM47 wiąże się z KEAP1 i pomaga zapobiegać rozkładowi NRF2. W obecności TRIM47 NRF2 może się kumulować, przenikać do jądra komórkowego i włączać geny detoksykujące reaktywne formy tlenu. Gdy TRIM47 zostaje utracony, poziomy NRF2 spadają, geny antyoksydacyjne są mniej aktywne, a komórki śródbłonka stają się bardziej podatne na stres oksydacyjny.
Od nieszczelnych naczyń do problemów z pamięcią u myszy
Aby zbadać, jak ten mechanizm działa w żywym mózgu, naukowcy stworzyli myszy pozbawione genu Trim47 w całym organizmie oraz linię, w której Trim47 można było usunąć wyłącznie w komórkach śródbłonka. Dorosłe zwierzęta obu modeli wykazywały wyraźne zaburzenia uczenia się przestrzennego i pamięci, nie radząc sobie w zadaniach takich jak labirynt w kształcie litery Y czy test Morrisa, mimo prawidłowej sprawności ruchowej. Badanie mózgów wykazało, że bariera krew–mózg stała się nieszczelna: małe fluorescencyjne znaczniki i białka krwi przedostawały się z naczyń do otaczającej tkanki. Kluczowe białka „uszczelniające”, tworzące połączenia zamykające i adherens między komórkami śródbłonka, zwłaszcza Claudin-5 i Occludin, były zmniejszone. Sąsiednie astrocyty, komórki podporowe o gwiaździstym kształcie, które szybko reagują na uszkodzenia, uległy aktywacji, choć na tym etapie było mało oznak szeroko zakrojonego zapalenia czy utraty neuronów.
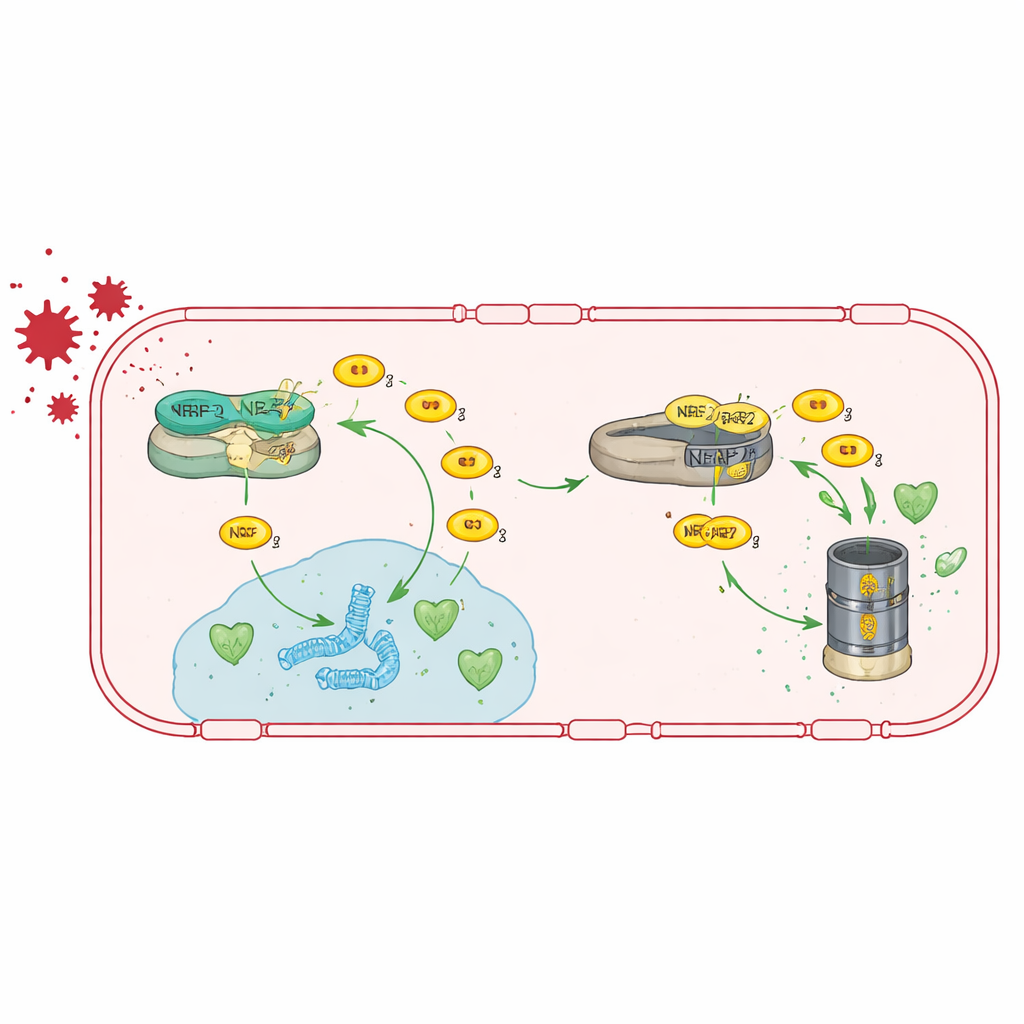
Ponowne włączenie szlaku antyoksydacyjnego
Ponieważ TRIM47 działa głównie poprzez wzmacnianie aktywności NRF2, zespół przetestował, czy można obejść jego utratę, bezpośrednio stymulując NRF2. Podawano myszom pozbawionym Trim47 dietę zawierającą tert-butylochino-1,4-diol (tBHQ), związek znany ze stabilizowania NRF2 i uruchamiania jego genów docelowych. To leczenie przywróciło aktywność genów antyoksydacyjnych w komórkach śródbłonka mózgowego, przywróciło ekspresję genów tworzących połączenia ścisłe w kierunku normy i zmniejszyło przeciekanie bariery krew–mózg. Co istotne, normalizowało także aktywację astrocytów i przywróciło wyniki zwierząt w testach pamięci, co sugeruje, że wzmocnienie tego szlaku antyoksydacyjnego może odwrócić zarówno zmiany naczyniowe, jak i poznawcze, przynajmniej u myszy.
Wskazówki z ludzkiej krwi i dalsze kroki
Aby powiązać eksperymenty na myszach z chorobą u ludzi, badacze przeanalizowali białka związane ze szlakiem NRF2 w próbkach krwi tysięcy osób, które miały badania rezonansem magnetycznym mózgu. Poziomy kilku białek regulowanych przez NRF2 korelowały z obrazowymi markerami choroby małych naczyń, takimi jak powiększone przestrzenie okołonaczyniowe i zmiany w istocie białej. Wspiera to koncepcję, że zaburzona sygnalizacja TRIM47–NRF2 ma znaczenie u ludzi, nie tylko u zwierząt doświadczalnych, i że te białka mogłyby służyć jako biomarkery nasilenia choroby lub jej postępu.
Co to oznacza dla zdrowia mózgu
Sumarycznie praca przedstawia TRIM47 jako molekularnego ochroniarza, który pomaga naczyniom mózgowym przeciwstawiać się uszkodzeniom oksydacyjnym, stabilizując system antyoksydacyjny NRF2. Gdy TRIM47 jest nieobecny lub upośledzony, bariera krew–mózg osłabia się, kumulują się subtelne urazy mózgu, a pamięć zaczyna zawodzić. Ponowne uruchomienie szlaku NRF2 może naprawić barierę i przywrócić funkcje poznawcze u myszy, co wskazuje na ten szlak sygnałowy jako obiecujący cel terapeutyczny w naczyniowych formach demencji. Chociaż samo tBHQ nie nadaje się jako lek dla ludzi, bezpieczniejsze związki wzmacniające NRF2 lub strategie naśladujące ochronną rolę TRIM47 mogłyby pewnego dnia pomóc zachować zdrowie mózgu przez wzmocnienie jego najmniejszych, najbardziej wrażliwych naczyń.
Cytowanie: Delobel, V., Grenier, C., Boulestreau, R. et al. Endothelial TRIM47 regulates blood-brain barrier integrity and cognition via the KEAP1/NRF2 signalling pathway in mice. Commun Biol 9, 399 (2026). https://doi.org/10.1038/s42003-026-09628-5
Słowa kluczowe: choroba małych naczyń mózgowych, bariera krew–mózg, TRIM47, szlak NRF2, otępienie naczyniowe