Clear Sky Science · pl
Do pełnej współpracy między podjednostkami wymagana jest ścieżka pośrednia dla entropicznie napędzanego i negatywnie kooperatywnego wiązania nukleotydów cyklicznych w kanale HCN2
Jak mały zegar serca wyczuwa sygnały chemiczne
Każde uderzenie serca i wiele rytmów mózgowych zależy od mikroskopijnych kanałów, które otwierają się i zamykają w błonach naszych komórek. Te kanały, zwane kanałami rozrusznikowymi HCN, są kontrolowane nie tylko przez napięcie elektryczne, lecz także przez małe cząsteczki sygnałowe znane jako nukleotydy cykliczne. Badanie stawia pozornie proste pytanie o dalekosiężnych implikacjach: jak te drobne cząsteczki wiążą się ze kanałem HCN2 w sposób skoordynowany i jak subtelne zaburzenia tego procesu mogą przyczyniać się do schorzeń, takich jak padaczka?
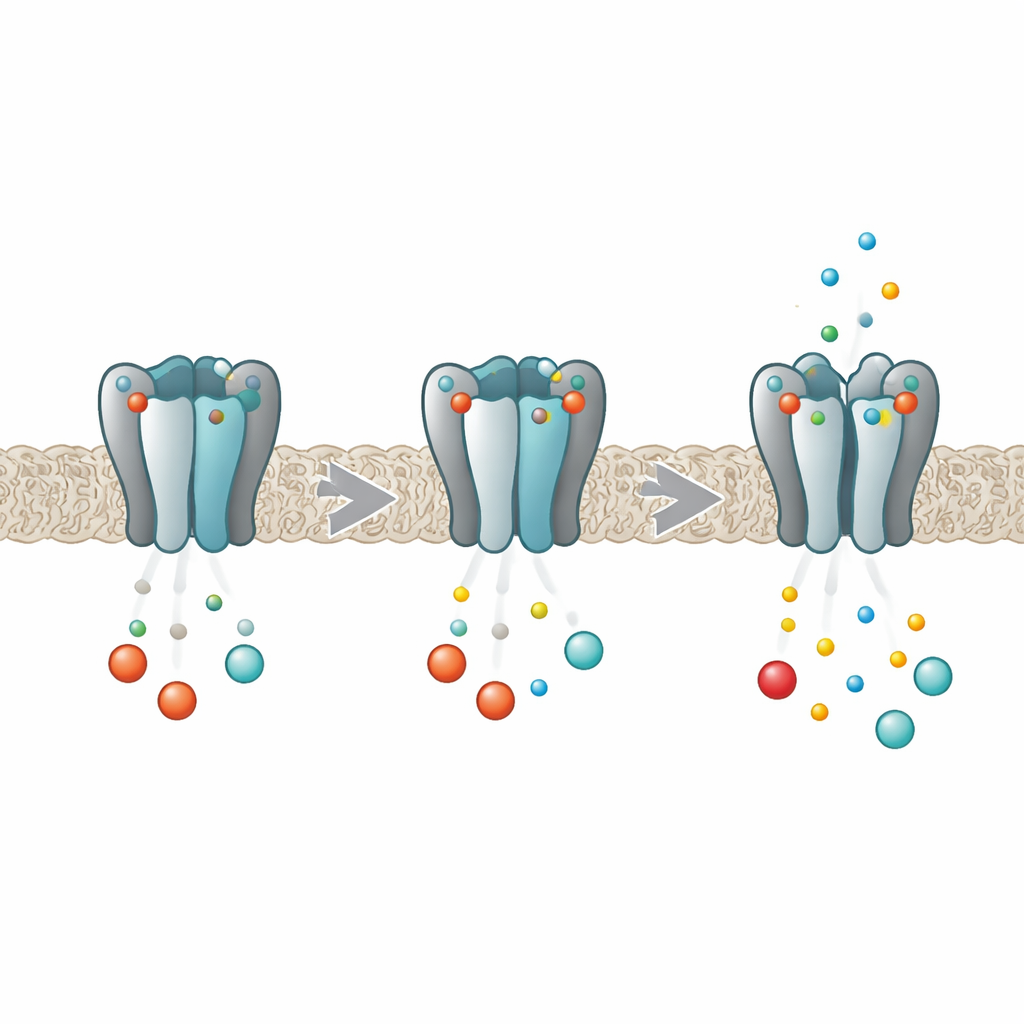
molekularny ściemniacz dla rytmów organizmu
Kanały HCN działają jak ściemniacze aktywności elektrycznej w komórkach serca i mózgu. Każdy kanał zbudowany jest z czterech identycznych podjednostek, które razem tworzą centralny otwór przez który przepływają jony. Głęboko w każdej podjednostce znajduje się kieszeń, która może chwytać nukleotydy cykliczne, takie jak cAMP i cGMP. Gdy te przekaźniki się z nimi łączą, ułatwiają otwarcie otworu, zwiększając prąd rozrusznikowy. Wcześniejsze prace wykazały, że w wariancie HCN2 wiązanie nie zachodzi niezależnie w każdej kieszeni; zamiast tego cztery miejsca wpływają na siebie nawzajem tak, że pierwsza cząsteczka wiąże się chętniej niż kolejne, co nazywa się negatywną kooperatywnością. Nowe badanie miało odkryć, w jaki sposób dokładnie cztery podjednostki komunikują się ze sobą podczas tego procesu.
Podjednostki, które „czują” swoich sąsiadów
Naukowcy połączyli symulacje komputerowe z pomiarami laboratoryjnymi na izolowanych fragmentach kanału HCN2. Wykorzystując długie symulacje dynamiki molekularnej, obserwowali, jak region ogonowy kanału — część zawierająca kieszenie na nukleotydy cykliczne i tzw. C‑linker łączący z otworem — wygina się i kołysze w zależności od liczby związanych cząsteczek cAMP lub cGMP. Stwierdzili, że gdy przekaźnik zajął jedno miejsce, nie stabilizował jedynie tej podjednostki. Zamiast tego subtelnie zmieniał stabilność sąsiadów, czasem czyniąc je bardziej sztywnymi, czasem bardziej elastycznymi, mimo że ogólny kształt białka prawie się nie zmieniał. Te wpływy między sąsiadami zależały od liczby zajętych miejsc i ich rozmieszczenia wokół pierścienia, co odpowiadało zachowaniom oczekiwanym przy negatywnej kooperatywności.
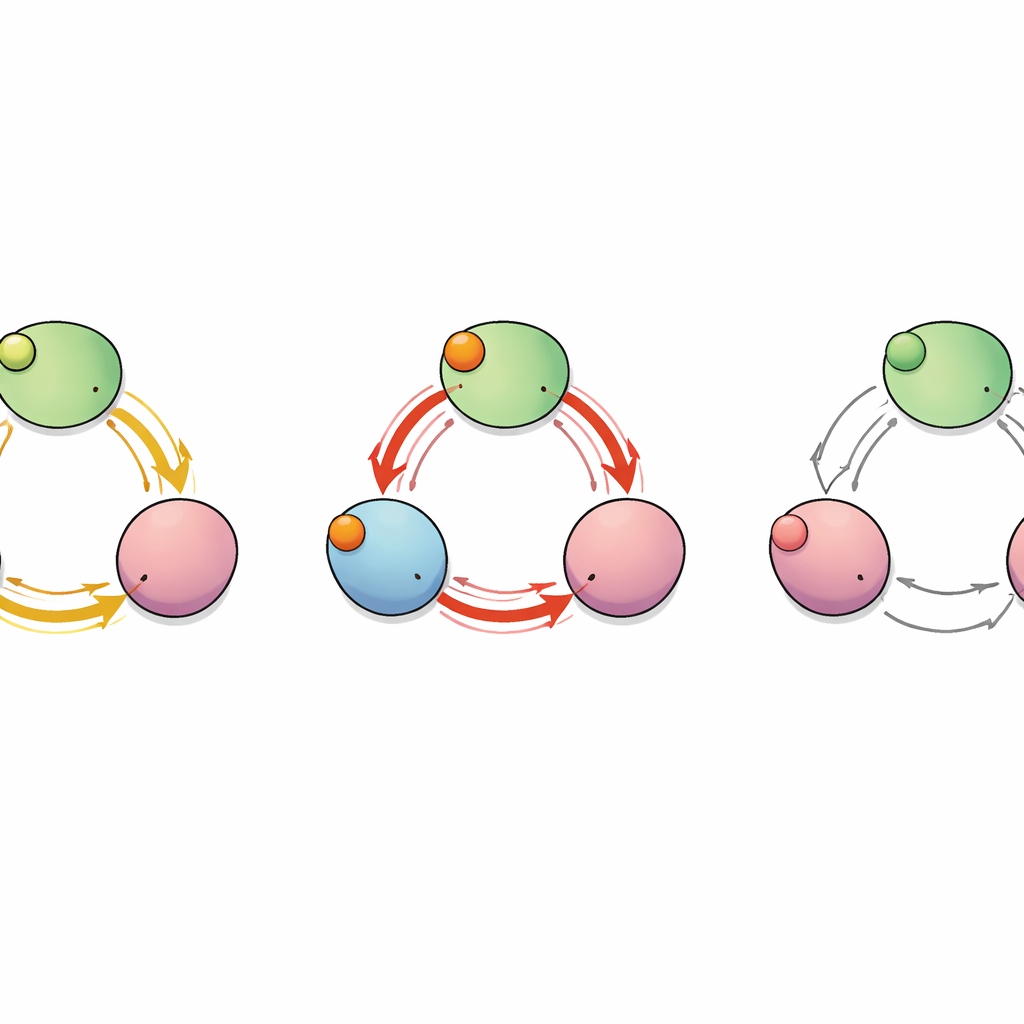
Ukryta ścieżka między podjednostkami
Aby odwzorować, jak „sygnał” wiązania przemieszcza się przez białko, zespół potraktował kanał jako sieć oddziałujących aminokwasów. Obliczyli, które reszty poruszały się w sposób skorelowany w trakcie symulacji i zastosowali narzędzia teorii grafów, by zidentyfikować najkrótsze i najwydajniejsze ścieżki komunikacji od kieszeni wiążących do segmentów C‑linker kontrolujących otwór. Analiza ujawniła kilka możliwych tras, z których dwie wyróżniały się: jedna pozostająca w obrębie pojedynczej podjednostki i druga przeskakująca z jednej podjednostki na sąsiednią. Wzdłuż tej między‑podjednostkowej trasy pojedyncza reszta — glutaminian na pozycji 488 (E488) — działała jako krytyczny węzeł, przez który przechodziło wiele najkrótszych ścieżek, sugerując, że może być kluczowym przekaźnikiem dla kooperatywnego wiązania.
Mutacje, które przerywają rozmowę
Autorzy zwrócili się następnie do eksperymentów z oczyszczonymi ogonami kanału, by przetestować znaczenie tej ścieżki. Zmienili E488 oraz pobliską tyrozynę 459 (Y459), która leży na sąsiedniej podjednostce, gdzie ścieżka się kończy. Za pomocą dynamicznego rozpraszania światła potwierdzili, że białka mutantów nadal składają się w kompleksy czteropodjednostkowe, ale nie wykazywały silnego ligandem indukowanego „dociśnięcia” między podjednostkami obserwowanego w białku dzikiego typu. Kalorymetria tandemu izotermicznego, śledząca maleńkie ciepła wiązania, ujawniła jeszcze większą różnicę: HCN2 typu dzikiego wykazywał dwa odrębne zdarzenia wiązania — krok o wysokim powinowactwie napędzany głównie wzrostem entropii (większym ruchem wewnętrznym), po którym następowały trzy kroki o niższym powinowactwie. W przeciwieństwie do tego mutanty w E488 lub Y459 wykazywały tylko jeden, umiarkowany tryb wiązania, pozbawiony korzystnego entropijnego wzmocnienia i pozbawiony cechowej negatywnej kooperatywności.
Dlaczego subtelne zmiany entropii mają znaczenie
Składając te elementy w całość, badanie kreśli obraz kanału HCN2 jako dynamicznego pierścienia czterech podjednostek połączonych specyficznymi „ścieżkami rozmów”. Gdy pierwszy nukleotyd cykliczny się wiąże, modyfikuje ruchy odległych części pierścienia przez E488 i Y459, sprawiając, że późniejsze zdarzenia wiązania są mniej korzystne i precyzując, jak otwór reaguje. Efekt ten jest napędzany nie dużymi przemianami strukturalnymi, lecz przesunięciami w wewnętrznej elastyczności — zmianami entropii, niewidocznymi na statycznych migawkach, ale kluczowymi dla funkcji. Mutacje zakłócające kluczowe reszty wzdłuż tej między‑podjednostkowej ścieżki „uciszają” rozmowę, likwidują negatywną kooperatywność i wiążą się z chorobami, takimi jak idiopatyczna uogólniona padaczka. Dla czytelnika nieznającego szczegółów wniosek jest taki, że krytyczne przełączniki w sercu i mózgu opierają się na misternie zorganizowanych molekularnych „szeptach” między podjednostkami białek, a zrozumienie tych szeptów pomaga wyjaśnić zarówno normalne rytmy, jak i to, co się dzieje, gdy się one psują.
Cytowanie: Costa, F., Ng, L.C.T., Chow, S.S. et al. An inter-subunit path is required for entropically-driven and negatively cooperative binding of cyclic nucleotides in the HCN2 channel. Commun Biol 9, 362 (2026). https://doi.org/10.1038/s42003-026-09626-7
Słowa kluczowe: kanał jonowy HCN2, wiązanie nukleotydów cyklicznych, negatywna kooperatywność, komunikacja allosteryczna, mutacja związana z padaczką