Clear Sky Science · pl
Mała cząsteczka allosterycznie aktywuje zależny od SecA system sekrecji
Przekształcenie doków wysyłkowych bakterii w nadmiarowy tryb pracy
Bakterie przetrwają, stale eksportując białka przez maleńkie bramki w swoich błonach. Te eksporty pomagają im budować ściany komórkowe, wydzielać toksyny i przystosowywać się do stresu — procesy kluczowe w wielu infekcjach. W badaniu opisano mały związek chemiczny, nazwany HSI#6, który robi coś nietypowego: zamiast blokować maszynerię eksportową, przełącza ją w hiperaktywny, mniej selektywny tryb. Zrozumienie, jak działa ten przełącznik, może ujawnić nowe strategie przeciwbakteryjne i dać biotechnologii sposób na zwiększanie wydajności sekrecji białek na żądanie.
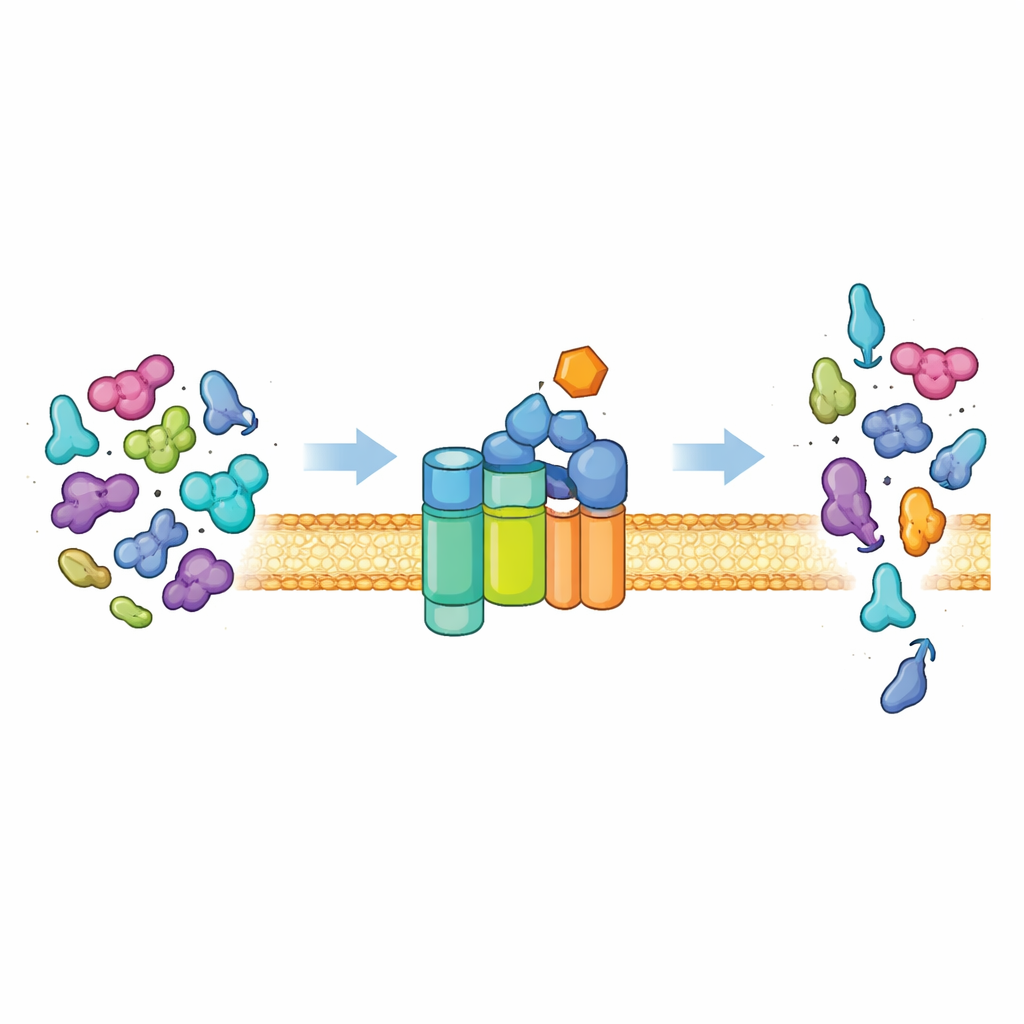
Bramka wyjścia białek w komórce
Większość bakterii wysyła białka na zewnątrz przez uniwersalną ścieżkę znaną jako system Sec. W jego centrum znajduje się kanał błonowy (SecYEG) oraz motor białkowy (SecA), który zużywa paliwo komórkowe (ATP), aby przepychać niezwinięte łańcuchy białkowe przez kanał. W normalnych warunkach system jest wybiórczy. Przede wszystkim eksportuje „prebiałka” niosące specjalne znaczniki adresowe, zwane peptydami sygnałowymi, oraz dodatkowe cechy w domenie głównej. Te elementy są potrzebne, aby przełączyć SecA ze stanu spoczynkowego o niskiej aktywności w silny motor. Tylko białka z właściwą kombinacją sygnałów potrafią odblokować pełną aktywność, co zapewnia, że komórka eksportuje właściwy ładunek i utrzymuje zwykłe białka cytoplazmatyczne bezpiecznie wewnątrz.
Mała cząsteczka, która budzi motor
Naukowcy odkryli HSI#6 w przesiewie związków wpływających na bakteryjną sekrecję białek i wzrost. Testy biochemiczne wykazały, że HSI#6 wiąże się bezpośrednio z SecA z siłą w zakresie mikromolarnym i zmienia efektywność wykorzystania ATP. W roztworze związek sprawia, że SecA silniej wiąże ATP; gdy SecA jest przyłączony do kanału, HSI#6 zarówno poprawia wiązanie ATP, jak i przyspiesza jego obrót. Ten wzorzec to znak rozpoznawczy aktywatora allosterycznego: molekuły, która wiąże się w jednym miejscu białka, a zmienia aktywność w innym, odległym miejscu. W przeciwieństwie do naturalnych klientów białkowych, HSI#6 nie musi pełnić roli ładunku, by pobudzić motor — po prostu dostraja wewnętrzną dynamikę SecA, tak że cała translokaza staje się katalitycznie przygotowana.
Z filtra selektywnego w maszynę „promiskuitywną”
Po związaniu HSI#6 system Sec przestaje wymagać zwykłych znaczników eksportowych. W eksperymentach in vitro związek w przybliżeniu podwajał sekrecję standardowego prebiałka i czynił kompleks bardziej odpornym na azotan sodu, znany inhibitor SecA. Co bardziej uderzające, HSI#6 pozwolił dzikiej, „naturalnej” maszynerii przesuwać białka pozbawione peptydów sygnałowych, a także białka normalnie występujące w cytoplazmie. W żywych komórkach bakteryjnych ten sam efekt zaobserwowano przy użyciu reporterów opartych na fosfatazie alkalicznej: gdy białka cytoplazmatyczne były połączone z enzymem sekrecyjnym, obecność HSI#6 powodowała wyraźny wzrost aktywności wydzielanej bez zmiany ilości wytwarzanego białka. Innymi słowy, HSI#6 skutecznie rozłącza eksport od zwykłych kontroli tożsamości klienta, przekształcając system Sec w szeroko działającą pompę eksportową dla dowolnego wystarczająco niezwiniętego białka.
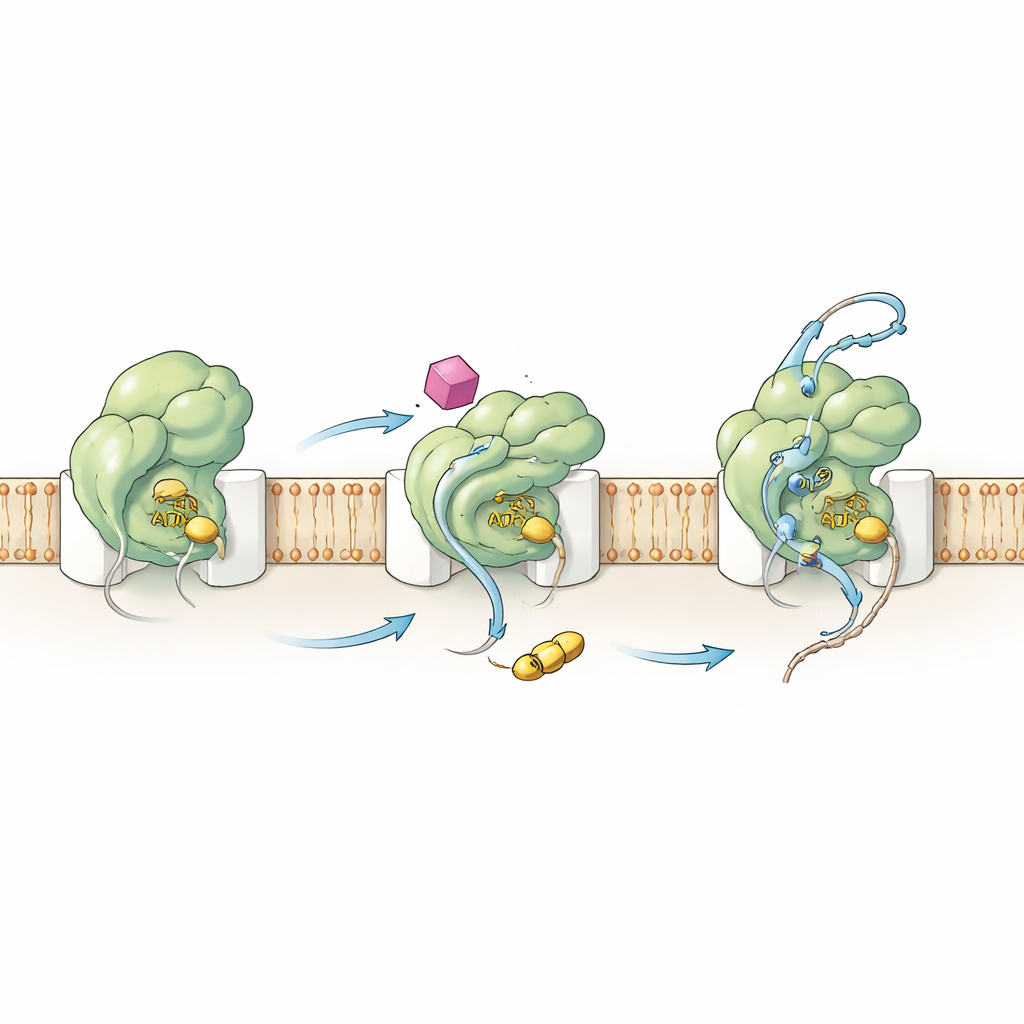
Przeprogramowanie motoru od wewnątrz
Aby zrozumieć, jak HSI#6 wywołuje to zachowanie, zespół zbadał zarówno chemię, jak i ruchy SecA. Pomiary kinetyczne wykazały, że związek przesuwa kluczowy krok aktywacji w górę ścieżki: kompleks SecA–kanał staje się katalitycznie aktywny nawet przed przyłączeniem klienta białkowego. HSI#6 także ułatwia SecA uwolnienie zużytego paliwa (ADP), co normalnie jest wolnym, ograniczającym szybkość krokiem, i w ten sposób wspiera szybszy cykl ATP. Przy użyciu spektrometrii mas z wymianą wodór–deuter (HDX-MS) autorzy zmapowali, jak HSI#6 zmienia elastyczność różnych regionów SecA. Związek selektywnie rozluźnia części białka, które wyczuwają klientów i łączą się z kanałem, jednocześnie usztywniając region rusztowania, który prawdopodobnie gości miejsce wiązania. Powstały wzorzec ruchu przypomina już zaangażowany, „włączony” stan translokazy, sugerując, że HSI#6 stabilizuje formę aktywowaną — być może faworyzując monomeryczne SecA związane z kanałem — bez obecności klienta.
Znaczenie dla medycyny i biotechnologii
Pokazując, że mała cząsteczka może allosterycznie aktywować SecA i odebrać mu normalną selektywność klientów, praca ta odkrywa nowy sposób kontroli centralnej maszyny bakteryjnej. W kontekście chorób zakaźnych wymuszone, niekontrolowane wydzielanie może osłabić patogeny poprzez drenaż energii i zakłócenie ich precyzyjnie wyregulowanych programów eksportu, co czyni aktywatory podobne do HSI#6 atrakcyjnymi punktami wyjścia do projektowania antybiotyków — lub wskazówkami przy tworzeniu przyszłych inhibitorów blokujących te same cechy regulacyjne. W biotechnologii ta sama zasada mogłaby zostać wykorzystana do zwiększenia sekrecji użytecznych białek rekombinowanych, bez potrzeby projektowania peptydów sygnałowych czy skomplikowanych modyfikacji genetycznych. W istocie badanie demonstruje, że bakteryjny „dok wysyłkowy” białek można chemicznie przeprogramować, otwierając nowe drogi zarówno do walki z mikroorganizmami, jak i wykorzystania ich jako mikroskopijnych fabryk.
Cytowanie: Sedky, H., Hamed, M.B., Krishnamurthy, S. et al. A small molecule allosterically activates SecA dependent secretion. Commun Biol 9, 368 (2026). https://doi.org/10.1038/s42003-026-09623-w
Słowa kluczowe: bakteryjna sekrecja białek, translokaza SecA, aktywacja allosteryczna, regulatory małocząsteczkowe, odkrywanie leków przeciwbakteryjnych