Clear Sky Science · pl
LncRNA P4HA2-AS1 napędza śródmiąższowe włóknienie nerek poprzez K63-ubikwitynację ULK1 zależną od TRIM32 i zaburzenia autofagii
Dlaczego bliznowacenie nerek ma znaczenie
Przewlekła choroba nerek dotyka setek milionów osób na całym świecie i często postępuje po cichu, aż dializa lub przeszczep stają się jedynymi sposobami na przeżycie. U podstaw tego pogorszenia leży proces zwany bliznowaceniem, w którym prawidłowa tkanka nerkowa stopniowo zostaje zastąpiona sztywnym, nieczynnym materiałem. W tym badaniu postawiono proste, lecz kluczowe pytanie: jakie molekularne przełączniki wewnątrz komórek nerek popychają je w kierunku szkodliwego bliznowacenia i czy można te przełączniki odwrócić?
Ukryty przełącznik RNA w komórkach nerek
Nasze nerki filtrują krew za pomocą rozbudowanych sieci maleńkich kanalików. Gdy te kanaliki są uszkadzane przez zablokowany odpływ moczu, wysoki poziom glukozy we krwi lub nagły spadek dopływu krwi, mogą reagować poprzez tworzenie tkanki bliznowatej między komórkami. Naukowcy przeanalizowali nerki myszy z różnymi typami urazów i porównali je ze zdrowymi nerkami za pomocą sekwencjonowania RNA — techniki wskazującej, które geny są aktywne. Odkryli, że słabo poznana cząsteczka o nazwie P4HA2-AS1, długie niekodujące RNA, które nie koduje białka, była konsekwentnie podwyższona w uszkodzonych, tworzących blizny nerkach oraz w ludzkich komórkach nerkowych poddanych stresowi w laboratorium. To RNA znajdowano głównie w płynnej części komórek, co sugeruje, że może ono regulować inne białka w tym obszarze. 
Obniżenie poziomu RNA jako ochrona nerek
Aby sprawdzić, czy P4HA2-AS1 jest tylko biernym wskaźnikiem czy aktywnym czynnikiem uszkodzenia, zespół zmniejszył jego poziom u myszy i w hodowlach ludzkich komórek nerkowych. W dobrze opisanym modelu myszy, w którym jeden moczowód jest podwiązywany, powodując długotrwałą niedrożność, obniżenie tego RNA za pomocą ukierunkowanego dostarczania wirusowego złagodziło wiele cech bliznowacenia: kanaliki zachowały lepszą integralność, międzykomórkowo występowało mniej kolagenu i innych białek bliznowatych, a markery funkcji nerek we krwi uległy poprawie. W hodowlach ludzkich komórek nerkowych zmniejszenie P4HA2-AS1 osłabiło również reakcję na silny sygnał bliznowacenia, TGF-β, prowadząc do mniejszej produkcji fibryonektyny, kolagenu i innych czynników pro-fibrotycznych. Te eksperymenty wykazały, że to RNA nie jest tylko markerem uszkodzenia, lecz aktywnie napędza proces bliznowacenia.
Autofagia: od sprzątania do szkody
Naukowcy następnie zapytali, jak to RNA wywołuje szkodę. Dane dotyczące ekspresji genów i obrazowania wskazały na autofagię — wewnętrzny system recyklingu komórkowego, który rozkłada zużyte białka i organelle. W normalnych warunkach autofagia jest zdrowym procesem porządkowym, ale gdy jest nadmiernie aktywowana przez długi czas, może popychać uszkodzone nerki ku nieprawidłowej naprawie i bliznowaceniu. W zestresowanych komórkach nerkowych P4HA2-AS1 zwiększało przepływ materiału przez autofagię, prowadząc do nagromadzenia pęcherzyków recyklingowych. Gdy RNA zostało zablokowane, ta nadaktywna „recyklerka” wracała bliżej normy, zarówno w komórkach, jak i w nerkach myszy z niedrożnością. Myszy pozbawione ULK1, kluczowego enzymu inicjującego autofagię, również były chronione przed bliznowaceniem, a w tych zwierzętach nadmierna ekspresja P4HA2-AS1 nie mogła już pogorszyć uszkodzenia, co jednoznacznie powiązało efekt RNA z tą ścieżką.
Trójelementowy łańcuch molekularny
Badając dalej, zespół zastosował biochemiczne metody „łowienia”, by zidentyfikować białka fizycznie wiążące się z P4HA2-AS1. Jedno wyróżniało się szczególnie: TRIM32, enzym, który znakuję inne białka małymi „flagami” zwanymi ubikwityną. RNA wiąże się z TRIM32 i chroni je przed degradacją, podnosząc jego poziomy w komórkach nerkowych. Stabilizowany TRIM32 z kolei przyłącza specyficzny typ łańcucha ubikwitynowego do ULK1. Zamiast kierować ULK1 do degradacji, ten łańcuch działa jak wzmocnienie, zwiększając zdolność ULK1 do uruchamiania autofagii. Gdy naukowcy usunęli TRIM32 u myszy lub wyciszyli je w komórkach nerkowych, zarówno bliznowacenie, jak i nadmierna autofagia uległy redukcji. Ponowne wprowadzenie TRIM32 do komórek, w których P4HA2-AS1 zostało zablokowane, częściowo przywróciło reakcję bliznowacenia, pokazując, że ten enzym jest kluczowym środkowym ogniwem w łańcuchu. 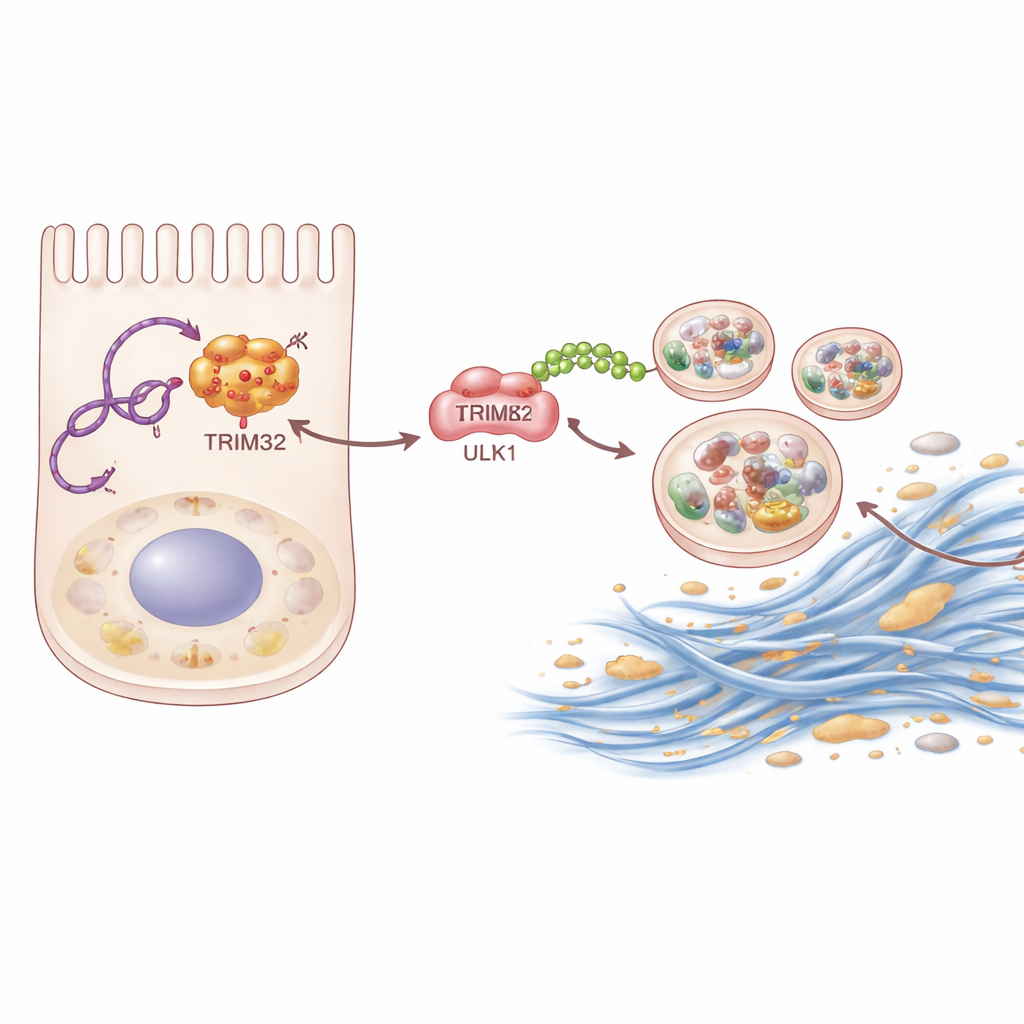
Nowe drogi ku miększym nerkom
Podsumowując, praca ujawnia wcześniej nieznaną drogę molekularną łączącą długie niekodujące RNA, znakowanie białek i komórkowy recykling z narastaniem tkanki bliznowatej nerek. W uszkodzonych nerkach P4HA2-AS1 wzrasta, stabilizuje TRIM32, wzmacnia ULK1 i napędza autofagię poza jej korzystny zakres, ostatecznie sprzyjając akumulacji białek włóknistych i utracie funkcji. Dla osób niezajmujących się specjalistycznie tematem najważniejsze jest, że bliznowacenie nerek nie jest nieuchronną czarną skrzynką: jest napędzane przez rozpoznawalne przełączniki, które mogą być potencjalnie modyfikowane farmakologicznie. Celowanie w oś P4HA2-AS1–TRIM32–ULK1 — obniżenie poziomu „rzucającego się w oczy” RNA, okiełznanie TRIM32 lub dopracowanie aktywności ULK1 — mogłoby pewnego dnia dać nowe terapie spowalniające lub zapobiegające postępowi przewlekłej choroby nerek.
Cytowanie: Pan, Z., Xiao, F., Hu, W. et al. LncRNA P4HA2-AS1 drives renal interstitial fibrosis via trim32-mediated k63 ubiquitination of ULK1 and autophagic dysregulation. Commun Biol 9, 339 (2026). https://doi.org/10.1038/s42003-026-09618-7
Słowa kluczowe: przewlekła choroba nerek, włóknienie nerek, autofagia, długie niekodujące RNA, kanaliki nerkowe