Clear Sky Science · pl
Inhibitory odwrotnej transkryptazy umożliwiają powstanie płodnych spermatydów z płodowych jąder myszy in vitro
Przekształcanie wczesnych komórek germinalnych w działające plemniki
Leczenie niepłodności i badania podstawowe zależą od zrozumienia, jak niedojrzałe komórki germinalne w jądrach przekształcają się w plemniki. To badanie pokazuje, że możliwe jest obecnie nakłonienie bardzo wczesnych płodowych jąder myszy, pobranych tuż po określeniu płci zarodka, do dokończenia tej przemiany całkowicie w naczyniu. Poprzez staranne dostrojenie środowiska chemicznego i poziomu tlenu, naukowcy nie tylko wytworzyli dojrzałe komórko-podobne plemniki, lecz także wykorzystali je do stworzenia zdrowego, płodnego potomstwa.
Dlaczego wczesny rozwój jądra trudno odtworzyć
Hodowla plemników poza organizmem była wcześniej osiągana przy użyciu tkanki jądra z noworodków lub starszych myszy, lecz wydajność była niska, a próby z znacznie wcześniejszą tkanką płodową w dużej mierze zawodziły. Na tym wczesnym etapie jądro nadal formuje swoją wewnętrzną architekturę, a komórki germinalne przechodzą rozległe zmiany w organizacji i znakowaniu DNA. Odtworzenie tej skomplikowanej choreografii w naczyniu jest trudne, i wcześniejsze hodowle rzadko postępowały dalej niż początkowe etapy, gdy zaczynano od jąder zebranych około 12,5 dnia zarodkowego, niedługo po ustaleniu płci zarodka.
Pozyskanie leków przeciwwirusowych, by chronić rozwijające się komórki
Zespół skupił się na ukrytej przeszkodzie: ruchomych elementach DNA zwanych retrotranspozonami, które potrafią kopiować się i wstawiać w nowe miejsca w genomie. W normalnych jądrach w organizmie te elementy są ściśle kontrolowane, zwłaszcza w komórkach germinalnych. W hodowli jednak autorzy zaobserwowali znacznie większą aktywność retrotranspozonów, podczas gdy własne geny obronne komórek były słabsze. Ta nierównowaga korelowała ze słabym rozwojem plemników. Ponieważ retrotranspozony wykorzystują enzym odwrotnej transkryptazy, podobny do tego u niektórych wirusów, badacze przetestowali kilka leków zaprojektowanych pierwotnie jako inhibitory odwrotnej transkryptazy. Konkretna mieszanka trzech leków, nazwana AEC, w przybliżeniu podwoiła odsetek komórek spermatogenicznych i ponad trzykrotnie zwiększyła udział haploidalnych, przypominających plemniki komórek w hodowlach jąder noworodków w porównaniu z nieleczonymi kontrolami.
Z maleńkich płodowych jąder do funkcjonalnych plemników
Uzbrojeni w ten koktajl leków, naukowcy zwrócili się ku jądrom płodowym. W tkance pobranej nieco przed urodzeniem inhibitory zwiększyły pojawienie się zaawansowanych spermatydów. Co bardziej uderzające, gdy hodowali jądra z zarodków w dniu 12,5 — stadium, w którym wcześniej nie wykazano pełnej spermatogenezy in vitro — mogli teraz uzyskać okrągłe i wydłużone spermatydy. Największe korzyści odniesiono, gdy połączyli mieszankę inhibitorów z niskotlenową atmosferą, która lepiej naśladuje warunki panujące w rozwijającym się organizmie. W tych warunkach hipoksycznych około jednej trzeciej powierzchni tkanki wykazywało markery zaawansowanego rozwoju komórek germinalnych, a z hodowli można było odzyskać plemniki z ogonkami.
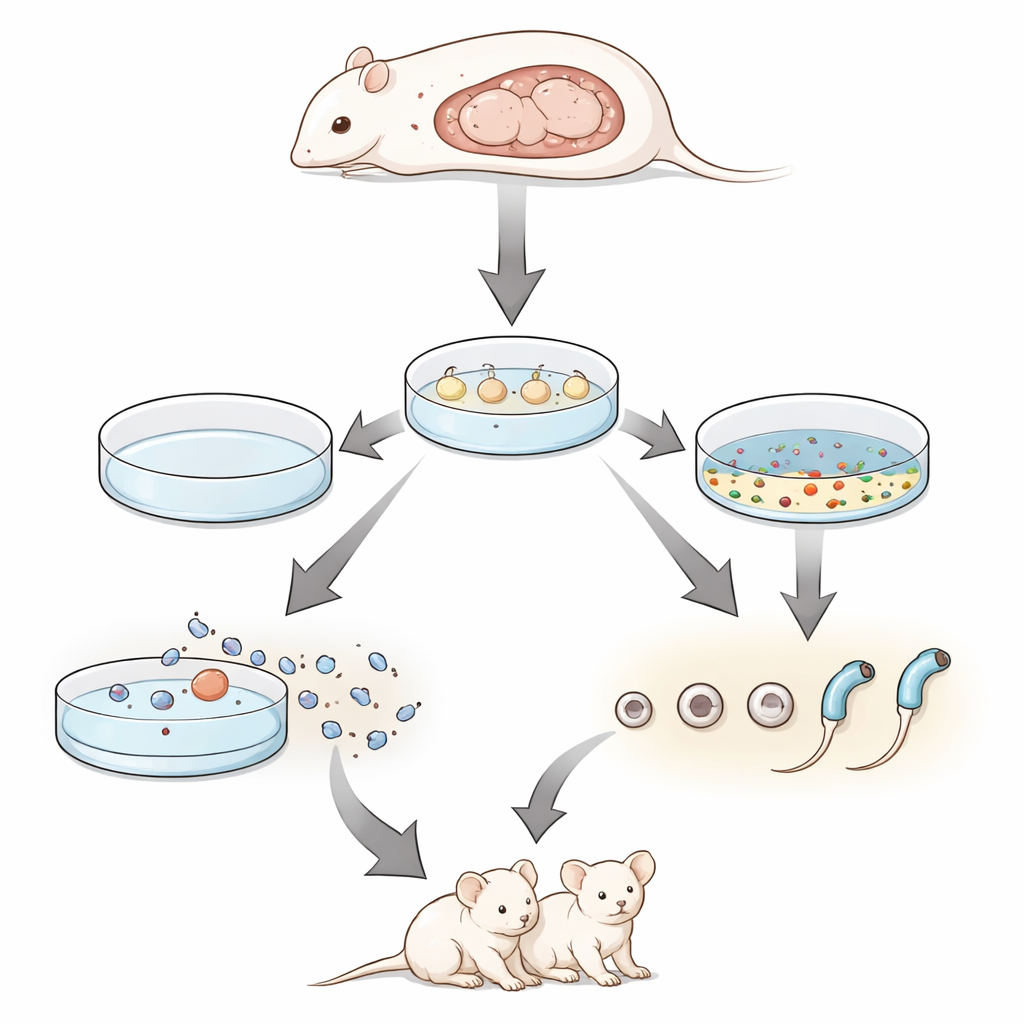
Testowanie, czy laboratoryjne spermatydy naprawdę działają
Aby sprawdzić, czy te komórki pochodzące z hodowli są rzeczywiście funkcjonalne, zespół zastosował technikę wstrzyknięcia okrągłych spermatyd (round spermatid injection). Wyizolowali okrągłe spermatydy z hodowanych płodowych jąder i wstrzyknięli je do oocytów mysich, które zostały delikatnie aktywowane. Powstałe zarodki przeniesiono do matek zastępczych. Zaledwie z dwóch fragmentów hodowanych jąder procedura dała wiele żywych młodych, z których wiele nosiło fluorescencyjny gen znacznikowy potwierdzający ich hodowlaną proweniencję. Kiedy te osobniki pierwszego pokolenia zostały dopuszczone do rozrodu, wydały na świat mioty o normalnej wielkości zdrowego potomstwa drugiego pokolenia, udowadniając, że spermatydy pozyskane w laboratorium wspierały nie tylko rozwój do narodzin, lecz także pełną płodność.
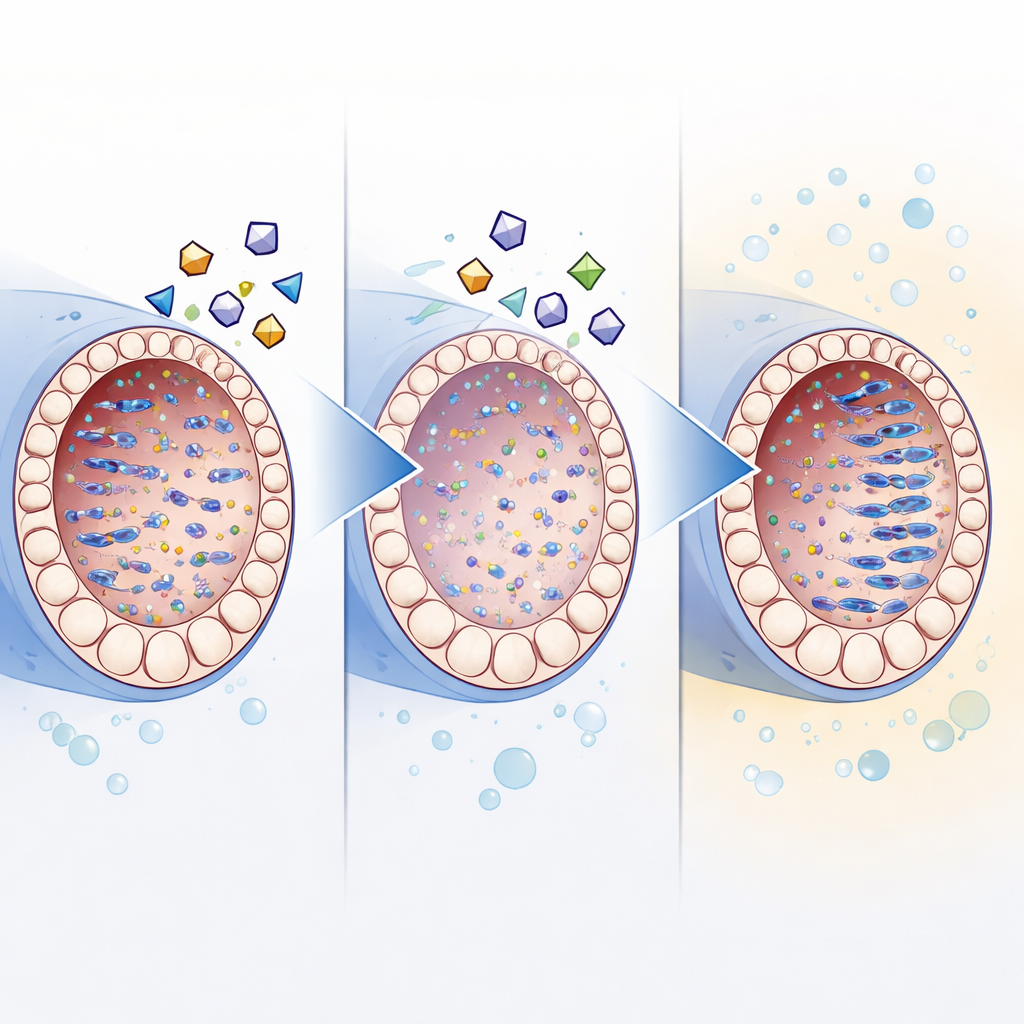
Jak blokowanie ruchomego DNA może umożliwić przyszłe terapie
Dalsze eksperymenty wspierały hipotezę, że inhibitory odwrotnej transkryptazy pomagają głównie przez powstrzymywanie ruchomego DNA. W porównaniu z jądrami w ciele w tym samym wieku, hodowane jądra wykazywały wyższe poziomy białek retrotranspozonów i dodatkowe kopie ich DNA, a także zmniejszoną ekspresję naturalnego mechanizmu wyciszania komórek. Dodanie koktajlu inhibitorów zmniejszało to nagromadzenie, jednocześnie poprawiając dojrzewanie komórek germinalnych. Chociaż leki nieznacznie spowalniały ogólny wzrost tkanki, próby skompensowania tego przy pomocy dodatków na bazie surowicy nie poprawiły produkcji plemników, co sugeruje, że wzrost i prawidłowa różnicowanie muszą być starannie wyważone.
Co to znaczy dla nauk o rozrodzie
Praca ta pokazuje, że nawet bardzo niedojrzałe płodowe jądra zawierają już wszystkie składniki potrzebne do zbudowania działającej „fabryki” plemników, pod warunkiem że środowisko chroni ich genomy i naśladuje kluczowe cechy warunków w macicy. Poprzez połączenie leków o działaniu przeciwwirusowym z niskim stężeniem tlenu, badacze stworzyli system hodowli, który odtwarza pełną spermatogenezę z jednego z najwcześniejszych przebadanych etapów i daje potomstwo, które rośnie i rozmnaża się normalnie. Choć badanie dotyczy myszy i jest dalekie od zastosowań klinicznych, otwiera potężne okno na najwcześniejsze etapy rozwoju męskich komórek germinalnych i dostarcza wskazówek, które kiedyś mogą pomóc zachować lub przywrócić płodność u pacjentów, których komórki rozrodcze zostały uszkodzone we wczesnym okresie życia.
Cytowanie: Nishida, M., Ono-Sunagare, Y., Kato, S. et al. Reverse transcriptase inhibitors enable the generation of fertile spermatids from fetal mouse testes in vitro. Commun Biol 9, 329 (2026). https://doi.org/10.1038/s42003-026-09613-y
Słowa kluczowe: in vitro spermatogeneza, hodowla płodowych jąder, inhibitory odwrotnej transkryptazy, retrotranspozony, męska płodność