Clear Sky Science · pl
Otyłość upośledza spermatogenezę poprzez ferroptozę komórek Leydiga wywołaną wątrobowymi egzosomami zawierającymi miR-122-5p
Dlaczego masa ciała i płodność są powiązane
Otyłość najczęściej omawia się w kontekście chorób serca i cukrzycy, ale może też cicho osłabiać męską płodność. Badanie na myszach ujawnia zaskakujący mechanizm, w którym tłusta dieta obniża poziom testosteronu i uszkadza produkcję plemników: wątroba wysyła do krwi maleńkie „bańki z wiadomościami”, które uruchamiają specyficzny rodzaj śmierci komórkowej w komórkach produkujących hormony w jądrach. Zrozumienie tej ukrytej komunikacji wątroba–jądro może pomóc wyjaśnić, dlaczego mężczyźni z nadwagą często borykają się z niskim poziomem testosteronu i niepłodnością oraz wskazać nowe cele terapeutyczne.
Ukryta poczta między narządami
Nasze narządy nieustannie ze sobą rozmawiają za pomocą hormonów i innych chemicznych przekaźników. Jedną z form tej komunikacji są egzosomy — nanometrowe pęcherzyki uwalniane przez komórki, które niosą lipidy, białka i materiał genetyczny. Badacze zaczęli od myszy karmionych dietą normalną lub wysokotłuszczową, która wywołała otyłość, insulinooporność i zaburzenia kontroli glikemii. U otyłych myszy jądra były mniejsze i mniej aktywne: spadły liczba plemników, poziomy testosteronu oraz rozmiar i liczba kanalika plemnikotwórczego. Po przeanalizowaniu kluczowych znaczników komórkowych w jądrach stwierdzono mniej komórek Leydiga produkujących testosteron oraz mniej komórek plemnikowych w stanach wczesnym i późnym, co potwierdza, że cała „taśma produkcyjna” plemników była upośledzona. 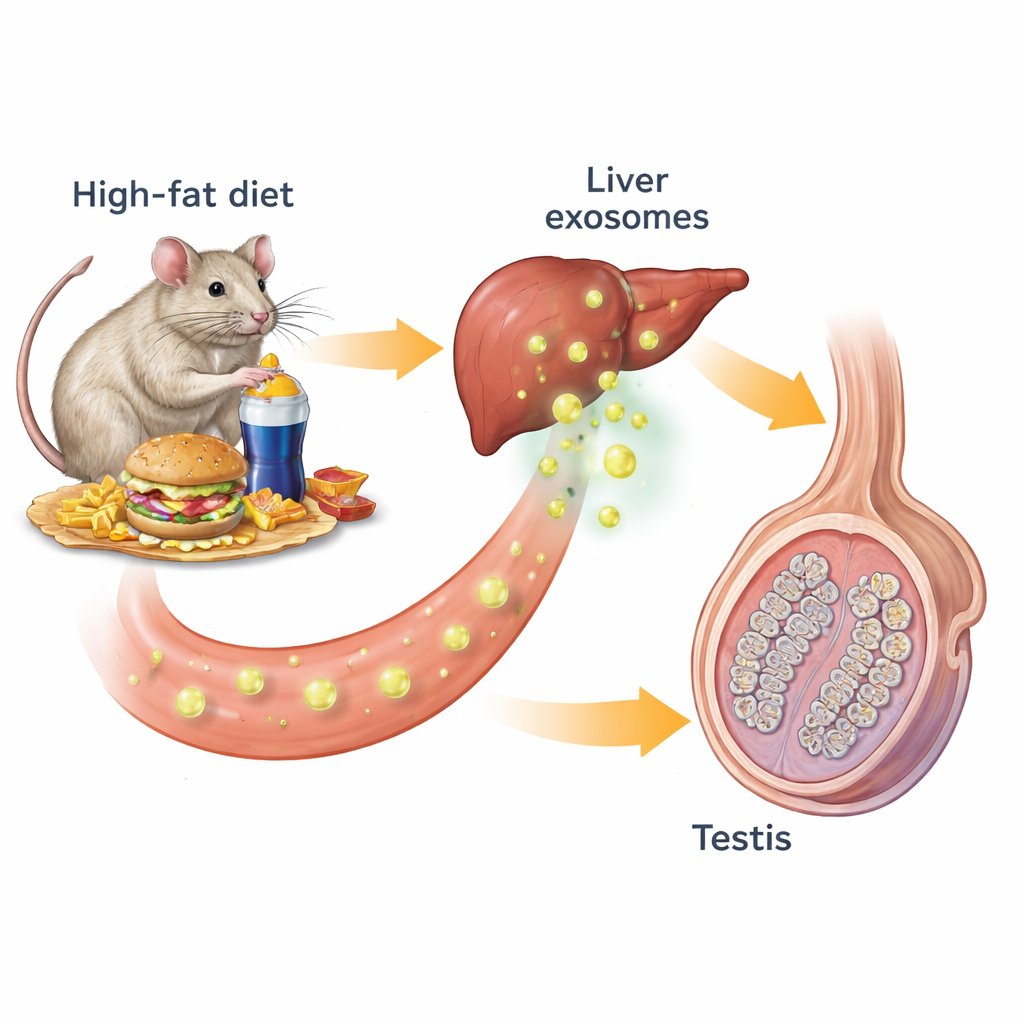
Egzosomy rozprzestrzeniają szkody
Aby sprawdzić, czy krążące egzosomy przyczyniają się do tych uszkodzeń, naukowcy oczyszczali egzosomy z krwi myszy otyłych i szczupłych. Wstrzyknięcie egzosomów pochodzących od myszy otyłych do zdrowych, szczupłych zwierząt wystarczyło, by odtworzyć wiele problemów: biorcy rozwinęli cechy zaburzeń metabolicznych, ich poziom testosteronu spadł, a liczba plemników i struktura jąder pogorszyły się. Zablokowanie wydzielania egzosomów u myszy otyłych lekiem GW4869 w dużej mierze odwróciło te zmiany, przywracając liczbę plemników, poziom testosteronu i normalną architekturę jąder. Wyniki te pokazują, że egzosomy we krwi nie są tylko biernymi obserwatorami; aktywnie przenoszą szkodliwe sygnały z otyłości do układu rozrodczego.
Toksyczny rodzaj śmierci komórki
Zespół następnie badał, co dokładnie egzosomy robią komórkom Leydiga. Skoncentrowali się na ferroptozie — formie śmierci komórkowej zależnej od żelaza, charakteryzującej się akumulacją żelaza, uszkodzeniem oksydacyjnym lipidów i uszkodzonymi mitochondriami — „elektrowniami” komórki. U myszy otyłych oraz u zdrowych myszy otrzymujących egzosomy z myszy otyłych w jądrach zaobserwowano wyższe poziomy żelaza i malondialdehydu, produktu ubocznego uszkodzenia lipidów, a także wyraźne uszkodzenia mitochondriów w mikroskopii elektronowej. Leczenie myszy otyłych związkiem blokującym ferroptozę, Ferrostatyną-1, chroniło komórki Leydiga, zwiększało poziom testosteronu i liczbę plemników oraz poprawiało zdrowie mitochondriów. W hodowli komórkowej ten sam lek chronił izolowane komórki Leydiga przed śmiercią i stresem oksydacyjnym wywołanym egzosomami pochodzącymi od zwierząt otyłych. Razem te eksperymenty wskazują ferroptozę jako kluczowe ogniwo łączące otyłość z upośledzoną produkcją testosteronu.
Wiadomość z wątroby i przełącznik SCD2
Aby namierzyć przekaz wewnątrz egzosomów, badacze zsekwencjonowali ich małą frakcję RNA i stwierdzili, że specyficzne mikroRNA, miR-122-5p, było silnie podwyższone w egzosomach myszy otyłych. To mikroRNA było szczególnie obfite w wątrobie i w egzosomach pochodzenia wątrobowego, a te wątrobowe egzosomy można było śledzić wędrujące do jąder. Gdy poziomy miR-122-5p zostały eksperymentalnie obniżone w egzosomach, komórki Leydiga były mniej podatne na ferroptozę, a produkcja testosteronu poprawiła się, chociaż zwierzęta pozostawały metabolicznie niezdrowe. Dalsze badania wykazały, że miR-122-5p bezpośrednio wycisza gen Scd2, który pomaga przekształcać niektóre tłuszcze w formy chroniące komórki przed uszkodzeniem oksydacyjnym. Redukcja Scd2 w komórkach Leydiga zwiększała ich podatność na ferroptozę i obniżała poziom testosteronu, podczas gdy zwiększenie ekspresji Scd2 u myszy otyłych częściowo przywróciło poziomy hormonów, produkcję plemników i strukturę mitochondriów. 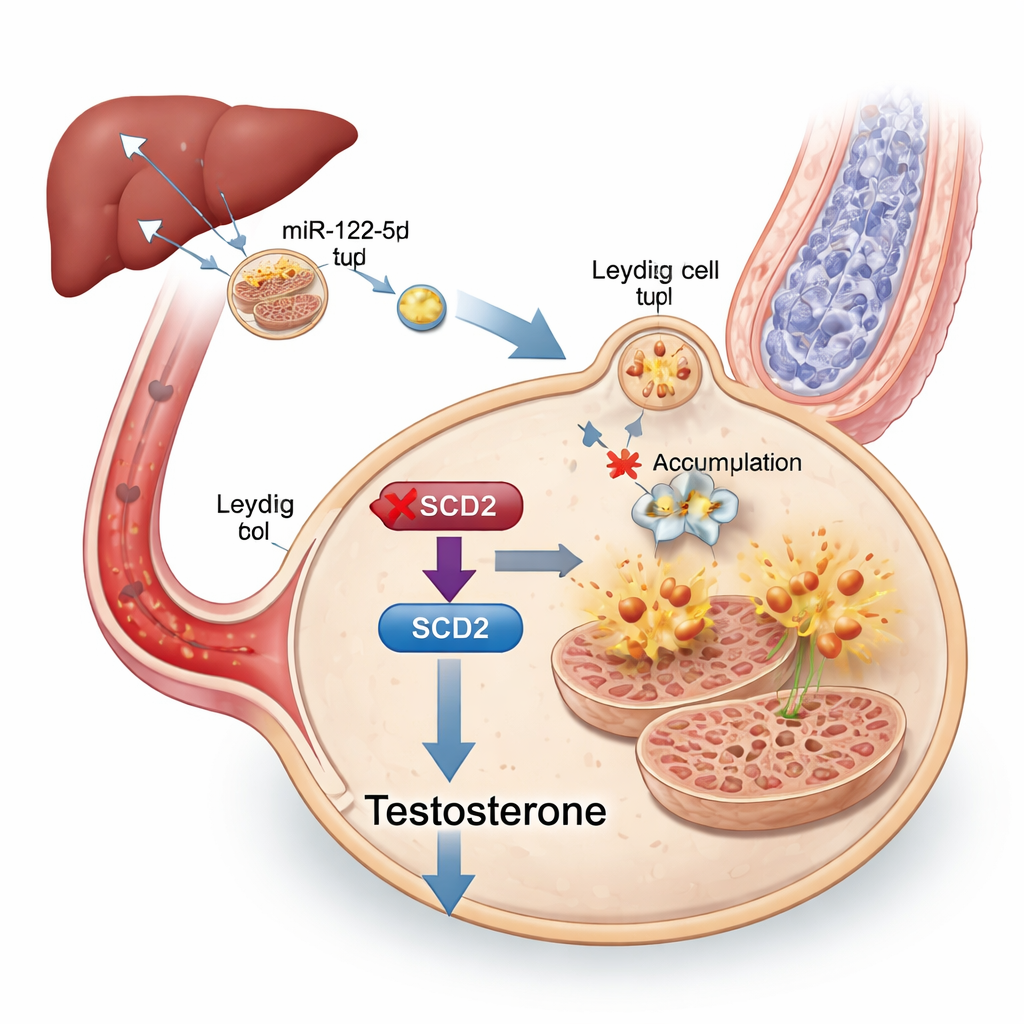
Co to oznacza dla zdrowia ludzi
Mówiąc wprost, praca ta pokazuje, że dieta wysokotłuszczowa może spowodować, iż wątroba załaduje egzosomy nadmiarem miR-122-5p. Te egzosomy przemieszczają się przez krew do jąder, gdzie mikroRNA wyłącza przełącznik Scd2 odpowiedzialny za „obrabianie” tłuszczów w komórkach Leydiga. Bez Scd2 komórki te gromadzą żelazozależne uszkodzenia oksydacyjne, przechodzą ferroptozę, produkują mniej testosteronu i ostatecznie wspierają mniej zdrowych plemników. Chociaż badania wykonano na myszach i wymagają potwierdzenia u ludzi, identyfikuje to wątrobowe egzosomy, miR-122-5p, ferroptozę i Scd2 jako obiecujące markery i potencjalne cele lekowe w leczeniu niepłodności męskiej związanej z otyłością — oraz podkreśla kolejny powód, dla którego długotrwałe diety wysokotłuszczowe mogą cicho niszczyć zdrowie rozrodcze.
Cytowanie: Wang, N., Zhang, B., Chen, T. et al. Obesity impairs spermatogenesis via Leydig cell ferroptosis induced by liver-derived exosomal miR-122-5p. Commun Biol 9, 318 (2026). https://doi.org/10.1038/s42003-026-09612-z
Słowa kluczowe: otyłość a płodność mężczyzn, testosteron, egzosomy, komórki Leydiga, ferroptoza