Clear Sky Science · pl
Dwufunkcyjna etykieta białkowa umożliwia rozpuszczalną ekspresję i zależną od wapnia oczyszczanie fragmentów przeciwciał jednoniciowych
Uproszczenie wytwarzania silnych przeciwciał
Współczesne leki coraz częściej opierają się na fragmentach przeciwciał — małych, precyzyjnych „kierowanych pociskach”, które potrafią rozpoznać komórki nowotworowe, ogniska zapalne lub cząsteczki wywołujące chorobę. Te obiecujące terapie są jednak zadziwiająco trudne w produkcji: w bakteriach mają tendencję do tworzenia grudek, nieprawidłowego fałdowania i oporu wobec standardowych metod oczyszczania. W pracy opisano nowy dodatek białkowy, nazwany etykietą CSQ, który jednocześnie rozwiązuje oba problemy, ułatwiając w prosty i niskokosztowy sposób produkcję i oczyszczanie tych fragmentów.
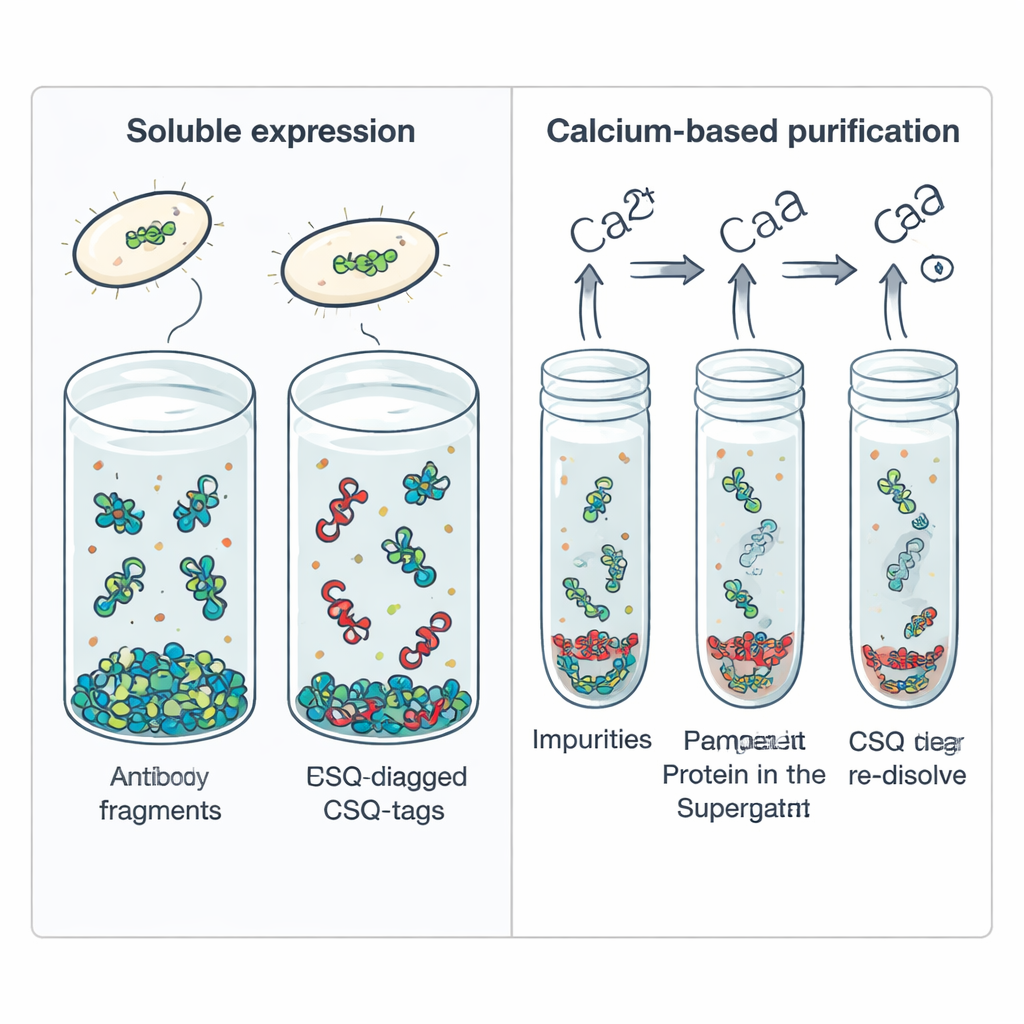
Dlaczego pomniejszone przeciwciała mają znaczenie
Pełnowymiarowe przeciwciała zrewolucjonizowały leczenie raka, chorób autoimmunologicznych i schorzeń oczu, ale ich duży rozmiar i złożona struktura mają też wady. Mogą długo zalegać w organizmie, słabo przenikać do guzów czy tkanek oraz są drogie w produkcji. Jednoniciowe fragmenty zmienne, czyli scFv, zachowują jedynie „działającą” część przeciwciała — fragment rozpoznający cel — połączony w jedną nić. Te kompaktowe cząsteczki lepiej wnikają w tkanki i można je zaprojektować na potrzeby zaawansowanych terapii i testów diagnostycznych. Jednak w powszechnie stosowanych bakteriach takich jak Escherichia coli wiele scFv tworzy nierozpuszczalne grudki zwane ciałkami inkluzyjnymi, a uniwersalnej, prostej metody ich oczyszczania brak.
Dwufunkcyjna pomocnicza etykieta
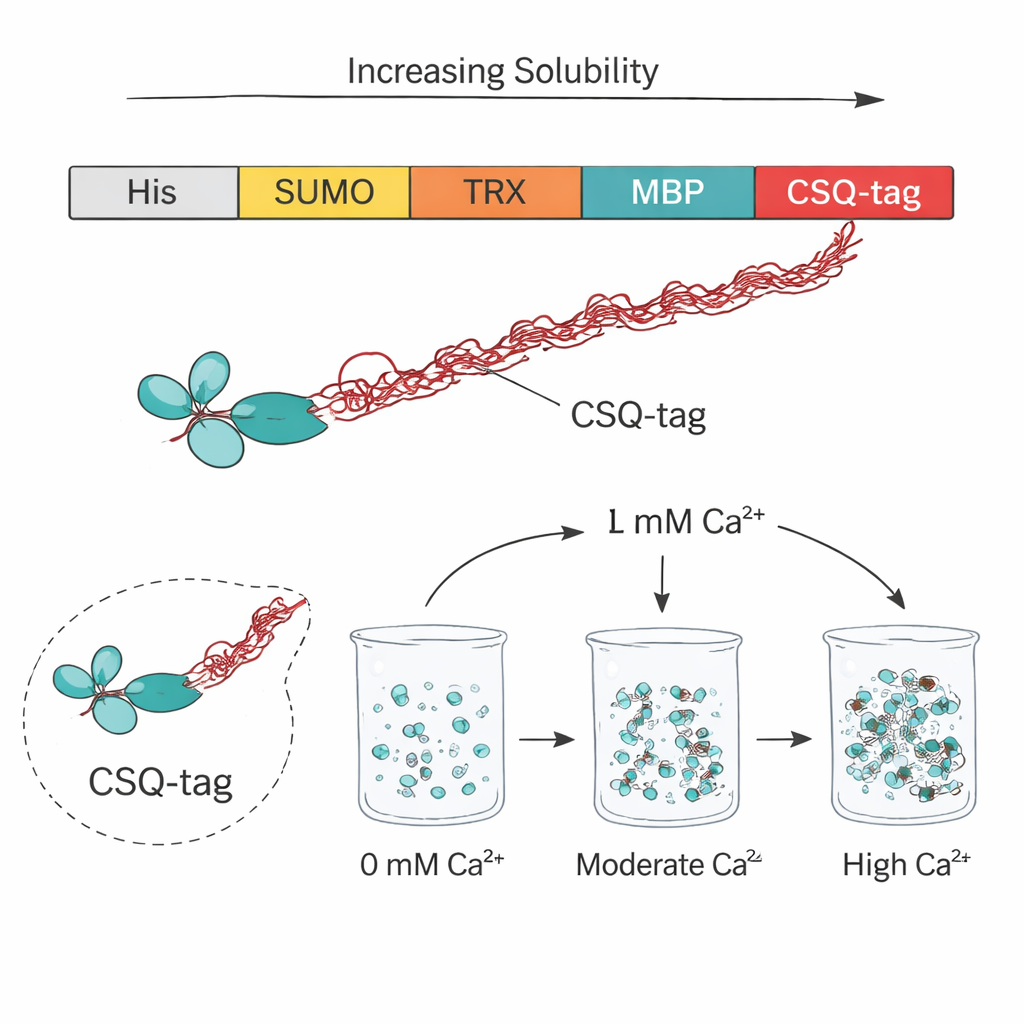
Naukowcy sięgnęli po calsequestrinę, naturalne białko magazynujące wapń w komórkach mięśniowych, aby zaprojektować pomocniczą etykietę nazwaną CSQ-tag. Etykieta ta jest wyjątkowo kwaśna i wysoce elastyczna, zawiera długie, nieuporządkowane regiony, które zachowują się jak „entropowe szczeciny” odpychające przestrzeń wokół dołączonego białka. Kiedy przypięto ją do czterech różnych terapeutycznych scFv, które zwykle agregują, CSQ-tag dramatycznie zwiększył ilość pozostającą w stanie rozpuszczonym w standardowych komórkach E. coli. Podczas gdy te same scFv z prostą etykietą His były niemal całkowicie nierozpuszczalne, wersje z CSQ osiągnęły średnią rozpuszczalność około 84 procent — nawet w szczepie bakteryjnym, który zwykle stwarza chemicznie trudne warunki dla prawidłowego fałdowania.
Pokonując ugruntowane technologie etykiet
Aby ocenić, jak CSQ-tag wypadł na tle popularnych etykiet białkowych, zespół porównał go z SUMO, tioredoksyną, GST i MBP, powszechnie używanymi do doprowadzania problematycznych białek do stanu rozpuszczalnego. W tym bezpośrednim teście z fragmentem przeciwciała przeciw VEGF (będącym podstawą leku okulistycznego brolucizumabu) tylko MBP i CSQ znacząco poprawiły rozpuszczalność, a CSQ wyraźnie okazał się lepszy. W czterech różnych scFv CSQ zwiększył produkcję rozpuszczalną około 1,8-krotnie więcej niż MBP, który długo uważano za jedną z najlepszych opcji. Dalsze eksperymenty wykazały, że najbardziej kwaśna i nieuporządkowana część calsequestryny, znana jako domena 3, była kluczowa dla tego efektu: jej usunięcie ostro zmniejszało rozpuszczalność, podkreślając, jak negatywny ładunek i strukturalna luźność etykiety pomagają zapobiegać sklejaniu partnerów białkowych.
Użycie wapnia jako prostego przełącznika oczyszczania
Oprócz ułatwiania rozpuszczalności scFv, CSQ-tag oferuje wbudowany trik oczyszczający. Calsequestrina naturalnie agreguje po związaniu wapnia i rozpada się ponownie po jego usunięciu. Autorzy wykorzystali to zjawisko, dodając wapń do ekstraktu komórkowego zawierającego scFv z CSQ-tag, co spowodowało agregację znakowanych białek fuzyjnych, podczas gdy większość bakterii niesprzężonych pozostała w roztworze. Szybkie odwirowanie osadziło białko z etykietą CSQ; dodanie chelatującego wapń EDTA ponownie je rozpuściło z wysoką czystością, powyżej 95 procent, bez użycia drogich żywic chromatograficznych. Ta fazowa przemiana napędzana wapniem mogła być powtarzana bez uszkadzania białka, co czyni ją atrakcyjną dla produkcji na dużą skalę.
Utrzymanie aktywności leku
Dla każdego leku zwiększenie produkcji ma znaczenie tylko wtedy, gdy produkt końcowy nadal działa. Po zastosowaniu standardnej enzymatycznej proteazy do odcięcia CSQ-tagu i końcowego etapu polerowania zespół przetestował wolne scFv przeciw VEGF. Wiązanie z celem miało siłę zasadniczo identyczną z zatwierdzonym lekiem brolucizumabem, a szczegółowe analizy chemiczne potwierdziły prawidłowe wiązania wewnętrzne i brak szkodliwych agregatów. Drugi, szczególnie problematyczny scFv skierowany przeciw receptorowi CD3 wykazał podobne zachowanie aktywności. Ogólne wydajności procesu z użyciem CSQ-tagu były wielokrotnie wyższe niż zgłaszane dla tradycyjnych metod ponownego fałdowania, przy użyciu prostszego sprzętu i tańszych reagentów.
Co to może oznaczać dla przyszłych terapii
Łącząc poprawioną rozpuszczalność i prosty uchwyt do oczyszczania w jednej etykiecie, system CSQ rozwiązuje dwa długoletnie wąskie gardła w produkcji fragmentów przeciwciał. Umożliwia twórcom leków stosowanie szybko rosnących, niedrogich szczepów E. coli, przy jednoczesnym uzyskaniu wysokiej jakości scFv, które zachowują swoją siłę wiązania. Chociaż nadal wymagana jest optymalizacja, szczególnie by zredukować straty po usunięciu etykiety, ta związana z wapniem, regulowana etykieta mogłaby usprawnić produkcję nie tylko fragmentów przeciwciał, lecz także innych wrażliwych białek terapeutycznych. Dla pacjentów może to w efekcie oznaczać szerszy wybór ukierunkowanych leków biologicznych produkowanych efektywniej i taniej.
Cytowanie: Lee, J., Park, H., Jeong, S. et al. Two-in-one protein tag enables the soluble expression and calcium-dependent purification of single-chain antibody fragments. Commun Biol 9, 326 (2026). https://doi.org/10.1038/s42003-026-09611-0
Słowa kluczowe: fragmenty przeciwciał jednoniciowych, ekspresja białka, etykieta calsequestryny, oczyszczanie zależne od wapnia, przeciwciała terapeutyczne