Clear Sky Science · pl
Demetylaza histonowa KDM7A negatywnie reguluje polaryzację makrofagów sprzyjających włóknieniu i postęp włóknienia płuc
Dlaczego bliznowacenie płuc ma znaczenie dla wszystkich
Gdy w płucach pojawiają się uporczywe blizny, oddychanie staje się codzienną walką. Ten stan, znany jako włóknienie płuc, dotyka miliony osób i na razie nie ma na niego lekarstwa — istnieją jedynie leki spowalniające postęp choroby. W tym badaniu naukowcy odkryli dotąd ukryty molekularny „hamulec” w komórkach odpornościowych zwanych makrofagami, który pomaga powstrzymywać bliznowacenie płuc. Zrozumienie tego mechanizmu może otworzyć drogę do nowych terapii nie tylko w przypadku włóknienia płuc, lecz także potencjalnie dla innych chorób, w których szkodliwe blizny i niekontrolowane zapalenie idą w parze.
Opowieść o zmiennokształtnych komórkach odpornościowych
Makrofagi to komórki obronne będące na pierwszej linii: patrolują tkanki, usuwają resztki i wspomagają naprawę uszkodzeń. Są jednak także zmiennokształtne: w pewnych sytuacjach stają się prozapalnymi „żołnierzami”, a w innych przechodzą w tryb gojenia ran, co może prowadzić do powstawania blizn. Szczególny typ promujący bliznowacenie, zwany makrofagami profibrotycznymi (Fib-Mac), jest silnie powiązany z włóknieniem płuc. Komórki te produkują czynniki aktywujące fibroblasty, które następnie odkładają nadmierne ilości kolagenu i innych składników macierzy, stopniowo usztywniając płuca. Autorzy chcieli dowiedzieć się, jak wewnętrzne „ustawienia” genetyczne w makrofagach decydują, czy stają się one niebezpiecznymi Fib-Mac, czy pozostają w bardziej zrównoważonych, ochronnych stanach.
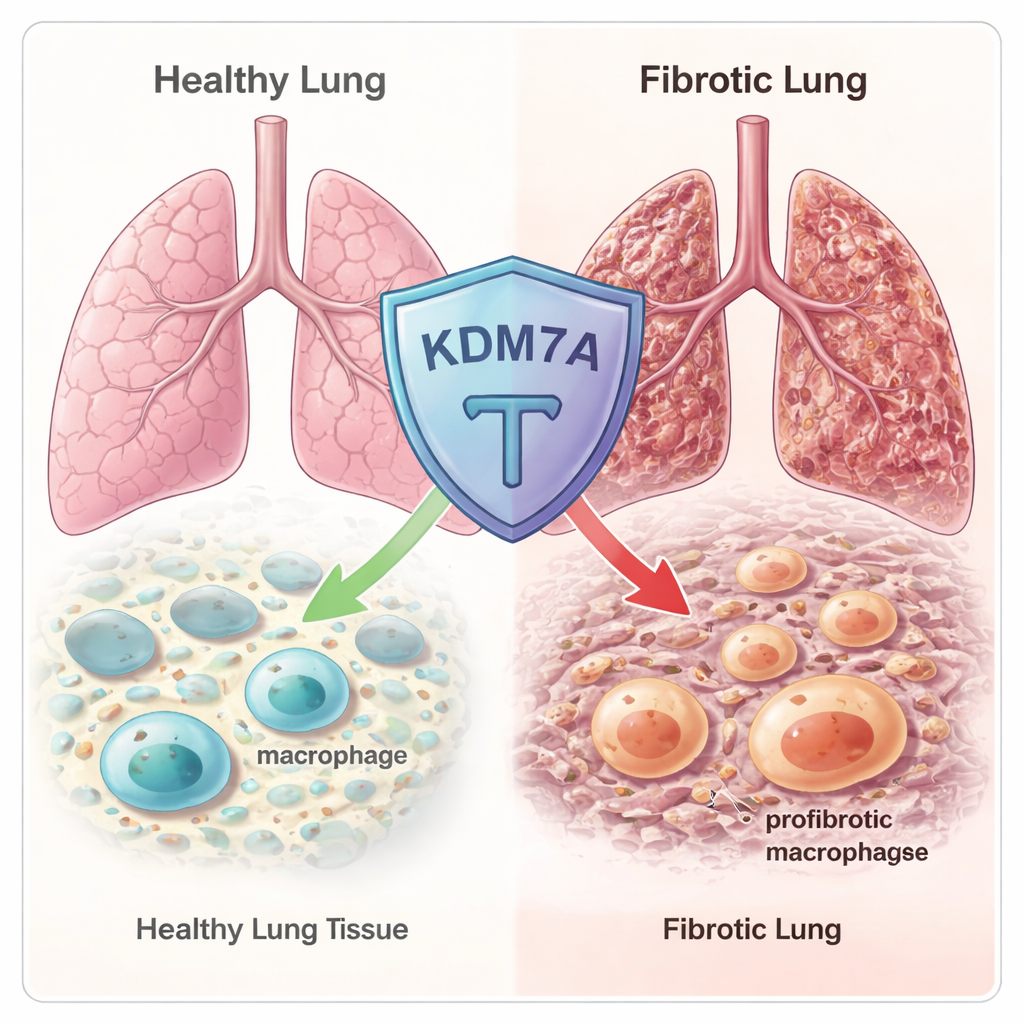
Epigenetyczny hamulec ukryty w genomie
Zespół rozpoczął od przesiewu setek znanych regulatorów epigenetycznych — białek, które precyzują, jak ciasno upakowane jest DNA i które geny są włączone lub wyłączone. Wykorzystując sekwencjonowanie RNA w makrofagach ludzkich i mysich, stwierdzili, że enzym o nazwie KDM7A był silnie aktywowany, gdy makrofagi były skłaniane do stanu profibrotycznego, związanego z gojeniem ran. KDM7A to „demetylaza histonowa”: usuwa określone chemiczne znaczniki z białek histonowych, wokół których owinięte jest DNA. Ten wzorzec sugerował, że KDM7A może działać jako wbudowany hamulec sprzężenia zwrotnego, aktywowany precyzyjnie wtedy, gdy makrofagi zaczynają zbaczać w kierunku tożsamości sprzyjającej bliznowaceniu.
Aby to przetestować, badacze użyli myszy pozbawionych genu Kdm7a i wywołali uszkodzenie płuc za pomocą leku chemioterapeutycznego bleomycyny, co stanowi standardowy model włóknienia płuc. Wkrótce po urazie tkanka płuc u zwierząt kontrolnych i pozbawionych Kdm7a wyglądała podobnie. Jednak po trzech tygodniach myszy bez Kdm7a wykazywały znacznie bardziej rozległe bliznowacenie, zapadnięcie pęcherzyków płucnych i wyższe „wyniki Ashcrofta” służące do kwantyfikacji włóknienia. Geny związane z produkcją kolagenu i innymi szlakami fibrogennymi były bardziej aktywne u tych myszy typu knockout, co potwierdza, że utrata Kdm7a zwiększa podatność płuc na długotrwałe, szkodliwe bliznowacenie.
Jak KDM7A odciąga makrofagi od losu sprzyjającego bliznom
Stosując sekwencjonowanie RNA pojedynczych komórek, autorzy przyjrzeli się pojedynczym komórkom płuc po urazie. Odkryli, że przy braku Kdm7a w tkance podporowej płuc znacząco rozszerzyła się szczególna podpopulacja makrofagów i przyjęła silny odcisk Fib-Mac, wyrażając geny takie jak Arg1, Spp1 i Trem2. Dalsze eksperymenty na hodowlach makrofagów wykazały, że usunięcie Kdm7a zwiększa ekspresję markerów Fib-Mac i przestawia metabolizm komórek na szlaki wspierające produkcję kolagenu oraz utrzymaną aktywację. Innymi słowy, KDM7A zwykle hamuje zarówno programy genetyczne, jak i metaboliczne, które popychają makrofagi w kierunku stanu sprzyjającego włóknieniu.
W dalszych analizach badacze zidentyfikowali kluczowego partnera w tym układzie hamującym: białko-czujnik TLR8, które wykrywa fragmenty RNA wewnątrz komórek odpornościowych. Stwierdzili, że KDM7A pomaga utrzymać gen Tlr8 aktywny, usuwając represyjny znacznik chemiczny (H3K27me2) z regionu wzmacniającego (enhancer) w pobliżu Tlr8. Gdy Kdm7a został wyłączony, znacznik ten kumulował się, poziomy Tlr8 spadały, a cechy Fib-Mac nasilały się. Bezpośrednie zmniejszenie Tlr8 w makrofagach również popychało je w kierunku profibrotycznej tożsamości, podczas gdy aktywacja lub nadprodukcja TLR8 cofała ten proces, nawet przy braku Kdm7a. To umieszcza szlak KDM7A–TLR8 w centrum molekularnego obwodu chroniącego płuca przed nadmiernym bliznowaceniem.
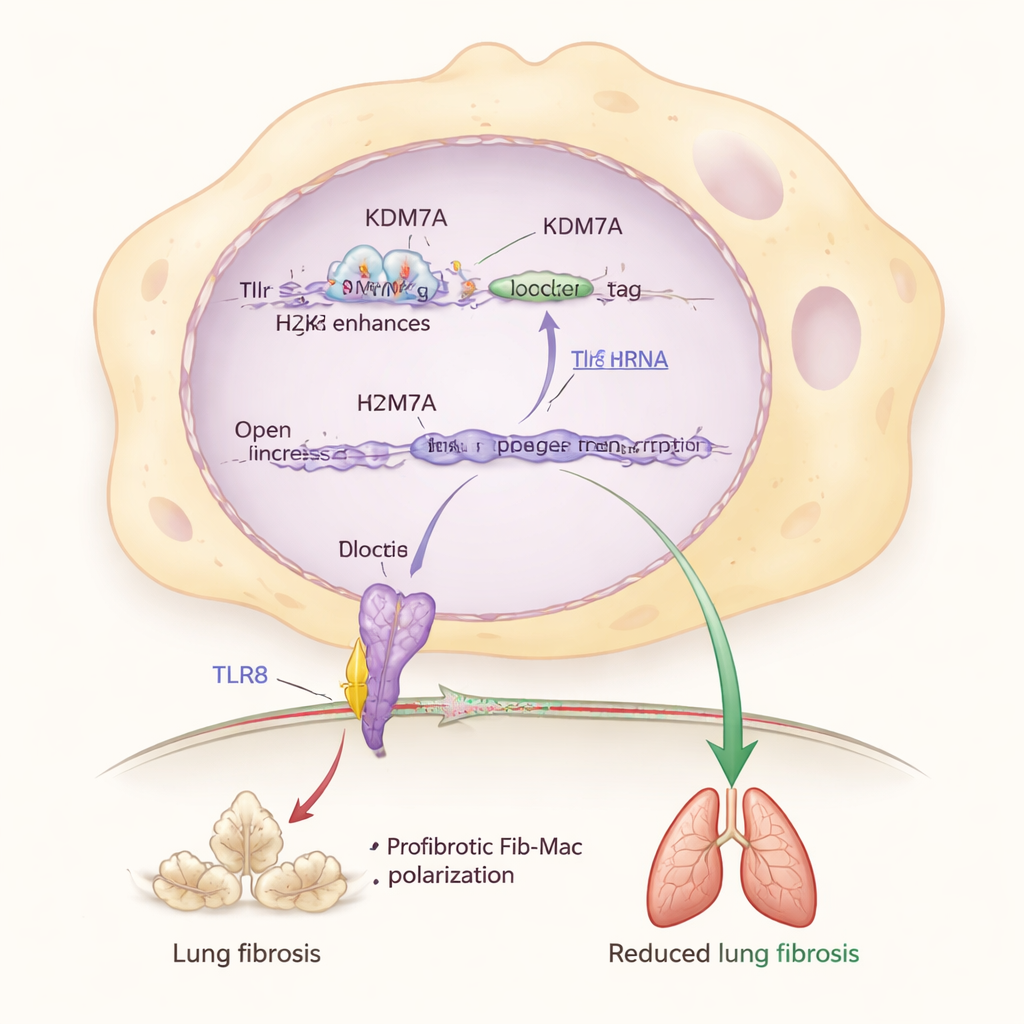
Od starzejących się płuc do chorób u ludzi
Aby powiązać te odkrycia z ludźmi, zespół zbadał tkankę płuc od pacjentów z chorobą włóknieniową. W porównaniu z tkanką kontrolną bez choroby, płuca włókniejące zawierały znacznie więcej makrofagów z markerami Fib-Mac, ale te same komórki wykazywały wyraźnie obniżone poziomy KDM7A i TLR8. Ponowna analiza istniejących zestawów danych z sekwencjonowania pojedynczych komórek od pacjentów z idiopatycznym włóknieniem płuc potwierdziła ten wzorzec: w miarę jak sygnatury Fib-Mac rosły, ekspresja KDM7A malała. Naukowcy przeanalizowali również dużą atlasową bazę danych myszy i stwierdzili, że ekspresja Kdm7a i Tlr8 w makrofagach spada wraz z wiekiem u samców, co odzwierciedla wyższe ryzyko włóknienia płuc u starszych mężczyzn. Sugeruje to, że związane z wiekiem i płcią osłabienie hamulca KDM7A–TLR8 może częściowo wyjaśniać, kto jest bardziej narażony na ciężkie bliznowacenie płuc.
Co to oznacza dla przyszłych terapii
Mówiąc w prostych słowach, praca ta pokazuje, że nasz układ odpornościowy nosi w sobie wewnętrzny mechanizm bezpieczeństwa, który zapobiega przekształceniu pomocnych komórek naprawczych w nadgorliwe jednostki napędzające trwałe blizny. KDM7A, działając przez TLR8, uniemożliwia makrofagom zablokowanie się w profibrotycznym trybie i tym samym pomaga zachować elastyczną, funkcjonalną tkankę płuc po urazie. Gdy ten system zawodzi — z powodu utraty genetycznej, starzenia lub innych czynników — makrofagi częściej stają się „wzmacniaczami blizn”, pogarszając włóknienie. Odkrycie tego epigenetycznego hamulca wskazuje na nowe strategie terapeutyczne: leki zwiększające aktywność KDM7A, naśladujące jego efekt lub ostrożna stymulacja TLR8 mogłyby kiedyś uzupełniać istniejące terapie przeciwfibrotyczne i oferować lepszą ochronę przed postępującym, ograniczającym życie bliznowaceniem płuc.
Cytowanie: Funagura, N., Koga, T., Etoh, K. et al. Histone demethylase KDM7A negatively regulates fibrotic macrophage polarization and lung fibrosis progression. Commun Biol 9, 309 (2026). https://doi.org/10.1038/s42003-026-09610-1
Słowa kluczowe: włóknienie płuc, makrofagi, epigenetyka, KDM7A, TLR8