Clear Sky Science · pl
Rozpoznawanie glikolipidów i wiązanie przez Siglec-6 zależą od interakcji z błoną komórkową
Jak nasze komórki rozróżniają „swoje” od „obcych”
Układ odpornościowy nieustannie skanuje własne komórki, decydując, kiedy zachować spokój, a kiedy zaatakować. Kluczowym elementem tego nadzoru jest rozpoznawanie cukrowych struktur na powierzchni komórek. Badanie to ujawnia, że jeden z ludzkich receptorów odpornościowych, nazwany Siglec-6, wykorzystuje nie tylko te cukry, lecz także samą błonę komórkową, aby podejmować wyjątkowo precyzyjne decyzje dotyczące wiązania. Ta nietypowa strategia może pomóc wyjaśnić, jak organizm dopracowuje sygnały odpornościowe i otwiera nowe możliwości terapeutyczne.
Bramkarz wyczuwający cukry na komórkach odpornościowych
Sigleki to rodzina receptorów obecnych na komórkach odpornościowych, które rozpoznają cukry zawierające kwas sjalowy i pomagają układowi odpornościowemu odróżniać „swoje” od „nie-swoich”. Większość Sigleców polega na jednym, silnie zachowanym aminokwasie — argininie — aby związać te cukry. Usunięcie tej argininy zwykle uniemożliwia wiązanie. Siglec-6 jest jednak wyjątkiem: wcześniejsze badania wykazały, że nadal potrafi wiązać niektóre lipidy z cukrem nawet przy zmutowanej tej kluczowej argininie. Nowe badanie miało wyjaśnić, jak Siglec-6 może „łamać” to pozorne prawo i co to oznacza dla jego roli na komórkach tucznych, pamięciowych limfocytach B oraz w komórkach ludzkiej łożyska.
Szczególne lipidy, których szuka Siglec-6
Na powierzchniach komórek istotne cukry mogą być prezentowane zarówno na białkach, jak i na lipidach. Praca koncentruje się na grupie lipidów z cukrem zwanych gangliozydami, zwłaszcza na trzech blisko spokrewnionych: GM1, GM2 i GM3. Wszystkie trzy wystawiają pojedynczą „główkę” zakończoną kwasem sjalowym ponad powierzchnią błony. Wcześniejsze eksperymenty pokazały, że Siglec-6 mocno wiąże GM1, gdy ten jest częścią błony, ale prawie wcale nie wiąże GM2 ani GM3, mimo że ich „główki” cukrowe są bardzo podobne. Za pomocą szczegółowych symulacji komputerowych realistycznych błon autorzy potwierdzili, że kwas sjalowy w GM1 i GM3 jest równie odsłonięty i dostępny. Innymi słowy, prosta fizyczna dostępność nie tłumaczy wyjątkowego statusu GM1. Zamiast tego krytyczną rolę odgrywa dodatkowy cukier na końcu GM1 — galaktoza terminalna — który pomaga odpowiednio ustawić Siglec-6 względem błony.
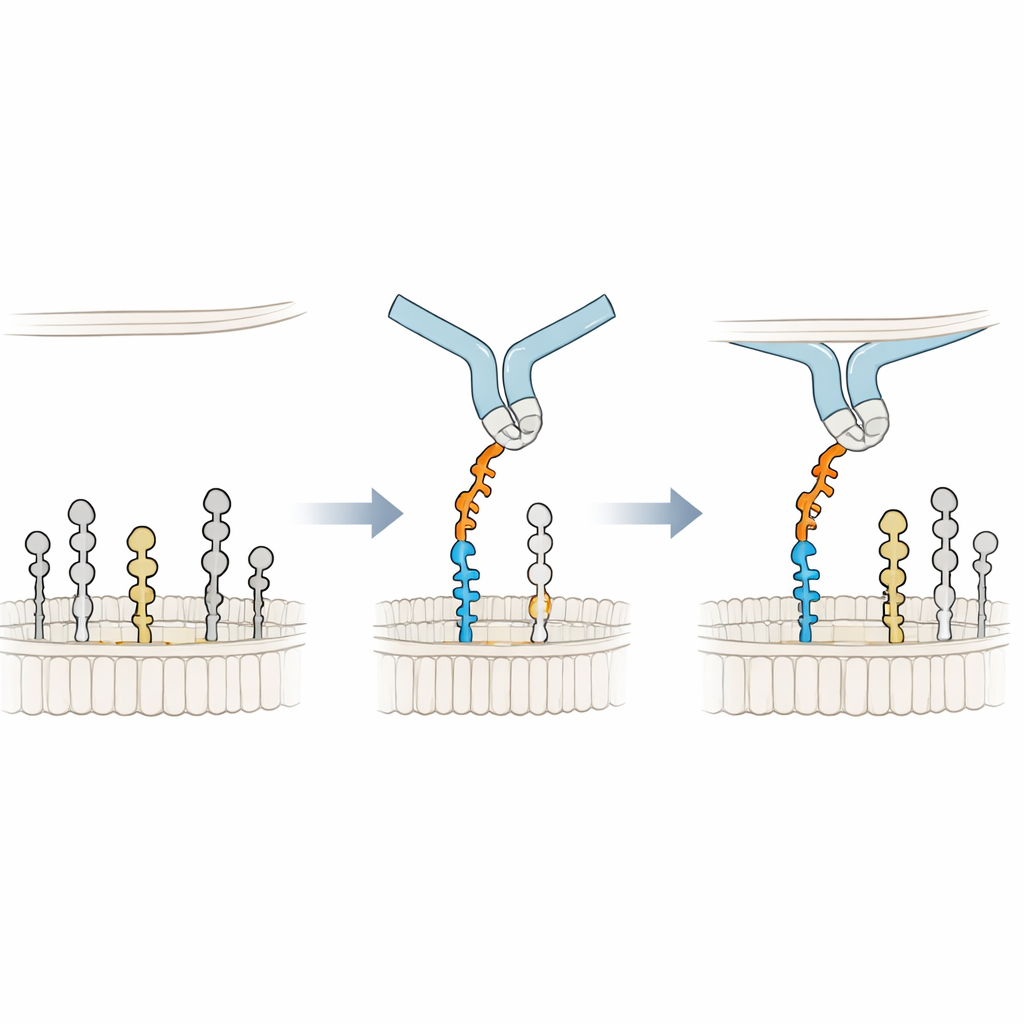
Opieranie się o błonę, by lepiej chwycić
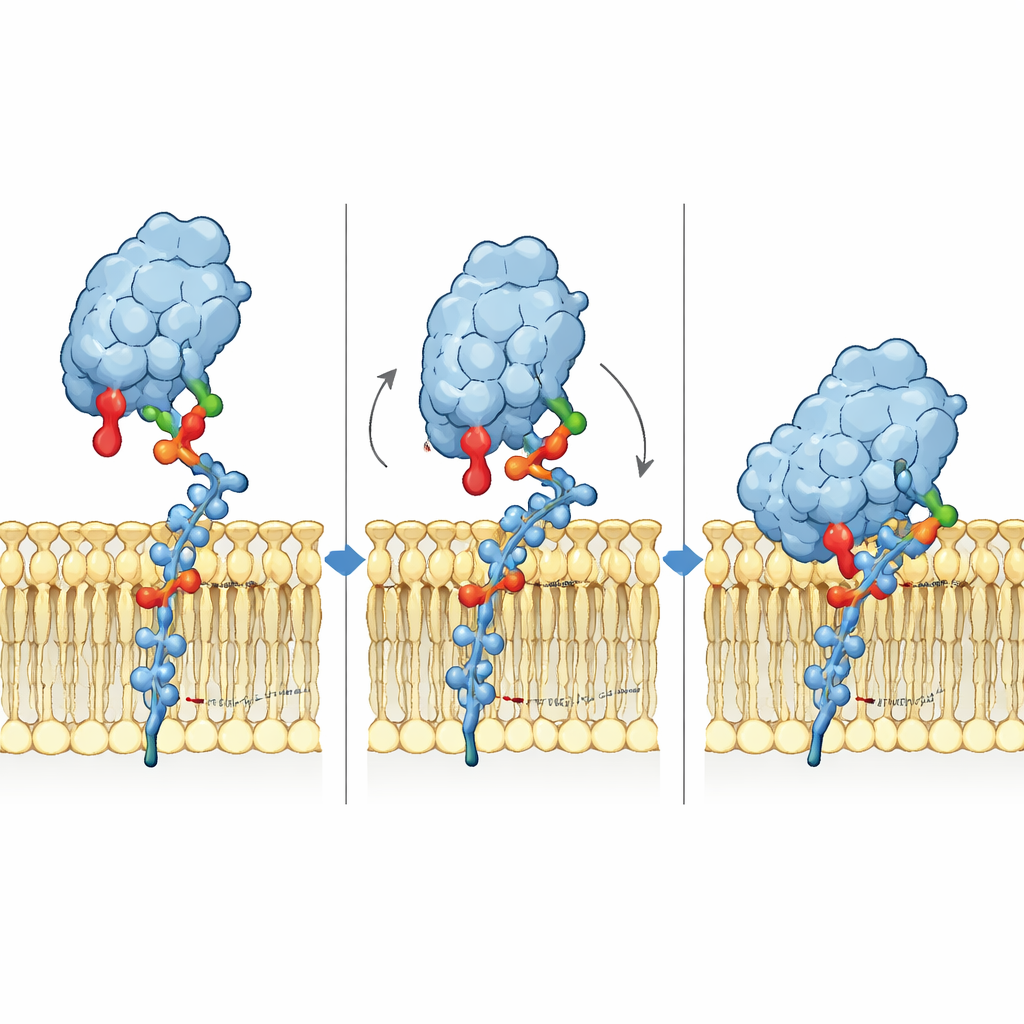
Aby zrozumieć mechanizm wiązania na poziomie atomowym, badacze zbudowali modele 3D Siglec-6 w kontakcie z GM1 w błonie i przeprowadzili długie symulacje dynamiki molekularnej. Odkryli, że Siglec-6 wciąż wykorzystuje swoją kanoniczną argininę (Arg122) do kontaktu z kwasem sjalowym, lecz ten kontakt migocze w czasie. Stabilność kompleksu zapewnia jednak coś nowego: pobliska tryptofan (Trp127) wsuwa się w tłustą część błony, podczas gdy przylegająca lizyna (Lys126) oddziałuje z naładowanymi grupami głów lipidów otoczenia. Ten „klin” w błonie uzupełnia zwykłą interakcję cukier–arginina, efektywnie pożyczając energię wiązania z otoczenia lipidowego. Gdy terminalna galaktoza GM1 zostaje usunięta, imitując GM2, elastyczna pętla w Siglec-6 wsuwa się w zwolnioną przestrzeń, odciąga receptor od błony i zakłóca to wspomagane przez błonę trzymanie, co tłumaczy utratę stabilnego wiązania.
Eksperymenty testujące mechanizm
Zespół następnie zweryfikował te komputerowe spostrzeżenia w żywych komórkach i testach biochemicznych. Zmodyfikowali komórki, aby wyrażały normalny lub zmutowany Siglec-6 i zmierzyli, jak dobrze komórki wiążą fluorescencyjne liposomy oraz małe dyski lipidowe zawierające GM1. Mutacja kanonicznej argininy tylko nieznacznie zmniejszyła wiązanie, gdy GM1 znajdował się w błonie, potwierdzając, że Siglec-6 nie polega wyłącznie na tym reszcie w takim kontekście. Natomiast mutacja Trp127 niemal całkowicie znosiła wiązanie do liposomów zawierających GM1, a mutacja obu: Trp127 i Lys126 prawie całkowicie eliminowała wiązanie. Te same mutanty wiązały się jednak normalnie do cukrów podobnych do GM1 prezentowanych poza błoną, co świadczy o zachowanej podstawowej strukturze Siglec-6. Pomiary spektrometrii mas natywnych dodatkowo wykazały, że Siglec-6 może wiązać nie tylko GM1, lecz także zwykłe fosfolipidy, a ta interakcja lipidowa zanika po usunięciu Trp127. Co godne uwagi, Siglec-6 przyczepiał się nawet do „nagich” liposomów pozbawionych GM1, ponownie w sposób zależny od Trp127, sugerując, że najpierw może rozpoznawać błonę, a następnie utrwalać wiązanie po napotkaniu GM1.
Wolne cukry opowiadają inną historię
Gdy te same trzy gangliozydy testowano jako wolne fragmenty cukrowe, a nie jako część błony, Siglec-6 zachowywał się bardziej jak jego krewni. W roztworze wiązał GM1, GM2 i GM3 z podobnie słabym powinowactwem, a teraz kanoniczna arginina była niezbędna: mutacja Arg122 wyraźnie zmniejszała wiązanie, podczas gdy mutacja Trp127 miała niewielki efekt. Ten kontrast pokazuje, że Siglec-6 skutecznie zmienia mechanizm w zależności od tego, czy napotyka cukry w błonie, czy w formie wolnej. W błonach polega na współdziałaniu między główką cukrową, terminalną galaktozą GM1 i bezpośrednim kontaktem z błoną; w roztworze wraca do klasycznego rozpoznawania skoncentrowanego wokół argininy.
Dlaczego to ma znaczenie dla kontroli odporności
W całości badanie ukazuje Siglec-6 jako precyzyjny czujnik, który wykorzystuje fizyczny kontekst błony, by wyostrzyć swoją specyficzność. Częściowo kotwicząc się w otaczających lipidach, może selektywnie rozpoznawać GM1 wśród bardzo podobnych gangliozydów, przekształcając ogólny „czytnik kwasu sjalowego” w detektor o wysokiej precyzji specyficznego wzoru powierzchniowego. Ta wspomagana przez błonę strategia wydaje się unikalna wśród dotychczas badanych Sigleców i może pomagać Siglec-6 skanować powierzchnie komórek w poszukiwaniu szczególnych sygnatur glikolipidowych, które regulują odpowiedzi odpornościowe lub oznaczają określone tkanki, na przykład ludzką łożysko. Zrozumienie tego podwójnego trybu rozpoznawania może wspierać projektowanie terapii i narzędzi diagnostycznych wykorzystujących niezwykłe połączenie sygnalizacji cukrowej i detekcji błonowej przez Siglec-6.
Cytowanie: D’Andrea, S., Schmidt, E.N., Bui, D. et al. Glycolipid recognition and binding by Siglec-6 hinges on interactions with the cell membrane. Commun Biol 9, 333 (2026). https://doi.org/10.1038/s42003-026-09609-8
Słowa kluczowe: Siglec-6, gangliozydy, błona komórkowa, rozpoznawanie glikolipidów, regulacja odporności