Clear Sky Science · pl
Destabilizacja otoczki przez nadekspresję AcrAB2NodT łączy oporność na antybiotyki z wrażliwością na metale u Caulobacter vibrioides
Gdy walka z antybiotykami ma ukrytą cenę
W miarę rozprzestrzeniania się oporności na antybiotyki zwykle wyobrażamy sobie bakterie jako po prostu twardsze i trudniejsze do zabicia. To badanie ujawnia zaskakujący zwrot akcji: w powszechnej bakterii słodkowodnej jeden mechanizm oporności na leki faktycznie czyni komórki bardziej podatnymi na niektóre metale, takie jak miedź i cynk. Zrozumienie tego ukrytego kompromisu może otworzyć nowe drogi do odwrócenia sytuacji na naszą korzyść, łącząc antybiotyki z innymi stresami wykorzystującymi słabości bakterii.
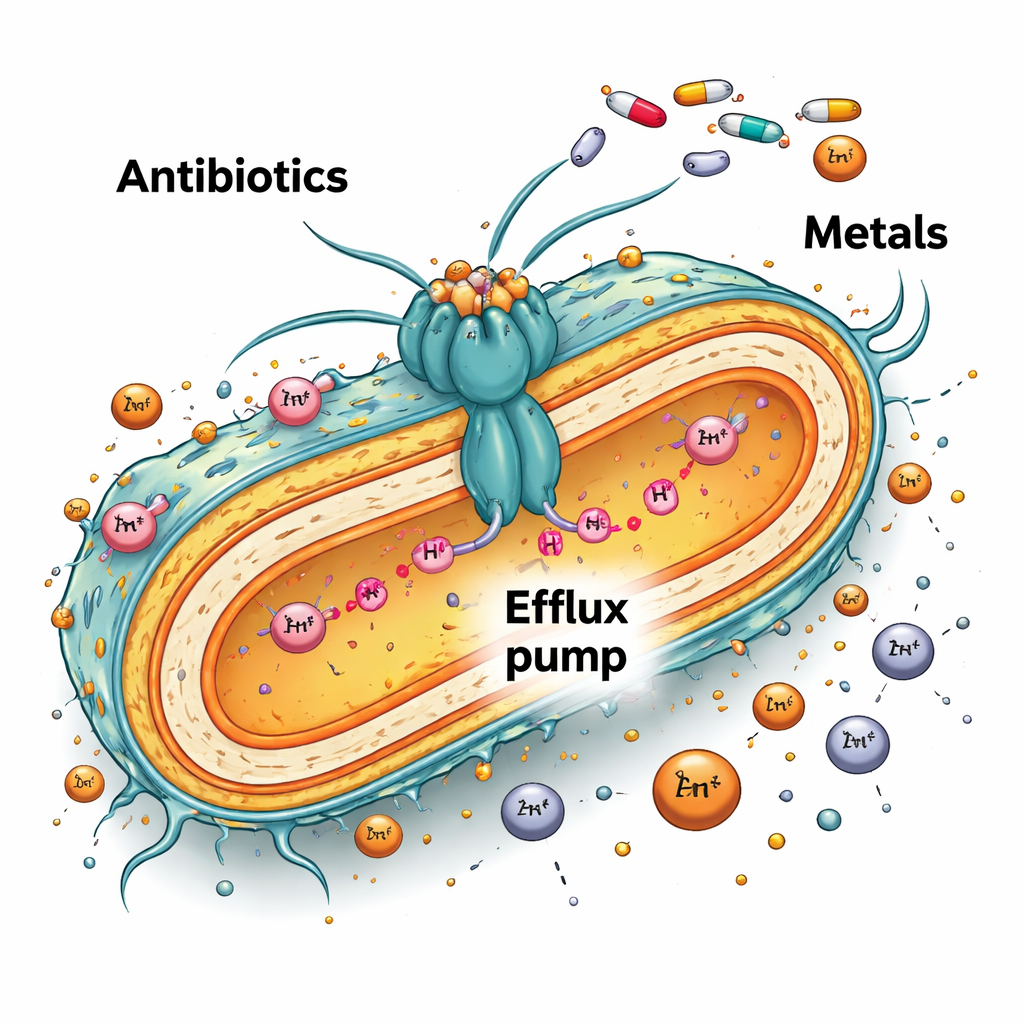
Pompa bakteryjna o podwójnej roli
Wiele bakterii broni się, używając potężnych molekularnych pomp osadzonych w ich zewnętrznych warstwach, które wypompowują szkodliwe związki, w tym antybiotyki. U Caulobacter vibrioides, wolno żyjącego mikroba dobrze radzącego sobie w ubogich w składniki jeziorach i rzekach, jedna z takich pomp nosi nazwę AcrAB2NodT. Przebiega ona przez błony wewnętrzną i zewnętrzną komórki i normalnie jest kontrolowana przez białko regulatorowe TipR. Gdy TipR jest obecny, pompę wytwarza się tylko wtedy, gdy jest potrzebna. Badacze sprawdzili, co się dzieje po usunięciu tipR, tworząc mutant, który działa tą pompą na pełnych obrotach przez cały czas.
Wygrywanie z lekami, przegrywanie z metalami
Mutant pozbawiony tipR rzeczywiście lepiej znosił niektóre antybiotyki beta-laktamowe, co potwierdza, że nadaktywna pompa pomaga komórkom wypompowywać leki. Jednak gdy zespół wystawił te komórki na działanie miedzi i innych metali, w tym cynku, niklu i kadmu, obraz się odwrócił: mutant stał się znacznie bardziej wrażliwy niż komórki normalne. Dokładne pomiary wykazały, że ta wrażliwość nie wynikała z akumulacji dodatkowej miedzi ani z produkcji większej ilości reaktywnych form tlenu. Zawartość metali wewnątrz mutanta była podobna do tej w komórkach normalnych, a standardowe wskaźniki stresu oksydacyjnego nie wzrosły. Oznaczało to, że podatność musiała wynikać ze zmian w strukturze komórki lub podstawowej fizjologii, a nie z prostego przeciążenia metalami.
Delikatna skóra i nieszczelna bariera
Przyglądając się bliżej powierzchni komórki, naukowcy użyli mikroskopii elektronowej i analiz białkowych, aby wykazać, że nadekspresja AcrAB2NodT zaburza bakteryjną „skórę”, zwaną otoczką komórkową. Komórki mutantów wykazywały wybrzuszenia, nietypowe kształty oraz falistą, nierówną przestrzeń między błoną wewnętrzną a zewnętrzną. Białka zaangażowane w budowę i przebudowę otoczki były bardziej obfite, co świadczy o tym, że komórki prowadziły stałą akcję naprawczą. Dodatkowe testy wykazały, że otoczka mutanta była bardziej przepuszczalna, pozwalając barwnikom łatwiej wnikać po eksperymentalnym wyłączeniu zdolności pompy do ich wypompowywania. Gdy badacze całkowicie unieruchomili pompę — albo przez usunięcie jej genów, albo przez wprowadzenie subtelnych mutacji, które pozostawiały ją obecna, lecz w dużej mierze nieaktywną — zarówno dziwne kształty komórek, jak i wrażliwość na metale w dużym stopniu zanikły, mimo że niektóre składniki pompy wciąż były obecne.
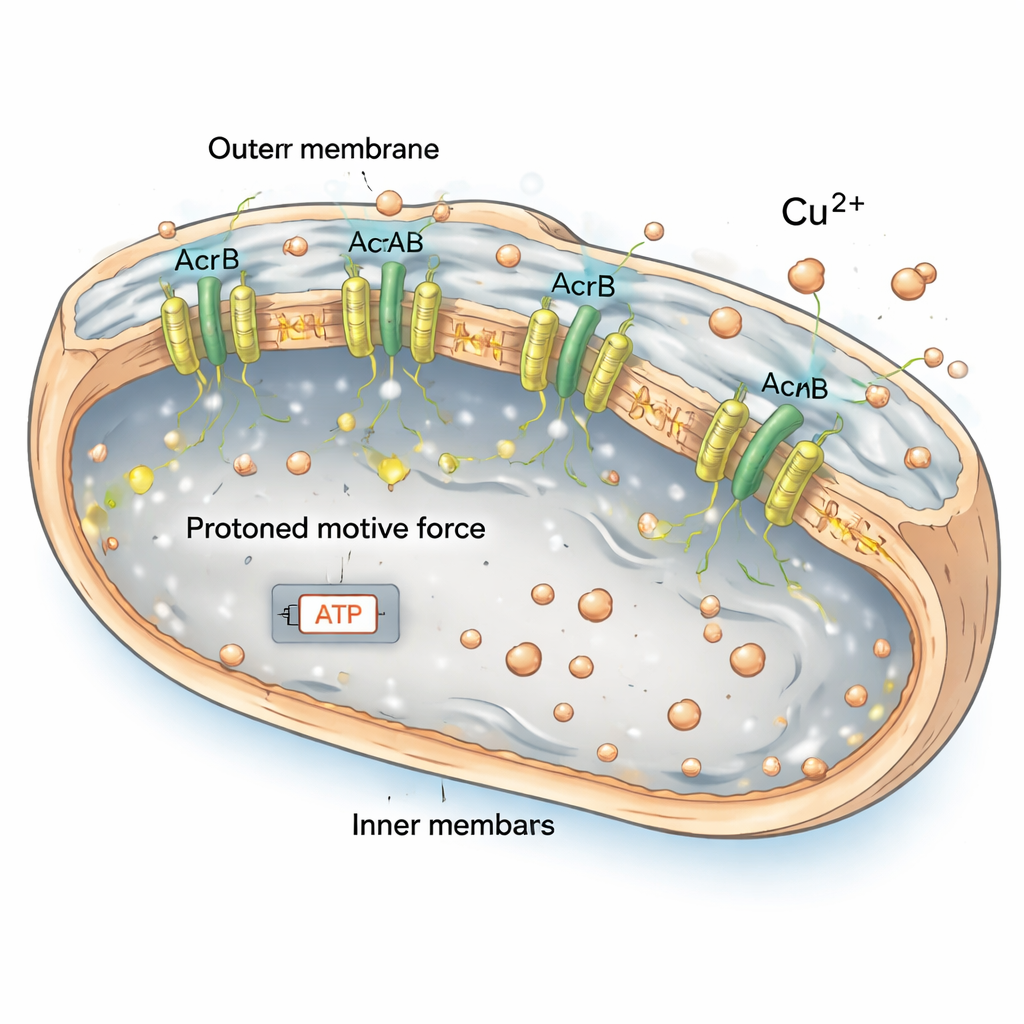
Rozładowane baterie i obciążenie energetyczne
Pompy wypompowujące, takie jak AcrAB2NodT, napędzane są siłą motoryczną protonów, pewnego rodzaju maleńką baterią wynikającą z różnicy ładunków po obu stronach błony wewnętrznej. W mutantach uruchomionych non stop ta „bateria” była częściowo rozładowana: barwnik raportujący napięcie błonowe wykazywał słabszy sygnał, a poziomy ATP, podstawowej waluty energetycznej komórki, były niższe. Bakterie próbowały to kompensować zwiększając szlaki wytwarzające energię, na przykład zaangażowane w rozkład kwasów tłuszczowych, lecz nie wystarczało to, by zapobiec ogólnemu niedoborowi energii. Gdy badacze chemicznie zniszczyli gradient protonowy w komórkach normalnych, te komórki zaczęły przypominać mutanta pod względem tego, jak słabo radziły sobie z miedzią. To mocno sugeruje, że kombinacja osłabionej otoczki i chronicznie niskiego poziomu energii sprawia, iż bakterie nadprodukujące pompę są wyjątkowo podatne na stres metaliczny.
Przekształcanie słabości w strategię leczenia
Dla osób niebędących specjalistami kluczowa wiadomość jest taka, że oporność na antybiotyki może mieć swoją cenę: bakterie mogą lepiej przetrwać leki, ale stać się bardziej kruche w innych aspektach. U Caulobacter ciągła praca potężnej pompy obciąża zewnętrzne warstwy i zasoby energetyczne komórki, przez co staje się ona mniej zdolna do radzenia sobie z metalami takimi jak miedź. Ten kompromis wskazuje na nowe pomysły terapeutyczne. Jeśli podobne słabości występują u bakterii wywołujących choroby, lekarze mogliby zwiększyć skuteczność antybiotyków, łącząc je z metalami lub innymi czynnikami, które wykorzystują energetyczne i strukturalne obciążenie mechanizmów oporności, doprowadzając oporne drobnoustroje za ich punkt krytyczny.
Cytowanie: Ote, M., Lardinois, L., Hendrickx, E. et al. Envelope destabilization by AcrAB2NodT overexpression links antibiotic resistance to metal sensitivity in Caulobacter vibrioides. Commun Biol 9, 313 (2026). https://doi.org/10.1038/s42003-026-09606-x
Słowa kluczowe: oporność na antybiotyki, pompy wypompowujące, wrażliwość na miedź, otoczka bakteryjna, metabolizm energetyczny