Clear Sky Science · pl
Hamowanie ATM zwiększa wydajność knock-in przez tłumienie aktywacji szlaków apoptozy wywołanej przez AAV
Ulepszanie edycji genów
Edycja genów metodą CRISPR obiecuje terapie chorób genetycznych, odporne uprawy i potężne narzędzia badawcze. Jednak jedna z jej najbardziej wartościowych umiejętności — precyzyjne wstawianie nowego DNA w wybrane miejsce w genomie, zwane „knock-in” — nadal działa niewystarczająco efektywnie. W tym badaniu zbadano, dlaczego niektóre komórki łatwiej przyjmują nowy DNA niż inne, i odkryto sposób, by skłonić komórki do częstszego wykonywania precyzyjnych edycji, zwłaszcza przy użyciu adeno‑zassobnego wirusa (AAV), wiodącego nośnika w terapii genowej.
Obserwowanie naprawy DNA w czasie rzeczywistym
Aby zrozumieć, co pomaga lub przeszkadza w precyzyjnym wstawianiu genów, badacze zbudowali skomplikowany „panel kontrolny” wewnątrz mysich embrionalnych komórek macierzystych. Ten potrójny system reporterów wykorzystuje trzy markery fluorescencyjne do śledzenia w tych samych komórkach, czy CRISPR przeciął DNA, czy nastąpił precyzyjny knock-in, oraz czy komórka zamiast tego wstawiła donorowy DNA przy użyciu bardziej niedokładnej metody naprawczej. Odczytując różne kombinacje kolorów za pomocą cytometrii przepływowej, mogli oddzielić czyste edycje oparte na matrycy od podatnych na błędy insercji i komórek nieedytowanych. To równoległe śledzenie pozwoliło im odwzorować, jak różne szlaki naprawy DNA przyczyniają się do każdego wyniku z dużo większą rozdzielczością niż starsze testy oparte na PCR.
Dwaj pomocnicy DNA, dwie bardzo różne odpowiedzi
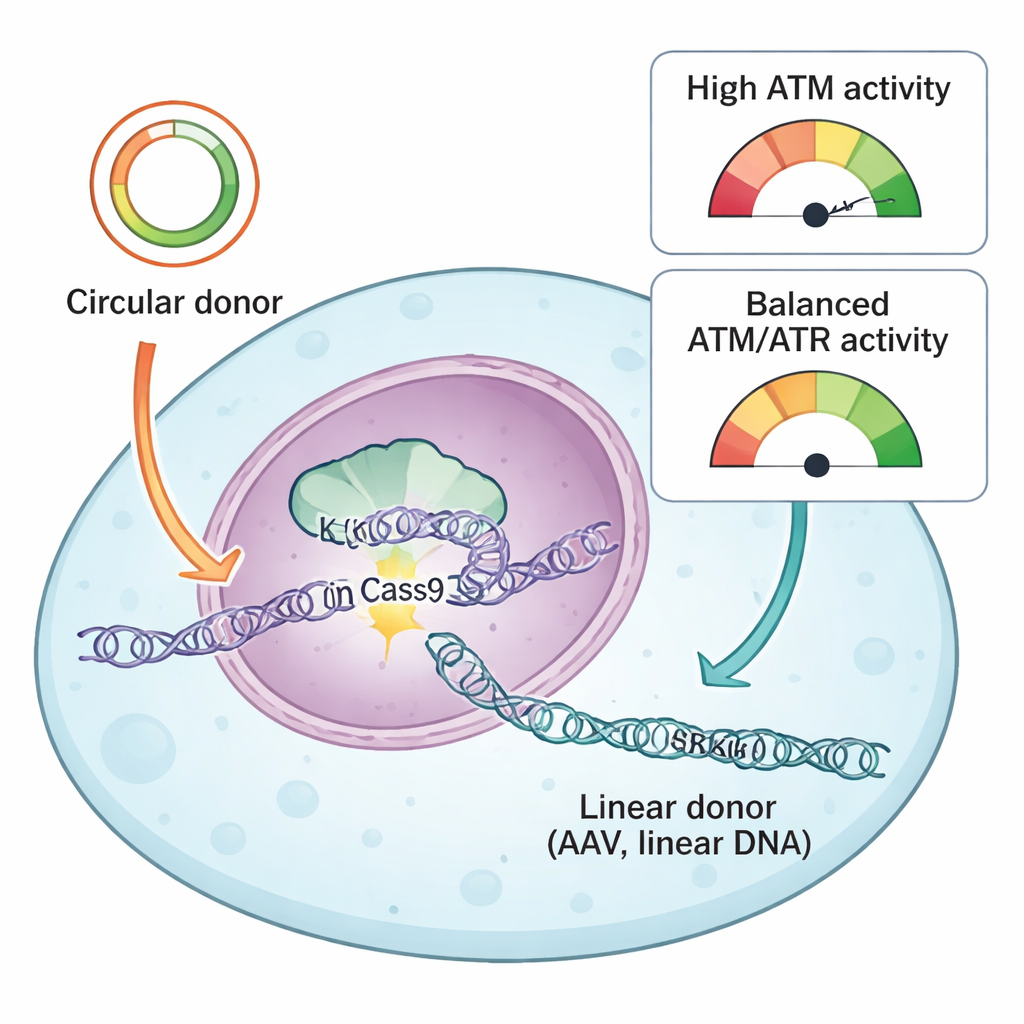
Zespół porównał dwa powszechne typy donorowego DNA stosowane do kierowania naprawami CRISPR: koliste plazmidy i liniowy DNA pochodzący z AAV. Oba niosą dopasowane „ramiona homologii”, które mówią komórce, gdzie wstawić nową sekwencję, ale wchodzą do komórki w różnych formach fizycznych. Koliste plazmidy to zamknięte pętle podwójnej nici DNA, podczas gdy donory AAV zwykle przybywają jako pojedyncze cząsteczki liniowe. Wykorzystując system reporterów i bibliotekę leków celujących białka odpowiedzi na uszkodzenia DNA, autorzy stwierdzili, że jedno kluczowe białko, ATR, było niezbędne dla udanych knock-inów dla obu typów donorów. Hamowanie ATR silnie zmniejszało precyzyjne wstawienia, podczas gdy łagodne wzmocnienie aktywności ATR poprzez szlak KEAP1–NRF2 zwiększało wydajność knock-inów, szczególnie przy donorach AAV.
Kiedy ochrona DNA działa na niekorzyść
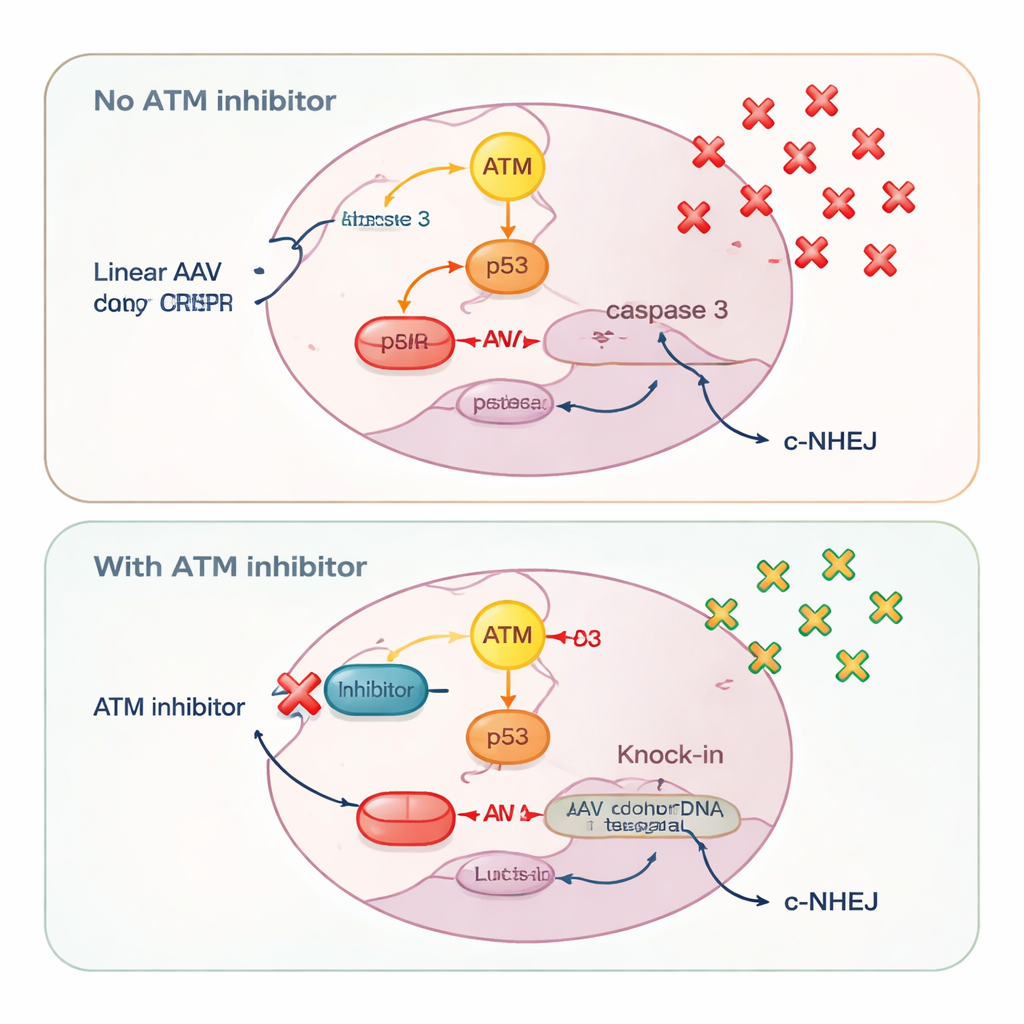
Inny sensor uszkodzeń DNA, ATM, okazał się zachowywać w sposób wyraźnie zależny od typu donora. Przy kolistych donorach plazmidowych blokada ATM zmniejszała zarówno precyzyjny knock-in, jak i insercje mediowane przez łączenie końców (end-joining), co odpowiada klasycznej roli ATM w pomocy przy naprawie pęknięć dwuniciowych. Jednak przy liniowym DNA — czy to pochodzącym z AAV, samokomplementarnego AAV, czy plazmidów pociętych na kawałki — hamowanie ATM działało odwrotnie: zwiększało wydajność knock-inów. Badacze przypisali ten efekt temu, jak komórki interpretują napływy liniowego DNA. Duże dawki AAV silnie aktywowały ATM, które z kolei uruchamiało p53 i kaspazę 3, główne elementy programu zaprogramowanej śmierci komórkowej. Komórki, które przyjęły wiele kopii donorowego DNA i w związku z tym miały największą szansę na udany knock-in, były też najbardziej narażone na zabicie przez ten system alarmowy.
Ocalenie najlepiej wyposażonych komórek
Dodając inhibitory ATM, naukowcy uciszyli szlak śmierci ATM–p53–kaspaza 3. W ten sposób oszczędzili komórki niosące duże ilości donorowego DNA, pozwalając większej ich liczbie przetrwać wystarczająco długo, by zakończyć precyzyjny knock-in. Pomiary liczby kopii genomu wirusowego potwierdziły, że hamowanie ATM zwiększyło liczbę cząsteczek AAV utrzymywanych wewnątrz komórek. Jednocześnie blokada ATM nieco osłabiła szybki, tępawy szlak naprawy zwany klasycznym niehomologicznym łączeniem końców (c-NHEJ), co wykazano poprzez zmniejszoną aktywację DNA‑PK, kluczowej enzymaty w tym szlaku. Osłabienie tej konkurencyjnej opcji naprawy pchnęło więcej przecięć CRISPR w kierunku knock-inów opartych na homologii, zamiast szybkich łatanek ignorujących matrycę donorową.
Co to znaczy dla przyszłych terapii genowych
Dla osób niebędących specjalistami przesłanie jest takie: te same mechanizmy ochronne komórek, które chronią nas przed uszkodzeniem DNA, mogą mimowolnie sabotować precyzyjną edycję genów, szczególnie gdy używa się dużych ilości wirusowego donorowego DNA. Praca ta pokazuje, że delikatne dostrojenie tych zabezpieczeń — utrzymanie aktywnego ATR przy jednoczesnym tymczasowym powstrzymaniu ATM, gdy obecne są liniowe donory takie jak AAV — może uczynić knock-iny CRISPR bardziej niezawodnymi i wydajnymi. Taka strategia mogłaby poprawić terapie genowe, inżynierię komórek i modele chorób, pomagając większej liczbie komórek zaakceptować zamierzoną zmianę przy jednoczesnym unikaniu niepotrzebnej utraty komórek.
Cytowanie: Natsagdorj, ME., Hara, H., Uosaki, H. et al. ATM Inhibition Enhances Knock-in Efficiency by Suppressing AAV-Induced Activation of Apoptotic Pathways. Commun Biol 9, 177 (2026). https://doi.org/10.1038/s42003-026-09604-z
Słowa kluczowe: CRISPR knock-in, edycja genów AAV, odpowiedź na uszkodzenia DNA, hamowanie ATM, inżynieria genomu