Clear Sky Science · pl
STING kontroluje glikolizę i lactylację histonów, napędzając metaboliczne przeprogramowanie makrofagów w pooperacyjnym ileus
Kiedy operacja sprawia, że jelito biernie się zatrzymuje
Po zabiegu chirurgicznym w obrębie jamy brzusznej wiele osób doświadcza, że jelita po prostu nie chcą powrócić do pracy. To zwolnienie, nazywane pooperacyjnym ileusem, może oznaczać dni nudności, wzdęć i opóźnionej rekonwalescencji. Streszczenie przedstawionego badania formułuje pozornie proste pytanie: dlaczego niektóre komórki odpornościowe w jelicie utrzymują tę bezruch, i czy przyciszenie jednego molekularnego przełącznika mogłoby pomóc jelitu znów się poruszyć?
Jak rutynowa operacja wywołuje zapalenie jelit
Zabieg w obrębie jamy brzusznej nieuchronnie narusza integralność jelit. U myszy delikatne manipulacje jelitem wystarczyły, by wywołać obrzęk, nagromadzenie płynu i zatkanie treści w jelicie cienkim. Gdy badacze śledzili, jak daleko nieszkodliwy, fluorescencyjny barwnik przesuwa się przez przewód pokarmowy, zaobserwowali znaczące spowolnienie jego przemieszczania — znak upośledzonej motoryki. Mikroskopowe badanie ściany jelita wykazało, że warstwa mięśniowa — tkanka, która faktycznie kurczy się, by przesuwać treść — stała się zapalna i zapełniona napływającymi komórkami odpornościowymi, w szczególności makrofagami i neutrofilami. Wyniki te sugerują, że własna warstwa mięśniowa jelita staje się po operacji miejscem intensywnego zapalenia, a to lokalne zapalenie jest ściśle związane z paraliżem jelit.
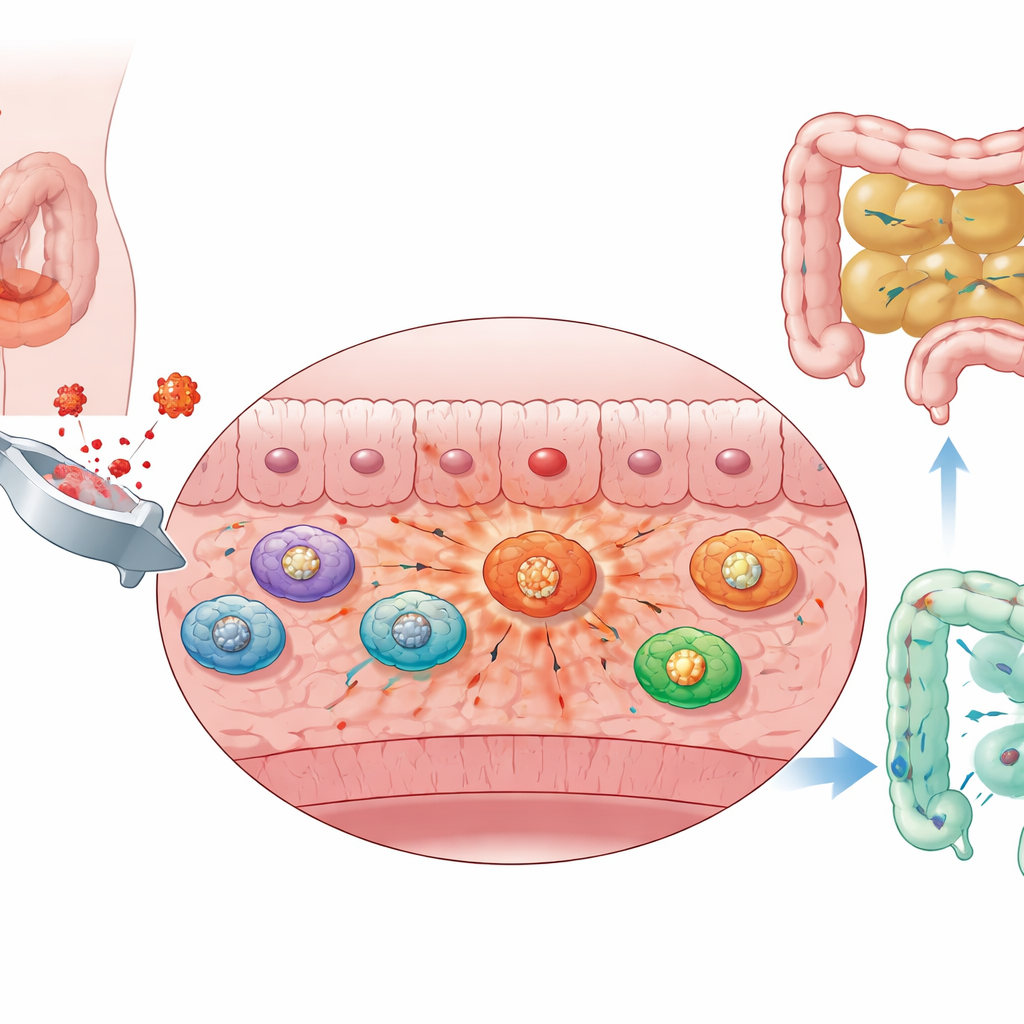
Makrofagi zmieniają paliwo i podsycają ogień
Aby zrozumieć, co robiły napływające makrofagi, zespół przeanalizował dane dużej skali: transkryptomowe i pojedynczokomórkowe z warstwy mięśniowej jelita. Odkryli, że makrofagi u zwierząt po operacji znacząco zwiększyły aktywność szybkiej, „cukro-spalającej” ścieżki znanej jako glikoliza. W porównaniu z innymi komórkami odpornościowymi w tym samym tkankowym mikrośrodowisku, infiltrujące makrofagi miały najwyższe wskaźniki glikolizy i wykazywały podwyższone poziomy kluczowych enzymów glikolitycznych. Wyodrębniono także odrębną podpopulację tych komórek silnie zależną od glikolizy, wykazującą silne sygnatury zapalne i intensywnie reagującą na składniki bakteryjne, takie jak lipopolisacharyd. Innymi słowy, makrofagi przestawiły się na tryb wysokiego „cukru” i wysokiego stanu zapalnego, co wydaje się pogłębiać zapalenie warstwy mięśniowej i utrzymywać jelito w stanie bezruchu.
Molekularny przełącznik łączący wykrywanie zagrożenia z spalaniem cukru
Następnie badacze skupili się na STING — białku znanym przede wszystkim jako system alarmowy wykrywający obce DNA, lecz coraz częściej rozpoznawanym także jako regulator metabolizmu. W zapalnej warstwie mięśniowej jelita podzbiór makrofagów o wysokiej glikolizie wykazywał znacząco wyższe poziomy STING, co potwierdzono barwieniami tkankowymi. W hodowlach komórkowych ekspozycja makrofagów na bakteryjny lipopolisacharyd zwiększała zarówno aktywność STING, jak i poziomy enzymów glikolitycznych, które przekształcają glukozę w energię i mleczan. Po wyłączeniu genu STING ten „wybuch” spalania cukru zaniknął: spadły stężenia pośrednich produktów glikolizy, zmniejszyła się zakwaszenie pożywki hodowlanej i wytwarzanie reaktywnych form tlenu. Komórki pozbawione STING produkowały także mniej mleczanu, co sugeruje ścisłe sprzężenie między ścieżką alarmową a silnikiem metabolicznym.
Od odpadu cukrowego do epigenetycznej pamięci
Mleczan jest często postrzegany jako produkt odpadowy metabolizmu, ale tutaj pełni subtelniejszą funkcję. Zespół wykazał, że w normalnych makrofagach napływ mleczanu jest wykorzystywany do chemicznej modyfikacji histonów — białek pakujących DNA — poprzez proces zwany lactylacją. Ta modyfikacja była szczególnie widoczna w miejscu H4K8 na histonach w pobliżu genu HK2, kluczowego enzymu kontrolującego glikolizę. W komórkach pozbawionych STING lactylacja histonów i dostępność chromatyny w rejonie promotora HK2 były zmniejszone, a specjalistyczne metody sekwencjonowania potwierdziły, że te zmiany osłabiły aktywację HK2. Równocześnie czynnik transkrypcyjny IRF3 okazał się wiązać bezpośrednio z promotorem HK2 łatwiej wtedy, gdy obecny był znak lactylacji histonów. Wspólnie te kroki tworzą samonapędzającą się pętlę: STING stabilizuje czynniki zwiększające glikolizę, glikoliza produkuje mleczan, mleczan modyfikuje histony, co otwiera gen HK2, a IRF3 nasila ekspresję HK2, dalej zasilając glikolizę i stan zapalny.
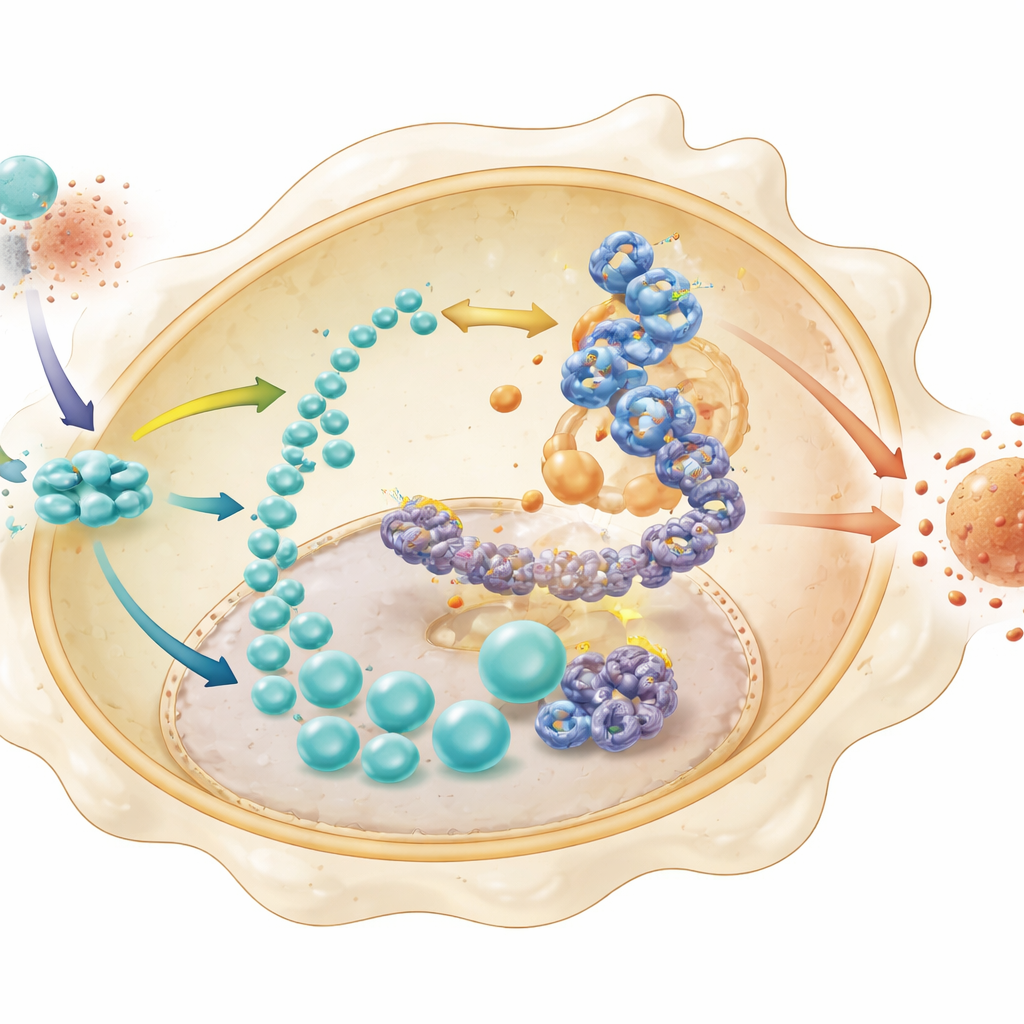
Przerwanie pętli, by pozwolić jelitu odzyskać funkcję
Na koniec zespół sprawdził, czy przerwanie tej pętli rzeczywiście może pomóc zwierzętom w powrocie do zdrowia po pooperacyjnym ileusie. U myszy pozbawionych STING tkanka mięśniowa jelita wykazywała mniejszą ekspresję enzymów glikolitycznych, zawierała mniej zapalnych makrofagów i przesunęła stosunek populacji makrofagów z agresywnego, prozapalnego stanu w kierunku profilu sprzyjającego ustępowaniu zapalenia. Napływ neutrofili był niższy, a pasaż jelitowy poprawił się. Farmakologiczne blokowanie STING u normalnych myszy przyniosło podobne korzyści, podczas gdy ponowna aktywacja enzymu HK2 u zwierząt pozbawionych STING częściowo przywróciła stan zapalny i zaburzenia motoryki. Dla czytelnika niezwiązanego z tematem przesłanie jest jasne: pojedynczy przełącznik wykrywający zagrożenie w makrofagach jelitowych może przestawić ich metabolizm w sposób, który zamyka jelito w przedłużonym bezruchu po operacji. Celowanie w STING — lub w regulowaną przez niego pętlę spalania cukru i zapisywania mleczanu w histonach — oferuje obiecującą drogę do przyspieszenia rekonwalescencji i złagodzenia jednego z najbardziej uporczywych powikłań zabiegów brzusznych.
Cytowanie: Chen, K., Li, G., Cheng, Y. et al. STING controls glycolysis and histone lactylation to drive macrophage metabolic reprogramming in postoperative ileus. Commun Biol 9, 358 (2026). https://doi.org/10.1038/s42003-026-09602-1
Słowa kluczowe: pooperacyjny ileus, metabolizm makrofagów, szlak STING, glikoliza, zapalenie jelit