Clear Sky Science · pl
Charakteryzacja podatności nanoprzeciwciał na rozwój terapeutyczny w celu ulepszenia projektowania leków za pomocą Therapeutic Nanobody Profiler
Dlaczego mali kuzyni przeciwciał mają znaczenie dla przyszłych leków
Wiele dzisiejszych leków‑bestsellerów to przeciwciała — białka, które z wielką precyzją wiążą cele chorobowe. Nowsza klasa jeszcze mniejszych wiążących molekuł, zwana nanoprzeciwciałami, potrafi wślizgnąć się w trudno dostępne zagłębienia wirusów, guzów i innych cząsteczek. Jednak zdolność do wiązania celu to nie wszystko: kandydat na lek musi być też łatwy do wytworzenia, stabilny w fiolce i bezpieczny w organizmie. W artykule przedstawiono Therapeutic Nanobody Profiler — narzędzie obliczeniowe zaprojektowane tak, by pomóc naukowcom wcześnie, na podstawie samego ciągu aminokwasów, ocenić, które nanoprzeciwciała mają największe szanse stać się praktycznymi lekami.
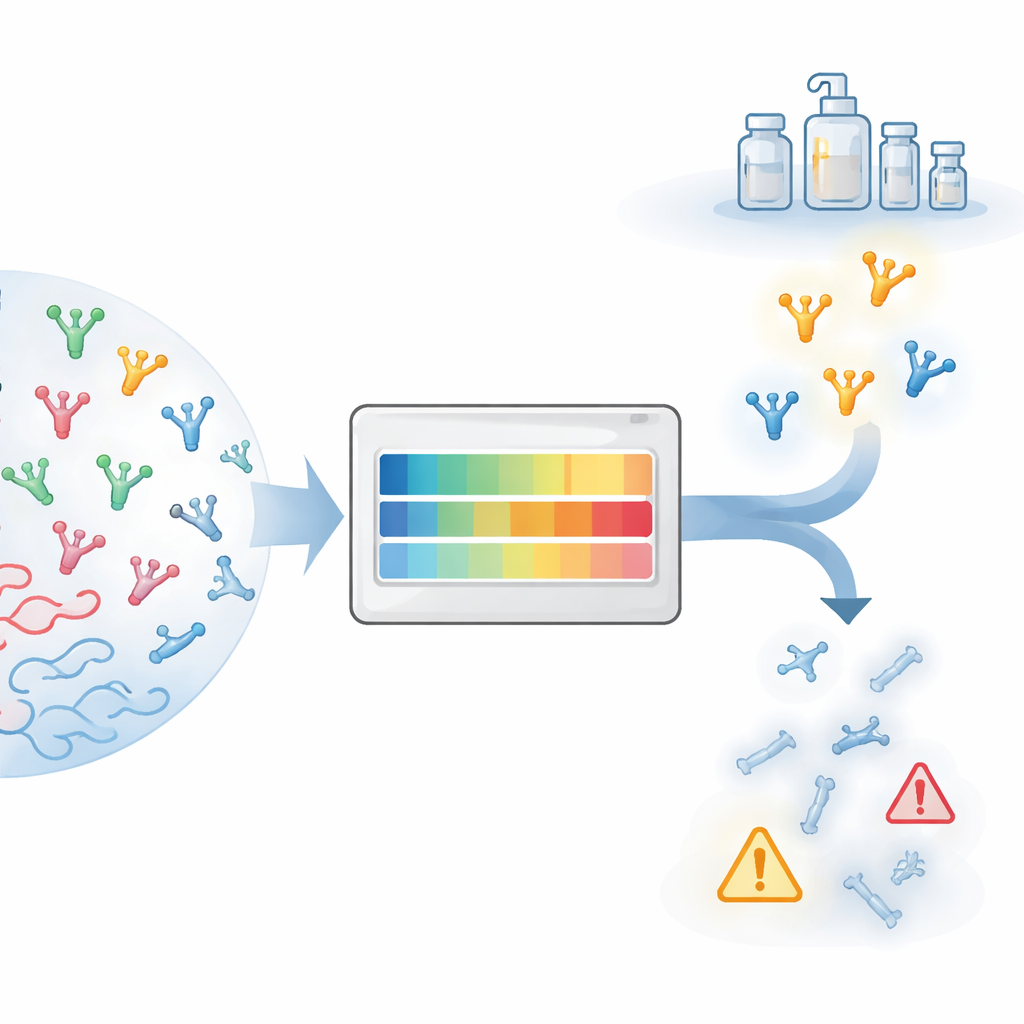
Od obiecującego pomysłu do praktycznego leku
Przekształcenie białka w rzeczywistą terapię wiąże się z wieloma praktycznymi przeszkodami określanymi łącznie jako „rozwijalność”. Białka muszą być produkowane w dużych ilościach, pozostawać rozpuszczalne, unikać tworzenia agregatów oraz zachowywać stabilność podczas transportu i przechowywania. W ostatniej dekadzie badacze nauczyli się przewidywać wiele z tych cech dla pełnowymiarowych przeciwciał monoklonalnych, wspierając te metody bogatymi danymi klinicznymi i specjalistycznymi testami laboratoryjnymi. Nanoprzeciwciała są jednak strukturalnie inne: składają się z pojedynczej domeny zamiast pary łańcuchów, często mają dłuższe pętle wiążące i odsłaniają obszary powierzchni, które w konwencjonalnych przeciwciałach są zakryte. W rezultacie metody dopasowane do zwykłych przeciwciał mogą dawać mylące wyniki przy zastosowaniu do nanoprzeciwciał.
Profiler zbudowany pod kątem osobliwości nanoprzeciwciał
Aby rozwiązać tę rozbieżność, autorzy opracowali Therapeutic Nanobody Profiler (TNP), inspirowany wcześniejszym narzędziem dla standardowych przeciwciał, ale przeprojektowanym z uwzględnieniem biologii nanoprzeciwciał. Skompilowali sekwencje nanoprzeciwciał z wielu źródeł: badań klinicznych, naturalnych repertuarów immunologicznych, patentów, prac naukowych i znanych struktur krystalograficznych. Korzystając z predyktorów struktury opartych na głębokim uczeniu, dostosowanych do przeciwciał jednodomenowych, wygenerowali modele 3D dla tych sekwencji. Z każdego modelu mierzyli długość pętli wiążących, jak daleko jedna kluczowa pętla wystaje od korpusu białka oraz jak rozmieszczone są skupiska hydrofobowych i naładowanych reszt na powierzchni — cechy mocno wpływające na rozpuszczalność, agregację i niespecyficzne przywieranie.
Dwa strukturalne warianty, oba użyteczne
Jednym z najbardziej uderzających odkryć jest to dotyczące głównej pętli wiążącej, znanej jako CDR3. Gdy zespół skwantyfikował, jak „kompaktowa” jest ta pętla — porównując jej długość z tym, jak daleko wystaje od białka — zaobserwowano wyraźny podział na dwa style strukturalne. W jednym podtypie pętla jest dłuższa i składa się z powrotem nad bokiem białka, tworząc wiele stabilizujących kontaktów z zestawem charakterystycznych reszt. W drugim pętla wystaje bardziej, podobnie jak w konwencjonalnym fragmencie przeciwciała. Nanoprzeciwciała w fazie klinicznej występują w obu podtypach, a porównanie licznych praktycznych pomiarów laboratoryjnych — takich jak agregacja, samo‑asocjacja i stabilność termiczna — nie wykazało systematycznej kary dla żadnego ze stylów. Oznacza to, że projektanci leków nie muszą faworyzować jednego kształtu pętli kosztem drugiego, pod warunkiem że pozostałe właściwości są akceptowalne.
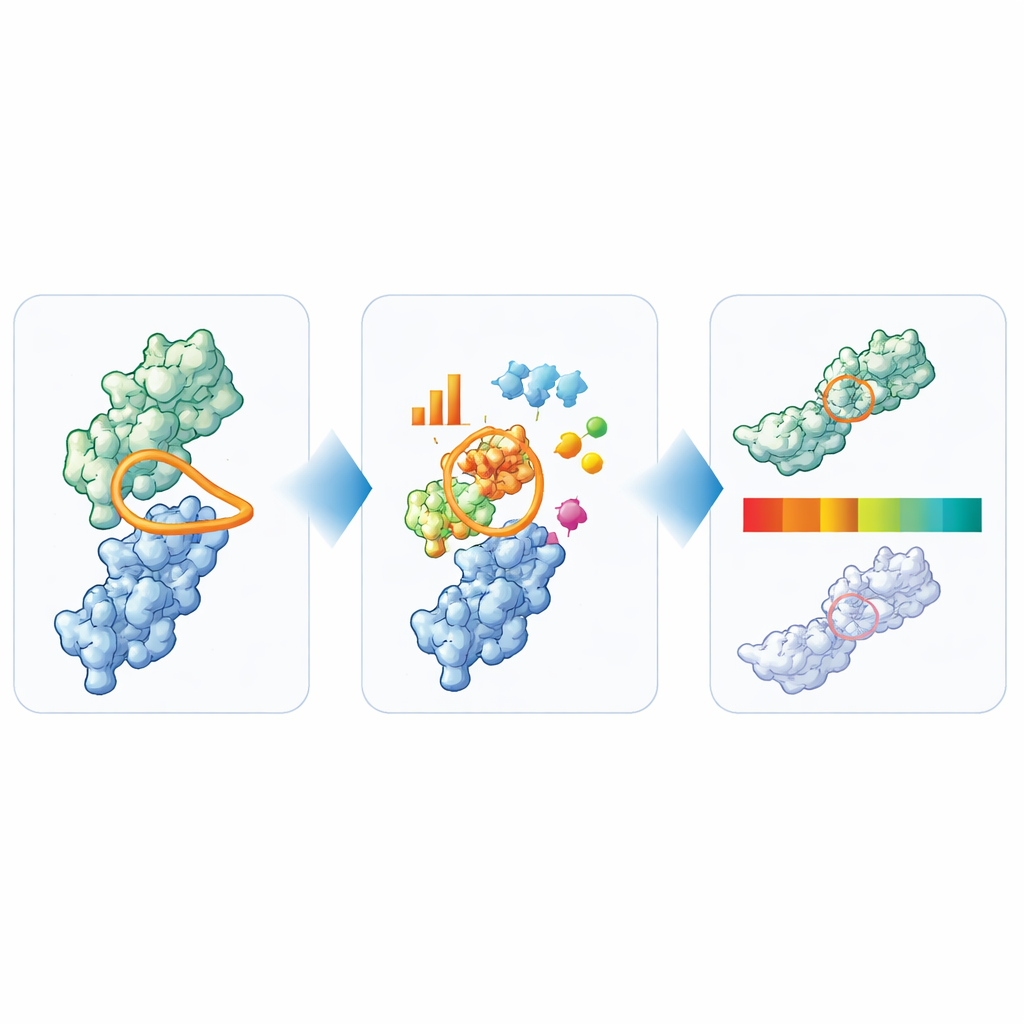
Przekształcanie struktury w proste sygnalizatory
Z szerokiej analizy autorzy wydestylowali sześć kluczowych cech, które razem oddają główne obawy dotyczące rozwijalności nanoprzeciwciał: całkowitą długość pętli, specyficzną długość i kompaktowość CDR3 oraz rozmiary hydrofobowych, dodatnio naładowanych i ujemnie naładowanych łatek powierzchniowych wokół miejsca wiązania. Następnie użyli 36 nanoprzeciwciał, które osiągnęły testy kliniczne, by ustalić praktyczne granice dla każdego miernika. Wartości w centralnym, często występującym zakresie oznaczono jako „zielone”, wartości na granicy jako „amber”, a wyraźne odchylenia jako „czerwone”. Aby sprawdzić informatywność tych sygnałów, zastosowali TNP do 72 dodatkowych, zastrzeżonych nanoprzeciwciał i porównali oznaczenia z obszernym panelem testów laboratoryjnych. Nanoprzeciwciała oznaczone przez TNP jako wyraźne odstępstwa zazwyczaj też wykazywały wiele eksperymentalnych sygnałów ostrzegawczych, podczas gdy te ocenione jako czyste komputerowo częściej zachowywały się dobrze w laboratorium.
Co to oznacza dla przyszłych terapii
Dla osób niebędących specjalistami główne przesłanie jest takie: kształt i wzór powierzchni nanoprzeciwciała można teraz przekształcić w prosty profil rozwijalności zanim rozpoczną się kosztowne prace laboratoryjne. Therapeutic Nanobody Profiler nie zastępuje eksperymentów i wciąż zdarzają się rozbieżności między predykcjami a testami, zwłaszcza że testy laboratoryjne przeprowadzano na nanoprzeciwciałach połączonych z większymi fragmentami przeciwciał. Jednak przez szybkie oznaczanie kandydatów o niezwykle długich lub mocno złożonych pętlach bądź o problematycznych łatkach powierzchniowych, TNP pomaga ukierunkować uwagę na nanoprzeciwciała, które z większym prawdopodobieństwem staną się niezawodnymi lekami. W miarę jak więcej nanoprzeciwciał wejdzie do badań klinicznych i powiększy zestaw odniesienia, narzędzie to powinno stać się jeszcze dokładniejsze, przyspieszając projektowanie małych, trwałych leków przypominających przeciwciała na szeroki zakres chorób.
Cytowanie: Gordon, G.L., Gervasio, J., Souders, C. et al. Characterising nanobody developability to improve therapeutic design using the Therapeutic Nanobody Profiler. Commun Biol 9, 344 (2026). https://doi.org/10.1038/s42003-026-09594-y
Słowa kluczowe: nanoprzeciwciała, rozwijalność leków biologicznych, profilowanie obliczeniowe, inżynieria przeciwciał, stabilność białek