Clear Sky Science · pl
Degradacja TUBB3 w komórkach Kupffera zależna od DTX1 łagodzi rozwój raka wątrobowokomórkowego przez regulację polaryzacji M1/M2
Dlaczego „sąsiedzi” immunologiczni w wątrobie mają znaczenie
Większość osób myśli o raku jako o chorobie wynikającej z niekontrolowanego wzrostu złośliwych komórek. Tymczasem guzy znajdują się w tętniącej życiem okolicy złożonej z komórek układu odpornościowego, naczyń i tkanki podporowej, które mogą albo zwalczać nowotwór, albo potajemnie mu pomagać. W tym badaniu przeanalizowano raka wątroby — konkretnie raka wątrobowokomórkowego — i odkryto, jak białko w wyspecjalizowanych komórkach odpornościowych wątroby może przechylać równowagę między odpowiedzią antynowotworową a środowiskiem sprzyjającym guzowi. Zrozumienie tego ukrytego „włącznika” może otworzyć nowe drogi do poprawy istniejących terapii immunologicznych.
Rak wątroby napędzany przez swoje otoczenie
Wątroba jest bogata w komórki układu odpornościowego, w tym w populację rezydentnych makrofagów zwanych komórkami Kupffera, które normalnie pomagają utrzymać narząd w zdrowiu. W raku wątroby wiele z tych komórek przekształca się w makrofagi związane z guzem, które mogą albo atakować nowotwór (stan podobny do M1), albo go chronić (stan podobny do M2). Pacjenci, których guzy są przesycone makrofagami typu M2, mają zwykle gorsze rokowanie i często słabo odpowiadają na leki odblokowujące mechanizmy odpornościowe, takie jak inhibitory PD-1. Autorzy zaczęli od analizy publicznych baz genowych i próbek pacjentów w poszukiwaniu cząsteczek powiązanych jednocześnie z rakiem wątroby i tymi makrofagami, skupiając uwagę na białku strukturalnym TUBB3, które niespodziewanie było obficie obecne w tkance nowotworowej.
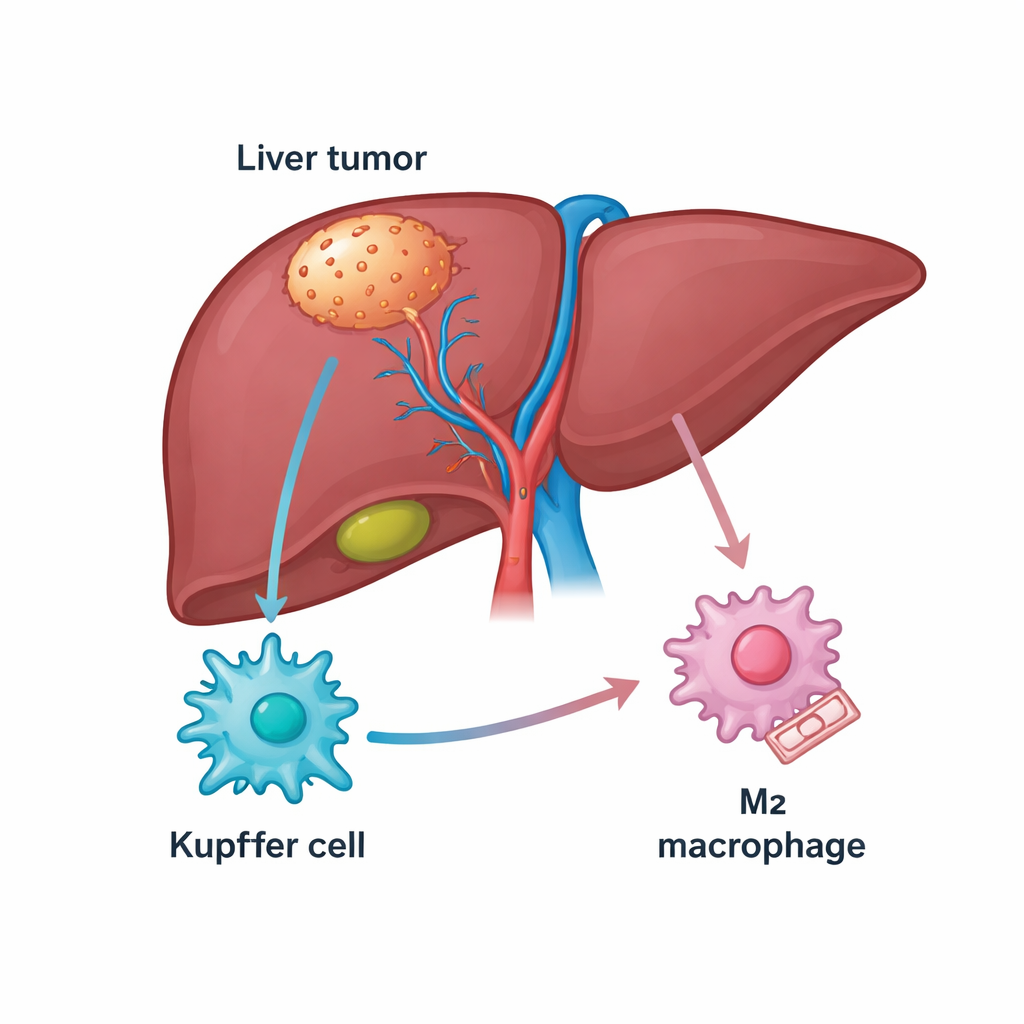
Niespodziewane białko, które skłania komórki odpornościowe do wspierania guza
TUBB3 jest najbardziej znane jako składnik mikroskopijnych „torów” wewnątrz komórek, ale powiązano je także z agresywnym przebiegiem i opornością na leki w kilku nowotworach. W niniejszym badaniu naukowcy stwierdzili, że poziomy TUBB3 były znacznie wyższe w guzach wątroby niż w przylegającej zdrowej tkance, a pacjenci z wyższą ekspresją TUBB3 mieli tendencję do krótszego przeżycia. Dzięki technikom barwienia wykazali, że TUBB3 był szczególnie wzbogacony w komórkach Kupffera wewnątrz guzów i jego obecność silnie korelowała z markerami stanu M2 sprzyjającego nowotworowi. Innymi słowy, komórki Kupffera z dużą ilością TUBB3 miały większą skłonność do zachowań tłumiących atak immunologiczny i wspierających wzrost nowotworu.
Przeprogramowanie makrofagów, by powstrzymać guzy wątroby
Aby zbadać związek przyczynowo-skutkowy, zespół zmniejszył poziomy TUBB3 w komórkach Kupffera w eksperymentach laboratoryjnych. Po wyciszeniu TUBB3 te komórki produkowały mniej sygnałów typu M2, więcej sygnałów typu M1 i wydzielały mniej cząsteczek, które normalnie tłumią aktywność układu odpornościowego. Komórki raka wątroby eksponowane na te przeprogramowane makrofagi rosły wolniej, dzieliły się rzadziej i miały mniejszą zdolność migracji oraz inwazji. U myszy mieszanie komórek raka wątroby z komórkami Kupffera pozbawionymi TUBB3 prowadziło do mniejszych guzów, większej śmierci komórek nowotworowych oraz większego napływu zabójczych limfocytów CD8 uzbrojonych w białka efektorowe. Jeśli makrofagi usunięto z organizmów całkowicie, korzyść wynikająca z blokady TUBB3 w dużej mierze znikała, co podkreśla, że efekt przebiega przez te komórki odpornościowe, a nie jedynie przez same komórki nowotworowe.
Odkrycie wewnętrznego hamulca kluczowej ścieżki sygnałowej
Badanie zbadało także mechanizm działania TUBB3. Autorzy skupili się na znanej ścieżce wzrostu i przeżycia kontrolowanej przez białka PTEN i AKT, która również kształtuje, czy makrofagi przyjmują tożsamość M1 czy M2. Stwierdzili, że obniżenie TUBB3 zwiększało PTEN, co z kolei redukowało aktywujące „znaczniki fosforanowe” na AKT, skłaniając makrofagi w kierunku stanu walczącego z guzem. Gdy sztucznie reaktywowano AKT, makrofagi powracały do wzorca M2, a komórki nowotworowe odzyskiwały agresywne zachowanie, nawet przy braku TUBB3. To umiejscowiło TUBB3 powyżej PTEN i AKT jako swego rodzaju wewnętrzny regulator zachowania makrofagów.
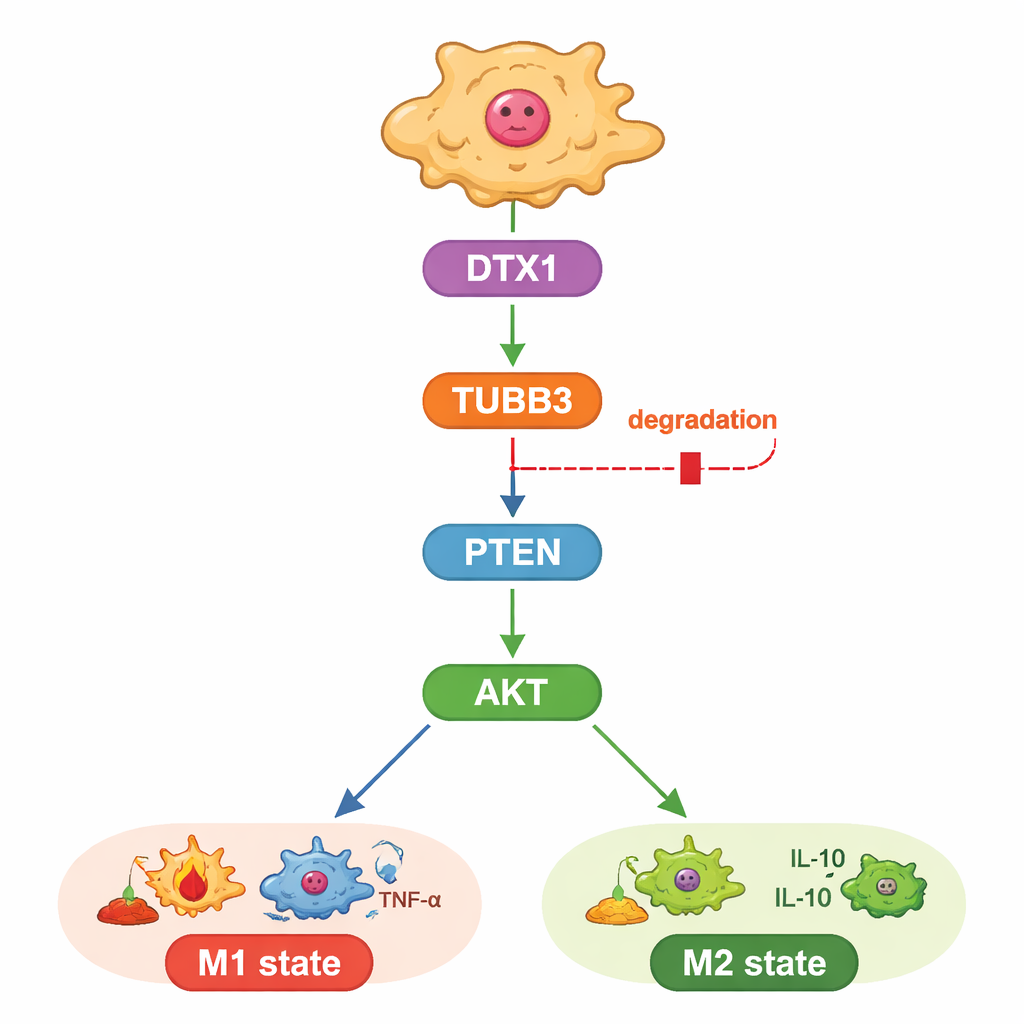
Wbudowany znacznik na śmieci, który można przywrócić
Na koniec badacze zapytali, dlaczego TUBB3 jest tak obfite w guzach wątroby. Łącząc przewidywania bioinformatyczne z danymi ekspresji, zidentyfikowali enzym DTX1, należący do rodziny znakującej białka do degradacji, jako prawdopodobnego regulatora. Poziomy DTX1 były niższe w guzach wątroby niż w zdrowej tkance i wiązały się z lepszym rokowaniem pacjentów oraz większą obecnością makrofagów typu M1. W komórkach zwiększenie DTX1 przyspieszało rozkład TUBB3, tłumiło aktywność AKT i przesuwało makrofagi w stronę stanu zwalczającego guz, hamując wzrost komórek nowotworowych. Nadpisanie tego przez ponowne wprowadzenie nadmiaru TUBB3 niwelowało korzyści płynące z DTX1, zarówno w hodowlach komórkowych, jak i w guzach myszy. Razem wyniki te rysują jasne powiązanie od DTX1 przez TUBB3 i PTEN/AKT do immunologicznego tonu guza.
Co to oznacza dla przyszłego leczenia raka wątroby
Dla osób niebędących specjalistami kluczowy wniosek jest taki, że ta praca identyfikuje wcześniej ukryty układ sterowania wewnątrz rezydentnych komórek odpornościowych wątroby, który decyduje, czy one pomagają, czy przeszkadzają w walce z rakiem. Gdy enzym znakujący do degradacji DTX1 jest niski, TUBB3 się kumuluje, ścieżka wzrostu zostaje włączona, a komórki Kupffera przesuwają się w kierunku trybu wspierającego guz, co osłabia skuteczność immunoterapii. Przywrócenie tej drogi — przez obniżenie TUBB3, zwiększenie DTX1 lub ostrożne dostrojenie sygnału PTEN/AKT — mogłoby ponownie uaktywnić miejscowe mechanizmy odpornościowe i uczynić terapie takie jak inhibitory PD-1 bardziej skutecznymi. Choć takie strategie są wciąż na etapie eksperymentalnym, podkreślają obiecujące podejście polegające na leczeniu nie tylko komórek nowotworowych, lecz także otaczających je „sąsiadów” immunologicznych, którzy silnie wpływają na zachowanie raka wątroby.
Cytowanie: Sun, J., Sun, T., Zhang, Y. et al. DTX1-mediated degradation of TUBB3 in Kupffer cells mitigates hepatocellular carcinoma progression by regulating M1/M2 polarization. Commun Biol 9, 311 (2026). https://doi.org/10.1038/s42003-026-09593-z
Słowa kluczowe: rak wątrobowokomórkowy, makrofagi związane z guzem, komórki Kupffera, immunoterapia, sygnalizacja AKT