Clear Sky Science · pl
Uszczelnianie i decorrelacja aktywności komórek ziarnistych w zakręcie zębatym przez noradrenalinę
Dlaczego zryw pobudzenia może wyostrzyć wspomnienia
Chwile, które nas wyrywają ze stanu obojętności — niemalowy unik na drodze, nieoczekiwany komentarz, zaskakujący zwrot akcji w filmie — często zapadają w pamięć znacznie lepiej niż przeciętny dzień. Badanie to wyjaśnia istotny powód: związek chemiczny mózgu powiązany z pobudzeniem, noradrenalina, subtelnie przekształca sposób, w jaki kluczowa brama pamięci w hipokampie filtruje i rozdziela doświadczenia, ułatwiając późniejsze rozróżnianie podobnych zdarzeń.
Bramkarz mózgu dla podobnych doświadczeń
W hipokampie znajduje się zakręt zębaty, region pełniący rolę bramkarza dla nowych wspomnień. Otrzymuje on obfite informacje z kory entorhinalnej — sygnały o tym, gdzie jesteśmy i co się dzieje wokół nas — i przekształca je w wzorce aktywności w komórkach ziarnistych, swoich głównych neuronach. Teoria i eksperymenty sugerują, że wzorce te muszą być „rzadkie” (aktywnych jednocześnie tylko kilka komórek) i „zdekorrelowane” (różne doświadczenia aktywują różne zestawy komórek), aby wspomnienia się nie zlewały. Nadal jednak nie było jasne, jak ta transformacja zachodzi na poziomie konkretnych komórek i obwodów.
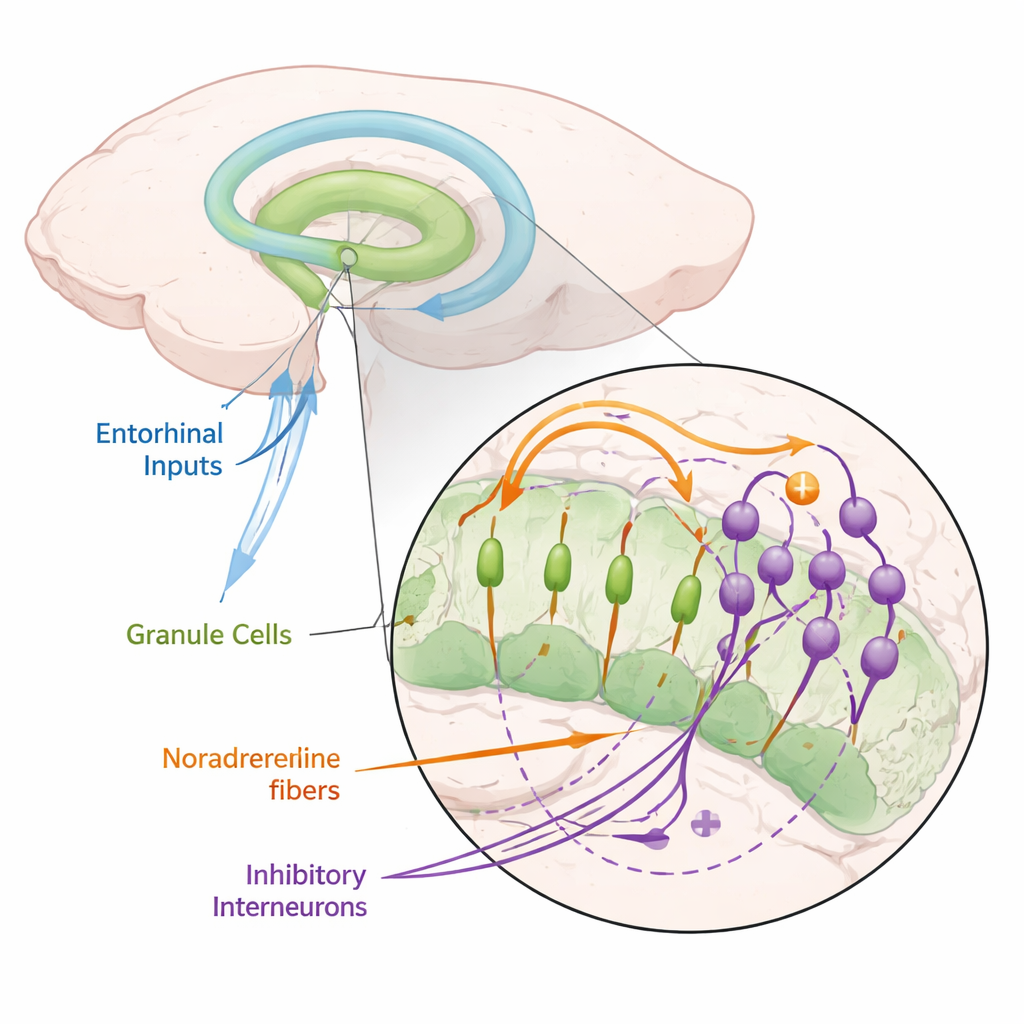
Chemiczny sygnał pobudzenia, który ucisza kluczowe komórki pamięci
Autorzy skupili się na noradrenalinie, neuromodulatorze uwalnianym przez neurony w małej części pnia mózgu zwanej jądrem sinawym (locus coeruleus), która aktywuje się podczas uwagi, nowości i stresu. Używając myszy, wyrazili w tych noradrenergicznych neuronach białka wrażliwe na światło, co pozwoliło im uwalniać noradrenalinę na żądanie przy pomocy błysków światła. Kiedy stymulowali główną drogę wejściową do zakrętu zębatego i rejestrowali odpowiedzi komórek ziarnistych, stwierdzili, że uwolnienie noradrenaliny silnie zmniejsza skłonność tych komórek do wyładowań. Tłumienie to obserwowano zarówno na poziomie pojedynczych neuronów, jak i sygnałów populacyjnych, i można było je odtworzyć przez zanurzenie preparatów w noradrenalinie. Zablokowanie receptorów noradrenaliny usuwało efekt, co dowodziło, że zależy on od tego przekaźnika chemicznego.
Nie słabsze pobudzenie, lecz silniejsze hamulce
Aby zrozumieć, w jaki sposób noradrenalina wygasza komórki ziarniste, zespół sprawdził oczywiste możliwości. Nie zmieniała ona znacząco potencjału spoczynkowego ani rezystancji wejściowej komórek ziarnistych, co oznacza, że ich podstawowa pobudliwość pozostała mniej więcej niezmieniona. Nie osłabiła też prądów pobudzających, które te komórki otrzymują z kory entorhinalnej. Zamiast tego, po zablokowaniu receptorów GABA_A, które pośredniczą w hamowaniu, noradrenalina nie była już w stanie stłumić wyładowań komórek ziarnistych. Szczegółowe pomiary prądów wykazały, że noradrenalina selektywnie wzmacniała szybką, sprzężoną z napływem formę hamowania: sygnały pobudzające najpierw napędzały grupę interneuronów, które następnie szybko hamowały komórki ziarniste, zanim te zdążyły wystrzelić. Analizy czasowe ujawniły, że ten wrażliwy na noradrenalinę prąd hamujący pojawiał się tuż po bezpośrednim pobudzeniu, ale przed wzrostem aktywności głównej populacji komórek ziarnistych — cecha charakterystyczna hamowania feedforward.
Specjalistyczne komórki hamujące, które wymuszają precyzyjne tempo
Które interneurony dostarczały tego kluczowego hamowania? Ku zaskoczeniu, komórki wyrażające parwalbuminę, uważane przez długi czas za dominujące w szybkim hamowaniu feedforward, nie były odpowiedzialne — noradrenalina wręcz zmniejszała ich aktywność. Zamiast nich kluczową rolę odgrywały interneurony wyrażające cholecystokininę (komórki CCK). Te komórki otrzymują bezpośrednie wejście z tych samych włókien korowych, które pobudzają komórki ziarniste, i wyładowują się tuż przed komórkami ziarnistymi, co wskazuje na rolę feedforward. Noradrenalina depolaryzowała komórki CCK, ułatwiając ich rekrutację, i zwiększała częstotliwość, z jaką sygnały wejściowe je wyzwalały, bez zmiany siły pojedynczych połączeń hamujących. Gdy badacze farmakologicznie zablokowali wyjście z komórek CCK, noradrenalina przestała tłumić aktywność komórek ziarnistych. W efekcie noradrenalina wzmacnia obwód komórek CCK, który narzuca bardzo wąskie okienko czasowe, w którym przychodzące impulsy pobudzające mogą skutecznie wywołać wyładowanie komórek ziarnistych.
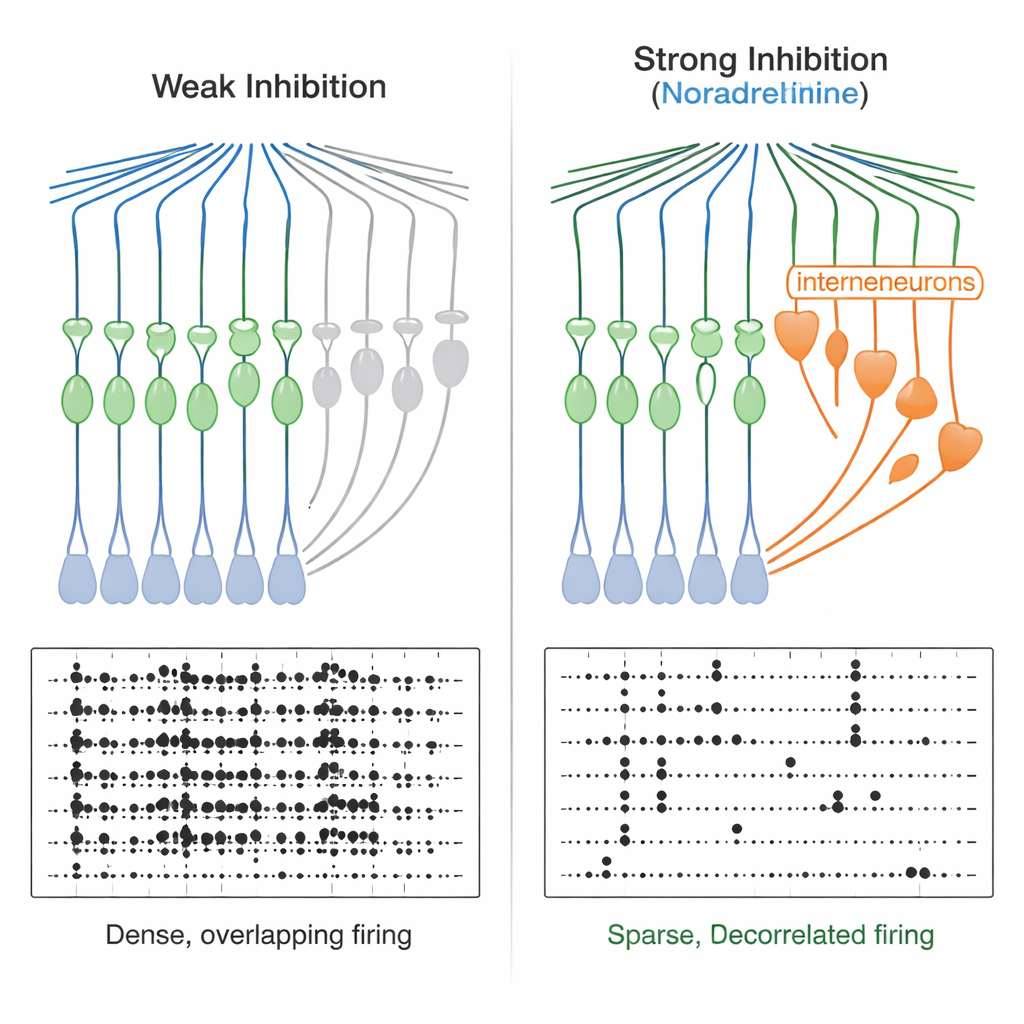
Od wąskich okienek do czyściejszych kodów pamięci
To wyostrzone tempo ma poważne konsekwencje. Gdy zespół dostarczał pary krótkich impulsów pobudzających, stwierdzili, że w normalnych warunkach komórki ziarniste potrafiły integrować impulsy rozdzielone dziesiątkami milisekund i zamieniać je w pojedyncze wyładowanie. W obecności noradrenaliny okienko to skurczyło się do kilku milisekund — komórki ziarniste reagowały niemal wyłącznie na silnie zsynchronizowane wejścia. Modele obliczeniowe sieci potwierdziły, że wzmocnienie i przyspieszenie hamowania feedforward prowadzi do rzadszego wyjścia i zmniejszenia nakładania się wzorców aktywności, poprawiając „dekorrelację”. Doświadczalnie, gdy badacze wprowadzili do zakrętu zębatego dwa podobne, ale nieidentyczne wzorce wejściowe, komórki ziarniste odpowiadały bardziej odrębnymi wzorcami wyładowań w obecności noradrenaliny, zarówno w pojedynczych rejestracjach komórkowych, jak i w obrazowaniu wapnia obejmującym wiele komórek. Jednocześnie ogólna aktywność komórek ziarnistych stawała się rzadsza.
Jak pobudzenie może pomóc oddzielić podobne wspomnienia
Dla czytelnika niebędącego specjalistą wniosek jest taki: noradrenalina, uwalniana gdy jesteśmy czujni lub emocjonalnie zaangażowani, pomaga kluczowemu filtrowi pamięci w hipokampie stać się bardziej selektywnym. Poprzez pobudzenie konkretnej klasy hamujących neuronów, zawęża ona okienko czasowe, w którym sygnały mogą wywołać komórki ziarniste, tak że przepuszczane są jedynie silnie zsynchronizowane, istotne impulsy. To zmniejsza całkowite wyładowania, zmniejsza nakładanie się wzorców aktywności i pomaga mózgowi przechowywać podobne doświadczenia — jak dwie klasy czy dwie rozmowy — jako odrębne wspomnienia zamiast rozmytej mieszaniny. Praca ujawnia konkretny mechanizm obwodowy łączący chwilowe pobudzenie z dokładniejszym, mniej podatnym na pomyłki pamiętaniem.
Cytowanie: Glovaci, I., Mihály, A., Vervaeke, K. et al. Sparsification and decorrelation of granule cell activity in the dentate gyrus by noradrenaline. Commun Biol 9, 323 (2026). https://doi.org/10.1038/s42003-026-09592-0
Słowa kluczowe: noradrenalina, zakręt zębaty, hamujące neurony wewnętrzne, separacja wzorców, pamięć epizodyczna