Clear Sky Science · pl
Wgląd strukturalny w helikazę WRN ujawnia stany konformacyjne i możliwości odkrywania leków przeciw rakowi MSI‑H
Dlaczego ma to znaczenie dla leczenia raka
Niektóre nowotwory mają wrodzoną słabość: źle naprawiają błędy w DNA. Białko zwane helikazą WRN działa jak molekularne narzędzie naprawcze, które utrzymuje przy życiu te kruche guzy. Badanie to pokazuje, w atomowym detalu, jak WRN porusza się po DNA i jak eksperymentalne leki mogą zablokować jego ruch — wskazując drogę do nowych terapii, które selektywnie zabijają te wrażliwe komórki nowotworowe, oszczędzając tkanki zdrowe.
Genetyczny majsterkowicz pod mikroskopem
Helikaza WRN jest częścią komórkowej ekipy konserwacyjnej, pomagając rozwijać DNA, aby uszkodzenia mogły zostać wykryte i naprawione. Osoby urodzone bez funkcjonującego WRN rozwijają zespół Wernera, rzadkie schorzenie charakteryzujące się przedwczesnym starzeniem, co pokazuje, jak kluczowe jest to białko dla utrzymania genomu. Guzy z „wysoką niestabilnością mikrosatelitarną” (MSI‑H) — powszechny defekt w raku jelita grubego i niektórych innych nowotworach — okazują się być szczególnie zależne od WRN. Gdy WRN zostaje wyłączone w tych komórkach, ich już chwiejne DNA szybko się rozpada, a komórki nowotworowe giną. To czyni WRN atrakcyjnym celem terapeutycznym, ale do tej pory naukowcom brakowało przejrzystego obrazu, jak białko zmienia kształt, gdy łapie DNA, zużywa paliwo chemiczne i porusza się wzdłuż materiału genetycznego.
Obserwowanie, jak WRN się wygina i „oddycha”
Autorzy użyli krystalografii rentgenowskiej, aby uchwycić kilka wysokorozdzielczych „zatrzymań” rdzenia helikazy WRN człowieka. Rozwiązywali struktury WRN samego oraz WRN związane z jednoniciowym DNA i nieulegającą rozkładowi cząsteczką przypominającą ATP. Te obrazy ujawniły, że białko zbudowane jest z dwóch głównych płatów połączonych elastycznym zawiasem, który zachowuje się jak staw „oddychający”. W stanie spoczynkowym, bez paliwa, WRN przyjmuje kompaktową, „zamkniętą” formę, w której płaty leżą blisko siebie. Gdy obecne są cząsteczki ATP‑podobne i DNA, płaty rozchylają się do bardziej „otwartej” konfiguracji, która może mieścić DNA w dodatnio naładowanym rowku. Mała aromatyczna pętla wewnątrz WRN przekształca się w krótki heliks i wkłada się między zasady DNA, działając jak zapadka, która pomaga białku stąpać naprzód bez cofania się.
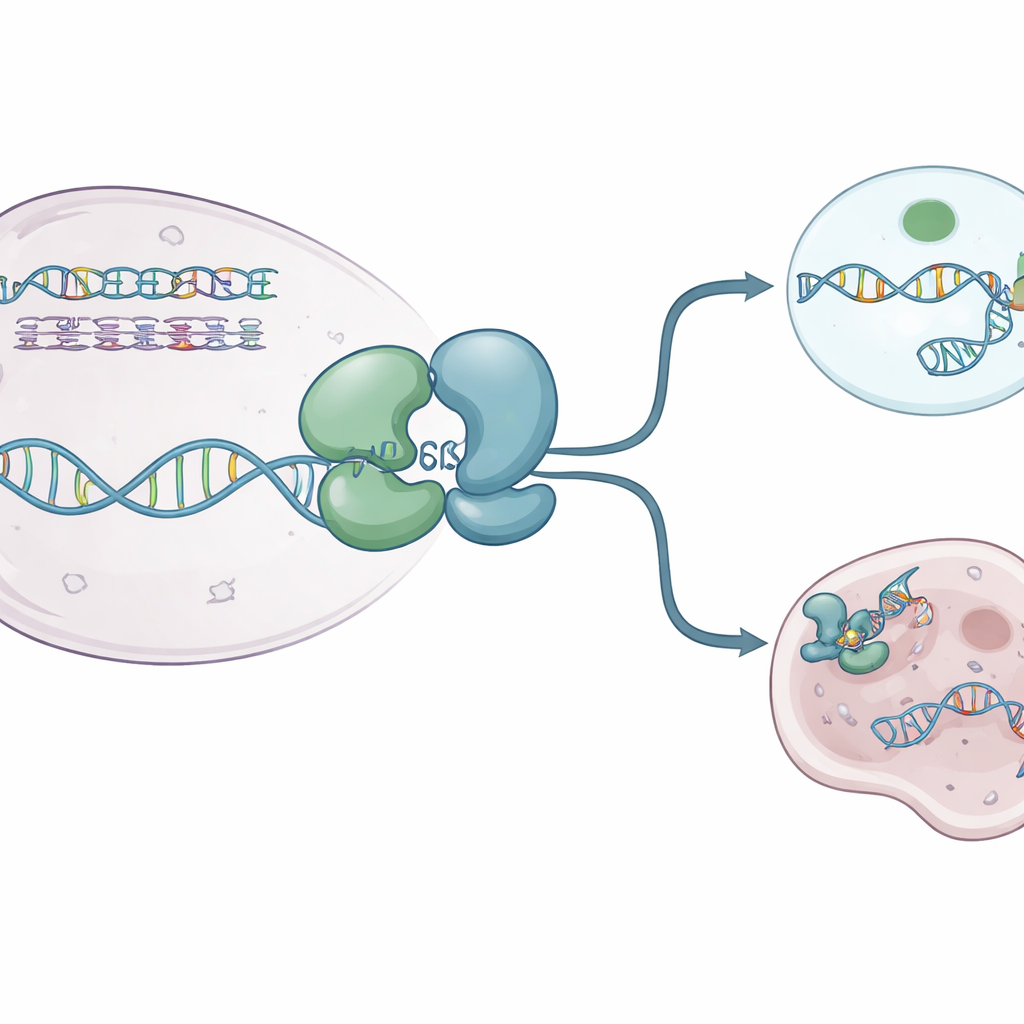
Jak obecne leki wyłączają WRN
Kilka związków blokujących WRN weszło ostatnio do badań klinicznych. Nie zatykają one bezpośrednio aktywnego rowka białka. Zamiast tego działają z dystansu, chwytając region zawiasowy i blokując WRN w kształtach, które nie mogą prawidłowo związać się z DNA. Niektóre molekuły, takie jak HRO761 i spokrewniony kandydat kliniczny z GSK, obracają jeden płat w przybliżeniu o 180 stopni względem drugiego, tworząc dramatyczną „skręconą” formę, która nie leży na DNA. Inne, w tym VVD‑133214 i blisko spokrewniony związek badany tutaj, przypinają WRN w ściśle „zamkniętym” układzie, który nie odsłania kluczowych powierzchni chwytających DNA. Doświadczenia biochemiczne potwierdziły, że po związaniu tych leków WRN nie może już tworzyć stabilnego kompleksu z jednoniciowym DNA, skutecznie odcinając związek między użyciem ATP a rozwijaniem DNA.
Jak komórki nowotworowe uczą się uciekać
Aby zobaczyć, jak guzy mogą unikać tych leków, zespół hodował komórki raka jelita grubego MSI‑H w obecności inhibitorów WRN przez tygodnie do miesięcy. Pojawiły się populacje oporne bardzo szybko. Analiza genetyczna wykazała, że w każdym przypadku komórki nabyły jedną, precyzyjną zmianę w genie WRN w pobliżu wiążącego lek zawiasu. Jedna mutacja osłabiła efekt inhibitora wywołującego „skręcony stan” HRO761, podczas gdy inna zmniejszyła wrażliwość na VVD‑133214, który faworyzuje stan zamknięty. Dodatkowo wiele komórek opornych zwiększyło produkcję WRN, dając sobie więcej kopii celu i częściowo rozcieńczając skutek leku. Odkrycia te odzwierciedlają wzorce oporności obserwowane przy innych ukierunkowanych lekach przeciwnowotworowych, gdzie drobne modyfikacje strukturalne białka docelowego lub jego nadekspresja mogą osłabić terapię.
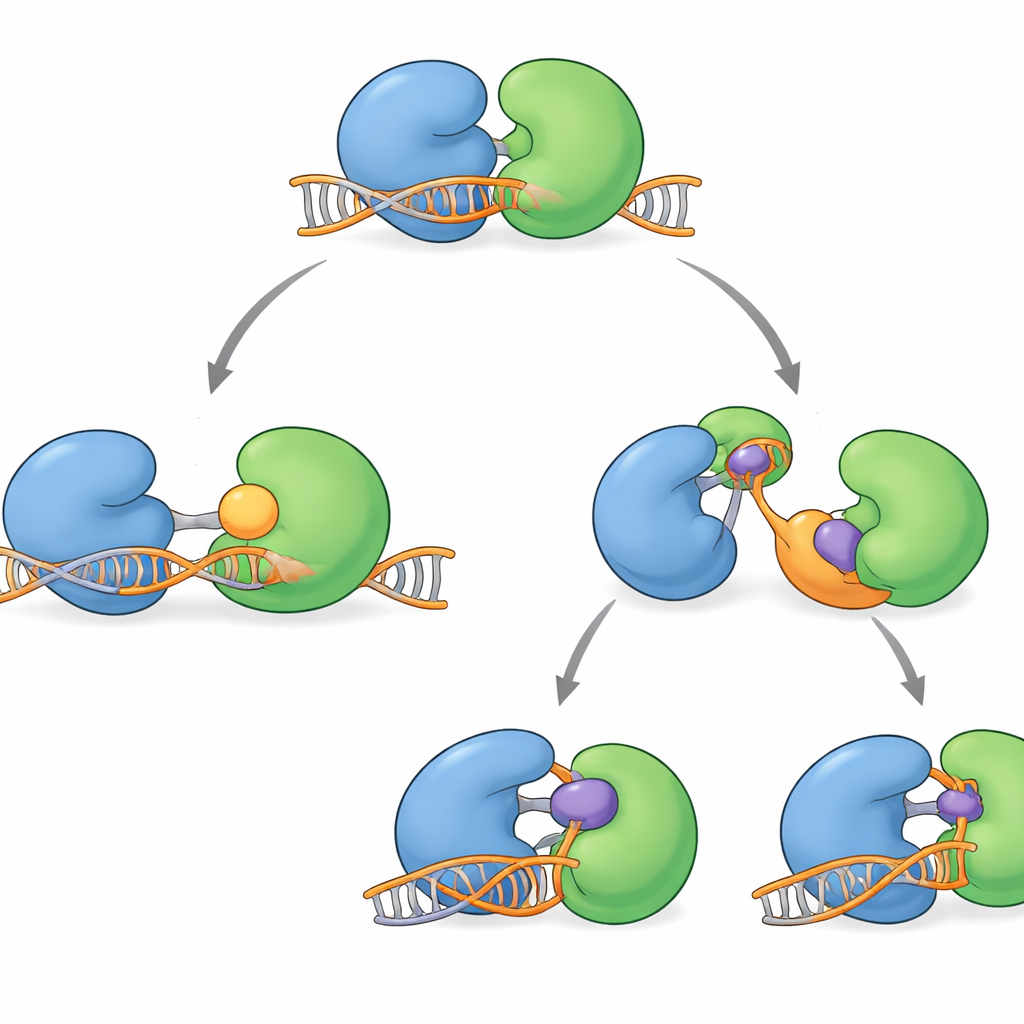
W kierunku mądrzejszych blokerów WRN
Razem nowe struktury mapują pełny cykl pracy WRN: jak przyczepia się do DNA, stawia kroki i się resetuje. Pokazują też, że dzisiejsze związki kliniczne głównie stabilizują formy białka „poza DNA”. Dla czytelnika niespecjalistycznego kluczowy punkt jest taki, że teraz rozumiemy, gdzie WRN jest podatne i jak guzy mogą się dostosować. To sugeruje kolejną falę inhibitorów, które będą wiązać WRN, gdy jest zablokowane na DNA, potencjalnie uwięziąc je w toksycznym stanie — podobnie jak skuteczne leki, które uwięziły inne enzymy naprawy DNA. Takie „on‑DNA” blokery WRN, stosowane samodzielnie lub razem z istniejącymi środkami, mogłyby zapewnić trwalsze sposoby wykorzystania ukrytej słabości nowotworów MSI‑H.
Cytowanie: Fletcher, C.T., Mornement, A.A., Barrett, C. et al. Structural insights into WRN helicase reveal conformational states and opportunities for MSI-H cancer drug discovery. Commun Biol 9, 334 (2026). https://doi.org/10.1038/s42003-026-09584-0
Słowa kluczowe: helikaza WRN, niestabilność mikrosatelitarna, naprawa DNA, inhibitory allosteryczne, oporność na leki