Clear Sky Science · pl
PiR48444 hamuje osteogeniczną różnicowanie MSC i regenerację kości przez celowanie w METTL7A/eIF4E‑zależną metylację m6A BMP2
Dlaczego małe cząsteczki mają znaczenie dla złamań
Złamania i związana z wiekiem utrata masy kostnej to powszechne problemy, a lekarze chętnie sięgają po komórki macierzyste, aby pomóc organizmowi odbudować uszkodzony szkielet. Jednak te komórki nie zawsze tworzą nową kość tak skutecznie, jak byśmy chcieli, zwłaszcza u osób starszych lub w tkankach objętych stanem zapalnym. W badaniu odkryto małą cząsteczkę RNA, nazwaną piR48444, która działa jak molekularny hamulec dla komórek tworzących kość. Usunięcie tego hamulca zwiększa naprawę kości i chroni przed utratą tkanki kostnej.
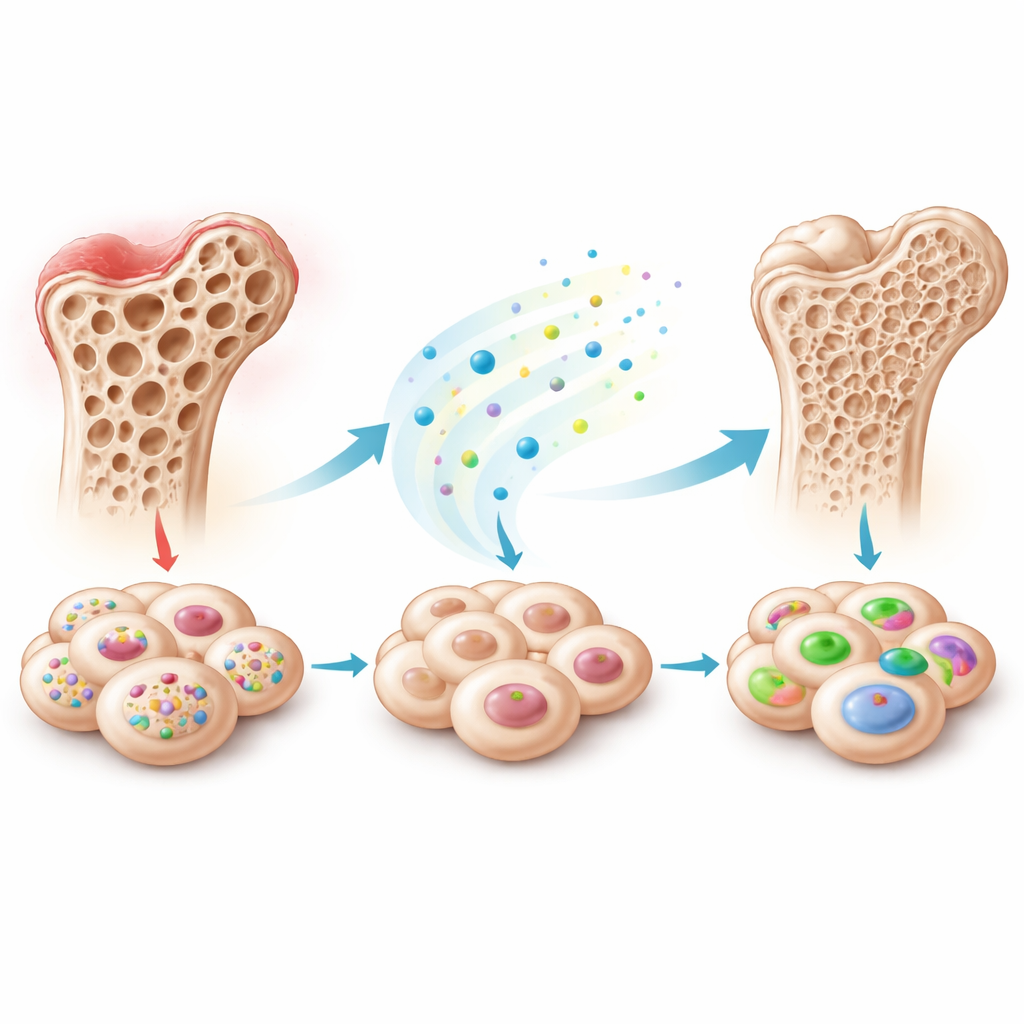
Ukryty hamulec w wielu rodzajach komórek macierzystych
Zespół skupił się na mezenchymalnych komórkach macierzystych — wszechstronnych komórkach, które mogą przekształcać się w kość, chrząstkę, tkankę tłuszczową i inne, izolowanych z wielu tkanek, takich jak szpik kostny, mleczne zęby czy tkanka tłuszczowa. Gdy w warunkach laboratoryjnych stymulowano je do różnicowania w kierunku kostnym, tysiące genów i małych RNA zmieniało aktywność. Sekwencjonując te molekuły w komórkach pochodzących z mlecznych zębów, badacze odkryli, że jedna z małych cząsteczek RNA — piR48444 — stopniowo malała w miarę przejścia komórek w kierunku kostnym. Sprawdzili następnie inne typy komórek macierzystych i zaobserwowali ten sam wzorzec: komórki tworzące więcej kości miały mniej piR48444, co sugeruje, że ta molekuła normalnie ogranicza ich zdolność do tworzenia tkanki kostnej.
Z naczyń do żywych kości
Aby sprawdzić tę hipotezę, naukowcy zmienili poziom piR48444 w kilku typach komórek macierzystych. Gdy zmniejszyli ilość piR48444, komórki odkładały więcej wapnia, włączały geny powiązane z kością i pod mikroskopem przypominały niedojrzałą tkankę kostną. Z kolei zwiększenie poziomu piR48444 przyniosło efekt przeciwny: aktywność związana z kością spadła. Zespół przeszedł następnie do modeli zwierzęcych. Komórki z wyłączonym piR48444 wykorzystano do wypełnienia małych ubytków czaszki u myszy. Zmodyfikowane komórki wytworzyły znacznie więcej nowej tkanki kostnej niż komórki kontrolne, co potwierdziły trójwymiarowe skany rentgenowskie i barwienia tkanek, sugerując, że blokada piR48444 może istotnie poprawić naprawę kości in vivo.
Ochrona kruchych kości w chorobach i starzeniu
Utrata masy kostnej wynika nie tylko z urazów, lecz także ze stanu zapalnego i procesu starzenia. W mezenchymalnych komórkach szpiku wystawionych na toksyny bakteryjne oraz w komórkach macierzystych pochodzących od starszych zwierząt poziomy piR48444 były nietypowo wysokie, podczas gdy markery tworzenia kości były niskie. Badacze opracowali „antagomir” — krótką cząsteczkę zaprojektowaną do neutralizacji piR48444 w krwioobiegu — i wstrzyknęli ją myszom z utratą kości wywołaną stanem zapalnym oraz myszom naturalnie starym. W obu modelach zwierzęta leczone zachowały znacznie więcej gąbczastej, wewnętrznej tkanki kostnej, o większej gęstości i liczbie drobnych beleczek kostnych, podczas gdy twarda zewnętrzna powłoka kości pozostała bez zmian. To wskazuje, że blokada piR48444 może selektywnie chronić delikatną, metabolicznie aktywną część szkieletu najbardziej narażoną podczas starzenia i przewlekłego zapalenia.
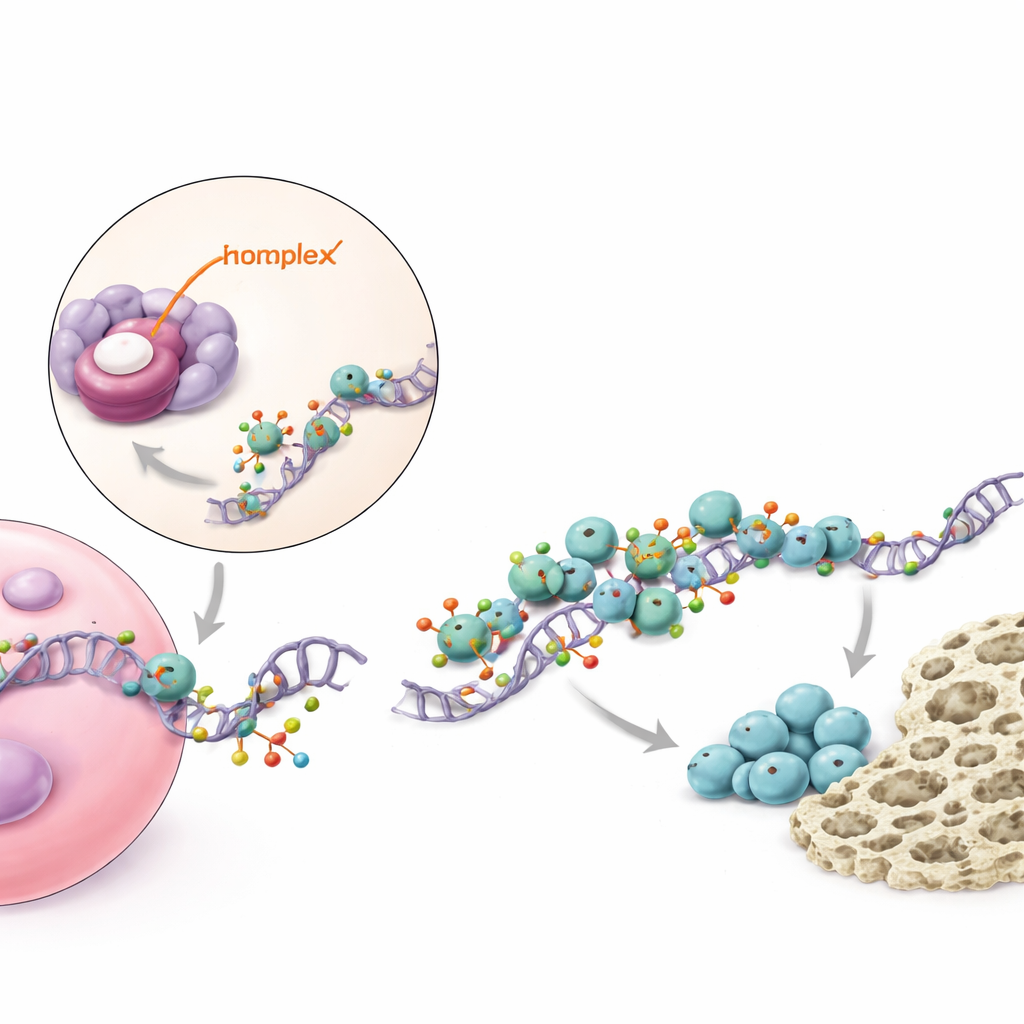
Molekularne przekaźnictwo wzmacniające kluczowy sygnał kostny
Doprecyzowując mechanizm, badanie zmapowało, jak piR48444 działa wewnątrz komórek. Małe RNA wiąże się i hamuje białko o nazwie METTL7A, które działa jako enzym modyfikujący cząsteczki mRNA niosące instrukcję dla BMP2 — znanego czynnika wzrostu silnie wspierającego tworzenie kości. METTL7A dodaje niewielkie chemiczne znaczniki do mRNA BMP2, stabilizując je i ułatwiając maszynie komórkowej do produkcji białek ich odczyt. METTL7A współdziała także z innym białkiem, eIF4E, które pomaga inicjować syntezę białek. Gdy piR48444 jest obficie obecne, METTL7A jest tłumione, mniej mRNA BMP2 otrzymuje znaczniki i jest tłumaczonych, w efekcie powstaje mniej białka BMP2, więc komórki rzadziej przechodzą w kierunku kostnienia. Gdy piR48444 jest zablokowane, poziomy METTL7A i BMP2 rosną, skłaniając komórki do tworzenia kości.
Co to oznacza dla przyszłej naprawy kości
Mówiąc prosto, autorzy ujawniają łańcuch kontroli, w którym małe RNA (piR48444) tłumi enzym pomocniczy (METTL7A), a ten z kolei ogranicza silny sygnał budujący kość (BMP2). Przerywając ten łańcuch na poziomie piR48444, można zwiększyć zdolność różnych komórek macierzystych do tworzenia kości i zmniejszyć utratę masy kostnej u myszy. Chociaż bezpieczeństwo, efekty poza celem i długoterminowe konsekwencje wymagają dalszych badań, praca wskazuje na piR48444 jako potencjalny marker krwiowy ryzyka osteoporozy oraz obiecujący cel dla leków mających poprawić regenerację kości opartą na komórkach macierzystych w praktyce klinicznej.
Cytowanie: Zheng, Z., Li, X., Qin, W. et al. PiR48444 inhibits MSC osteogenic differentiation and bone regeneration via targeting METTL7A/eIF4E-mediated BMP2 m6A methylation. Commun Biol 9, 337 (2026). https://doi.org/10.1038/s42003-026-09583-1
Słowa kluczowe: regeneracja kości, mezenchymalne komórki macierzyste, osteoporoza, RNA niekodujące, sygnalizacja BMP2