Clear Sky Science · pl
Lokalne zaciskanie kationów zniekształca i zmiękcza dupleks RNA
Dlaczego ten drobny skręt RNA ma znaczenie
Wewnątrz każdej komórki DNA i RNA są nieustannie zginane, rozciągane i skręcane, gdy przechowują i wykorzystują informację genetyczną. Te ruchy to nie tylko mechaniczne detale — kontrolują, jak odczytywane są geny, jak wirusy się replikują oraz jak będą działać nowe leki i nanourządzenia oparte na RNA. Badanie pokazuje, że proste sole złożone z jonów dodatnich i ujemnych mogą radykalnie zmieniać, jak sztywny lub elastyczny jest RNA, i że RNA reaguje zupełnie inaczej niż DNA. Zrozumienie tego subtelnego tańca „zmiękczania i usztywniania” może pomóc naukowcom lepiej projektować leki RNA, szczepionki i narzędzia molekularne.
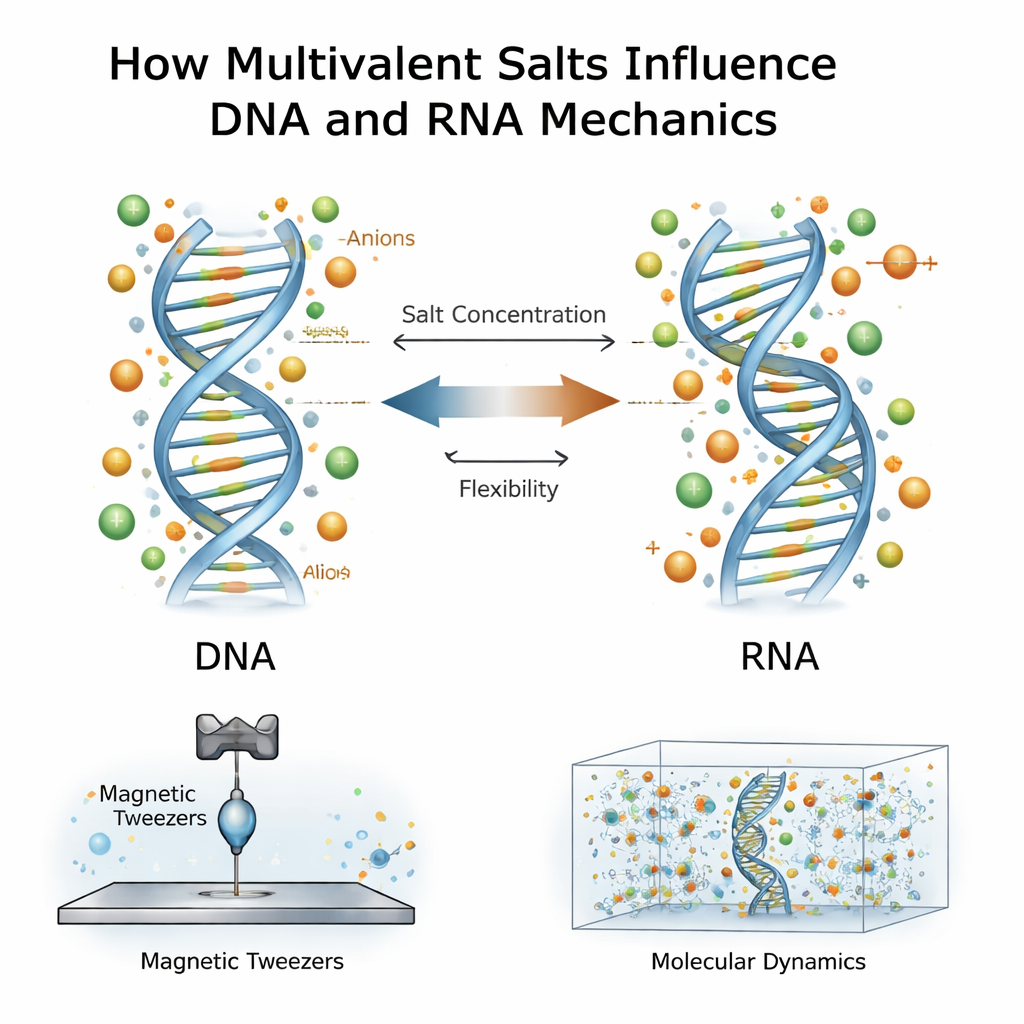
Słone otoczenie i cząsteczki genetyczne
DNA i RNA niosą silny ładunek ujemny, dlatego w wodnym środowisku otaczają je chmury jonów o przeciwnym ładunku. Większość wcześniejszych prac koncentrowała się na jonach dodatnich, zwłaszcza wielowartościowych, które niosą dwa lub trzy ładunki dodatnie, takich jak magnez czy spermidyna. Wiadomo, że jony te spajają nici DNA, kondensują je lub zmieniają ich podatność na zginanie. RNA, choć chemicznie podobne do DNA, zachowuje się inaczej: zwykle trudniej je zgiąć, ale łatwiej rozciągnąć. Nowa praca stawia głębsze pytanie: co się dzieje, gdy zarówno jony dodatnie, jak i towarzyszące im jony ujemne — aniony — oddziałują z DNA i RNA przy bardzo wysokich stężeniach soli, znacznie wyższych niż typowe w komórkach?
Sięgając po pojedyncze molekuły, by zmierzyć sztywność
Naukowcy użyli techniki zwanej pęsetami magnetycznymi, aby rozciągać pojedyncze podwójne helisy DNA lub RNA, po jednej naraz. Każda cząsteczka była przymocowana jednym końcem do szklanej powierzchni, a drugim do maleńkiej magnetycznej kulki. Przesuwając magnesy nad próbką, mogli wywierać kontrolowane siły i rejestrować, jak daleko każda cząsteczka się wydłużała i jak skręcała pod napięciem. Z krzywych siła–wydłużenie wyciągali cztery kluczowe cechy mechaniczne: jak trudno jest cząsteczce się zgiąć, jak trudno ją rozciągnąć, jej efektywną długość na parę zasad oraz jak skręcanie wpływa na wydłużenie. Powtarzali te pomiary dla szerokiego zakresu stężeń jonów wielowartościowych dla kilku różnych soli, w tym spermidyny i chlorku wapnia.
DNA znów się usztywnia, ale RNA nagle mięknie
W przypadku DNA zachowanie w dużej mierze zgadzało się z oczekiwaniami. Wraz ze wzrostem stężenia dodatnich jonów wielowartościowych DNA najpierw stawało się łatwiejsze do zgięcia — jego sztywność malała — ponieważ jony neutralizowały ładunek ujemny. Przy jeszcze wyższych stężeniach nadmiar jonów dodatnich nadkompensował, skutecznie odwracając ładunek netto DNA. Ta „inwersja ładunku” sprawiała, że DNA znów stawało się trudniejsze do zgięcia, więc jego sztywność rosła. Zaskakująco, RNA wykazało przeciwny i bardziej dramatyczny wzorzec. Przy niskich i umiarkowanych stężeniach sztywność zginania rosła: dupleks RNA prostował się i stawał się bardziej sztywny. Jednak przy bardzo wysokich stężeniach sztywność zginania RNA spadła o ponad połowę, a inne właściwości, takie jak rozciągliwość i zależność skręcania od wydłużenia, odwróciły się w nieoczekiwany sposób.
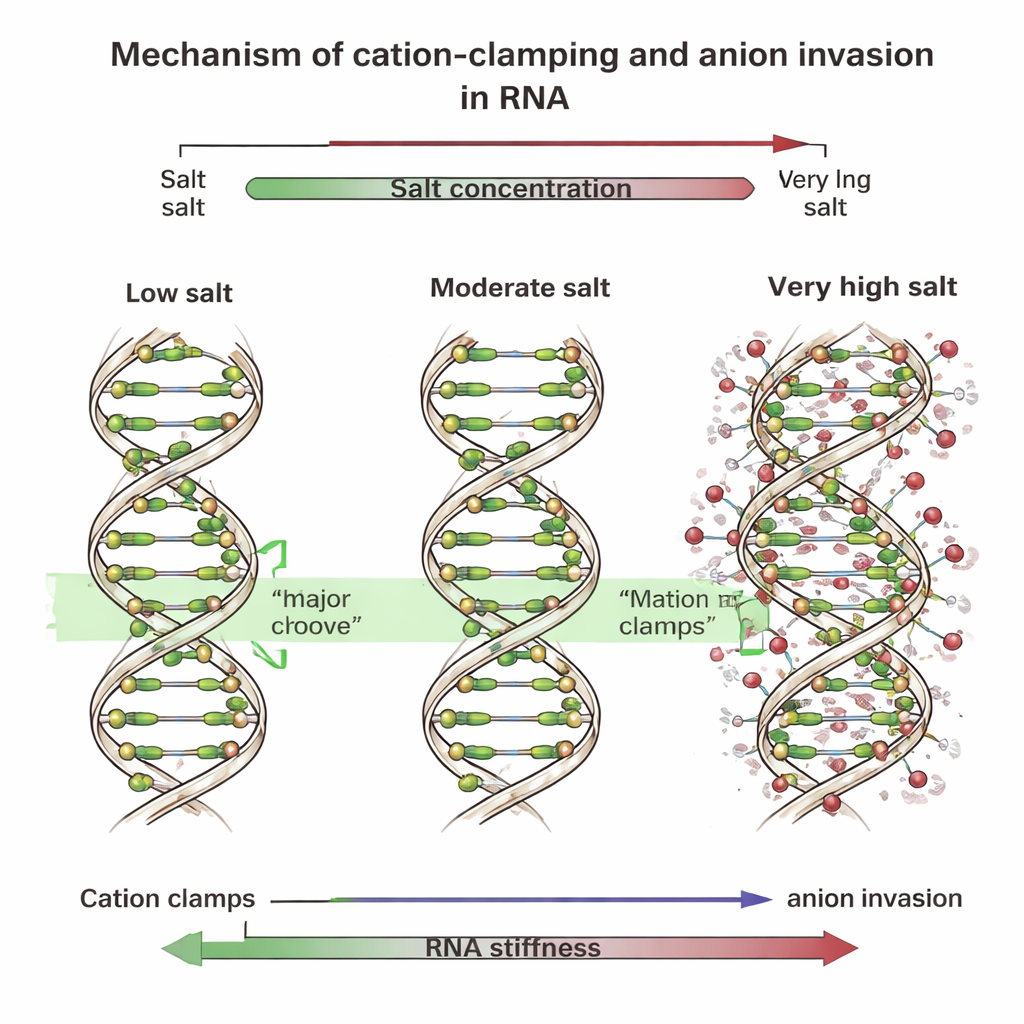
Zaciski, rowki i najeżdżające jony
Aby odkryć przyczynę, zespół przeprowadził szczegółowe symulacje komputerowe śledzące każdy atom krótkich fragmentów DNA i RNA w słonej wodzie. Symulacje ujawniły, że przy niskich i umiarkowanych stężeniach wielowartościowe jony dodatnie osadzają się w szerokim obszarze na RNA zwanym rowkiem głównym (major groove). Tworzą tam „zaciski kationowe”, które mostkują przeciwległe ściany rowka, ściągając je ku sobie, prostując helisę i zwiększając jej sztywność. DNA, którego rowki mają inną geometrię, wiąże te jony głównie wzdłuż zewnętrznego szkieletu. Przy bardzo wysokich stężeniach jednak wiele jonów ujemnych — na przykład chlorkowych — wpycha się blisko rusztowania RNA, a nawet w obręb rowka głównego. Ich obecność zaburza uporządkowane zaciski, rozpadając je na nieregularne, łatające się „lokalne zaciski”, które zniekształcają helisę. Gdy badacze naśladowali ten efekt, dodając w symulacjach sztuczne sprężyny lub lokując dodatkowe jony ujemne blisko RNA, szkielet RNA bardziej się wyginał, a jego ogólna sztywność gwałtownie spadała, dokładnie tak jak zaobserwowano w eksperymentach.
Co to oznacza dla przyszłych technologii RNA
Mówiąc wprost, badanie pokazuje, że RNA można uczynić albo prostszym i bardziej sztywnym, albo bardziej załamanym i elastycznym, po prostu zmieniając rodzaj i stężenie otaczających soli. Przy umiarkowanych poziomach jonów wielowartościowych ładunki dodatnie schludnie zaciskają zewnętrzną powierzchnię RNA i ją wzmacniają; przy ekstremalnych poziomach najeżdżające jony ujemne łamią to jednolite podparcie i tworzą zdeformowane, miękkie regiony. DNA nie wykazuje tak ostrego zmiękczenia, ponieważ wiąże jony w inny sposób i doświadcza odwrócenia ładunku netto. Te spostrzeżenia podkreślają, że nie tylko jony dodatnie, lecz także ich partnerzy ujemni są kluczowi dla kontrolowania kształtu RNA. Ta wiedza pomoże badaczom celowo stroić mechanikę RNA w laboratorium — na przykład stabilizować leki RNA, kontrolować sposób, w jaki RNA fałduje się w biosensorach, czy projektować bardziej niezawodne nanostruktury oparte na RNA.
Cytowanie: Zhang, C., Dong, HL., Zhang, JH. et al. Local cation-clamping distorts and softens RNA duplex. Commun Biol 9, 308 (2026). https://doi.org/10.1038/s42003-026-09580-4
Słowa kluczowe: mechanika RNA, jony wielowartościowe, zaciskanie kationów, DNA kontra RNA, efekty soli