Clear Sky Science · pl
CISH — kluczowy wewnątrzkomórkowy hamulec, w porównaniu i w połączeniu z istniejącymi i nowymi punktami kontrolnymi immunologicznymi w onkologii
Uwalnianie hamulców komórek walczących z rakiem
Immunoterapie nowotworowe zmieniły perspektywy wielu pacjentów, ale znaczna część osób nadal odnosi małe lub żadne korzyści. To badanie bada nowy sposób wzmocnienia własnych limfocytów T — „egzekutorów” układu odpornościowego — przez wyłączenie wewnętrznego „hamulca” nazwanego CISH. W przeciwieństwie do obecnych leków działających na przełączniki na powierzchni komórki, ta strategia celuje w system kontrolny zanurzony wewnątrz komórki, z celem uczynienia zaprojektowanych limfocytów T znacznie lepszymi w odnajdywaniu i niszczeniu guzów, nawet gdy nowotwory próbują się ukrywać.
Nowy rodzaj immunologicznego hamulca
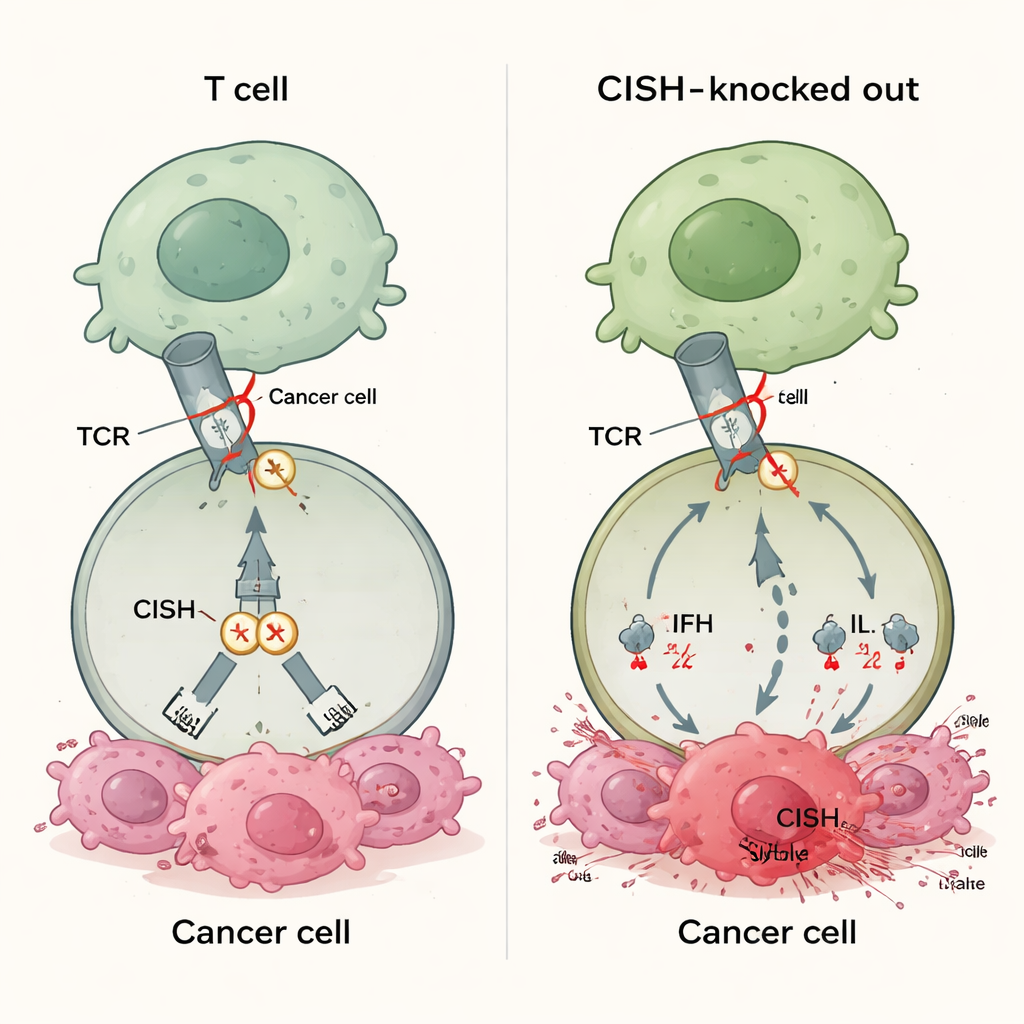
Większość zatwierdzonych leków immunoterapeutycznych blokuje białka takie jak PD-1 na powierzchni limfocytów T. Leki te działają tylko wtedy, gdy guzy wykazują dopasowane cząsteczki partnerów, jak PD-L1, a wiele nowotworów albo nigdy nie eksponuje wystarczających ilości tych partnerów, albo traci je w czasie. To pomaga wyjaśnić, dlaczego 30–60% pacjentów nie reaguje na dzisiejsze terapie blokujące punkty kontrolne. CISH należy do innej klasy hamulców, które znajdują się wewnątrz limfocytu T. Jest włączany, gdy receptor T komórki wykryje cel, a następnie tłumi sygnał poprzez promowanie degradacji kluczowego białka sygnałowego. Ponieważ ta czynność nie zależy od ligandów eksponowanych przez nowotwór, wyłączenie CISH mogłoby zasadniczo zwiększyć odpowiedzi limfocytów T w różnych typach nowotworów, niezależnie od statusu PD-L1 czy innych biomarkerów.
W bezpośrednim starciu z istniejącymi punktami kontrolnymi
Naukowcy użyli edycji genów CRISPR do usunięcia CISH i porównali powstałe limfocyty T z komórkami pozbawionymi PD-1 lub kilku innych wewnątrzkomórkowych hamulców. Kiedy stymulowali limfocyty T słabo — sytuacja mająca naśladować guzy eksponujące tylko niewielkie ilości antygenu — komórki z usuniętym CISH produkowały znacznie więcej kluczowych przekaźników immunologicznych, w tym interferonu gamma, TNF-alfa i IL-2. Komórki te były również bardziej „polifunkcjonalne”, co oznacza, że pojedyncze limfocyty T mogły wykonywać kilka zadań jednocześnie — cecha silnej aktywności przeciwnowotworowej. Dla porównania, samo usunięcie PD-1 nie pomagało w tych warunkach niskiego sygnału. W wielu testach utrata CISH silniej zwiększała aktywację, zdolność do zabijania i tworzenie trwałych, pamięciopodobnych limfocytów T niż wyłączanie innych kandydatów wewnątrzkomórkowych punktów kontrolnych, takich jak RASA2, CBLB, SOCS1, REGNASE1, HPK1 czy PTPN1/2.
Współdziałanie z innymi wewnętrznymi przełącznikami
Ponieważ sygnalizacja limfocytów T jest kontrolowana przez wiele nakładających się szlaków, zespół zapytał, czy połączenie usunięcia CISH z usunięciem innych hamulców może dać korzyści addytywne. Przy użyciu wielokrotnej edycji CRISPR odkryli, że usunięcie CISH wraz z SOCS1, HPK1 lub RASA2 dodatkowo zwiększało produkcję korzystnych cytokin przy słabej stymulacji. W modelu guza opartym na powszechnej mutacji KRAS, limfocyty T zaprojektowane z receptorem specyficznym dla KRAS były lepsze w zabijaniu komórek nowotworowych po usunięciu CISH, a efekt ten nasilał się, gdy utracie CISH towarzyszyło usunięcie SOCS1 lub RASA2. Wyniki te sugerują, że CISH kontroluje nieredundantny węzeł w biologii limfocytu T i może współpracować z wybranymi partnerami, by wyostrzyć zabijanie specyficzne dla guza.
Uodpornianie komórek CAR-T na podstępne guzy
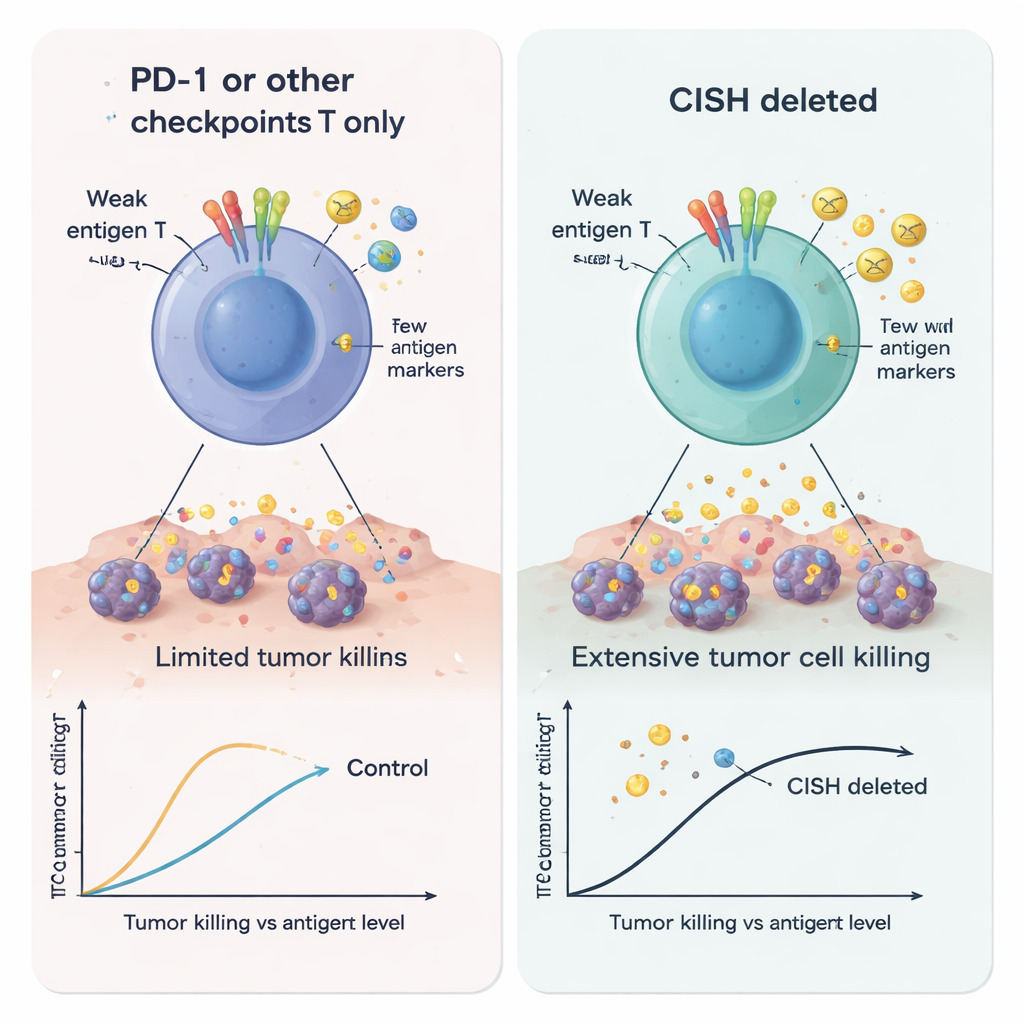
Autorzy zwrócili się następnie ku ustawieniu klinicznie istotnemu: komórkom CAR-T celującym w marker limfocytów B, CD19. Stworzyli komórki białaczkowe eksprymujące różne poziomy CD19, by naśladować guzy, które pozbywają się lub redukują swoje cele, by uciec przed terapią. Komórki CAR-T pozbawione CISH były zdecydowanie lepsze w niszczeniu komórek nowotworowych, nawet gdy CD19 było rzadkie, i wydzielały więcej sygnałów aktywujących i rekrutujących. Jednocześnie wydzielały mniejsze ilości cząsteczek znanych z osłabiania limfocytów T lub promowania wzrostu guza, takich jak Galektyna-1, Galektyna-3, rozpuszczalny 4-1BB, IL-1α oraz glikoproteina EMMPRIN/CD147. Te zmiany razem wskazują na bardziej agresywną, trudniej tłumioną komórkę CAR-T, szczególnie dobrze przystosowaną do wrogiego środowiska guza o niskiej ekspresji antygenu.
Od ławy laboratoryjnej do pacjentów
Ponad probówkami i naczyniami hodowlanymi, pomysł celowania w CISH już trafił do pacjentów. Pierwsze badanie u ludzi z użyciem naciekających nowotwór limfocytów, edytowanych w celu usunięcia CISH u osoby z zaawansowanym rakiem jelita grubego, przyniosło całkowitą odpowiedź, która utrzymuje się od ponad dwóch lat, pomimo oporności raka na liczne wcześniejsze terapie. Pokazując, że CISH jest potężnym, potencjalnie podatnym na leczenie wewnątrzkomórkowym punktem kontrolnym, który zwiększa wrażliwość limfocytów T nawet na słabe sygnały guza, to badanie pomaga wyjaśnić ten niezwykły wynik kliniczny i wspiera wysiłki nad rozwojem przyszłych terapii — czy to komórek z edytowanym genomem, czy leków doustnych — które bezpiecznie poluzują ten wewnętrzny hamulec i poszerzą zasięg immunoterapii przeciwnowotworowej.
Cytowanie: Cano, F., Bravo-Blas, A., Colombe, M. et al. CISH, a key intracellular checkpoint, in comparison and combination to existing and emerging cancer immune checkpoints. Commun Biol 9, 319 (2026). https://doi.org/10.1038/s42003-026-09579-x
Słowa kluczowe: immunoterapia nowotworów, limfocyty T, terapia CAR-T, punkty kontrolne układu odpornościowego, edycja genów CRISPR