Clear Sky Science · pl
Patogenna mutacja w α‑SNAP osłabia wiązanie z lipidami błonowymi przez ukrycie istotnej hydrofobowej pętli
Jak drobna zmiana w białku może zaburzyć rozwój mózgu
Komórki naszego mózgu nieustannie transportują ładunki w małych pęcherzykach, a białko pomocnicze o nazwie alpha‑SNAP odgrywa kluczową rolę w realizacji tych dostaw. Rzadka mutacja w alpha‑SNAP, znana z linii myszy „hyh”, powoduje poważne zaburzenia w formowaniu mózgu i równowadze płynów. W tym badaniu postawiono pozornie proste, lecz istotne pytanie: czy ta jedna zmiana w alpha‑SNAP uniemożliwia mu przyłączanie się do błon komórkowych i czy może to być istotny powód, dla którego rozwój mózgu przebiega nieprawidłowo?
Komórkowy pracownik portowy o wielu zadaniach
Alpha‑SNAP zwykle działa jak pracownik portowy dla pęcherzyków, pomagając im zlewać się z błonami komórkowymi, dzięki czemu ładunek może zostać uwolniony lub poddany recyklingowi. Współdziała z zestawem białek zwanych SNARE oraz maszyną zużywającą energię, NSF, które zbliżają błony, a potem resetują system przed kolejną rundą. Poza tą klasyczną rolą alpha‑SNAP pomaga też kontrolować procesy takie jak autofagia (samozamiatanie komórkowe), śmierć komórkowa, napływ wapnia i wykrywanie stanu energetycznego. Wszystkie te funkcje zależą, w mniejszym lub większym stopniu, od zdolności alpha‑SNAP do stykania się i częściowego wszczepiania w oleistą powierzchnię błon.
Ukryta pętla i problematyczna mutacja
Wcześniejsze prace wykazały, że alpha‑SNAP używa krótkiej, tłustej „pętli” blisko jednego z końców białka, by zaczepiać się o błony. W zdrowym białku ta pętla wystaje i może zanurzyć się w zewnętrznej warstwie błony. W myszy hyh pojedynczy element budulcowy na pozycji 105 zostaje zamieniony, tworząc mutację M105I. Autorzy zastosowali symulacje komputerowe, aby zobaczyć, jak ta zmiana wpływa na kształt białka. Stwierdzili, że białko zmutowane staje się nieco bardziej zwarte i zakrzywia się tak, że hydrofobowa pętla chowa się do wnętrza, z dala od wody i błon. W rezultacie mutant podchodzi do błon pod płytszym kątem i częściej naciska na nie mniej „lepkim” fragmentem, skracając zarówno czas kontaktu, jak i głębokość zanurzenia. Obliczenia energii wiązania to potwierdziły: białko typu dzikiego osiągało stan niskoenergetyczny, silnie związany, podczas gdy mutant preferował słabsze, płytkie kontakty.
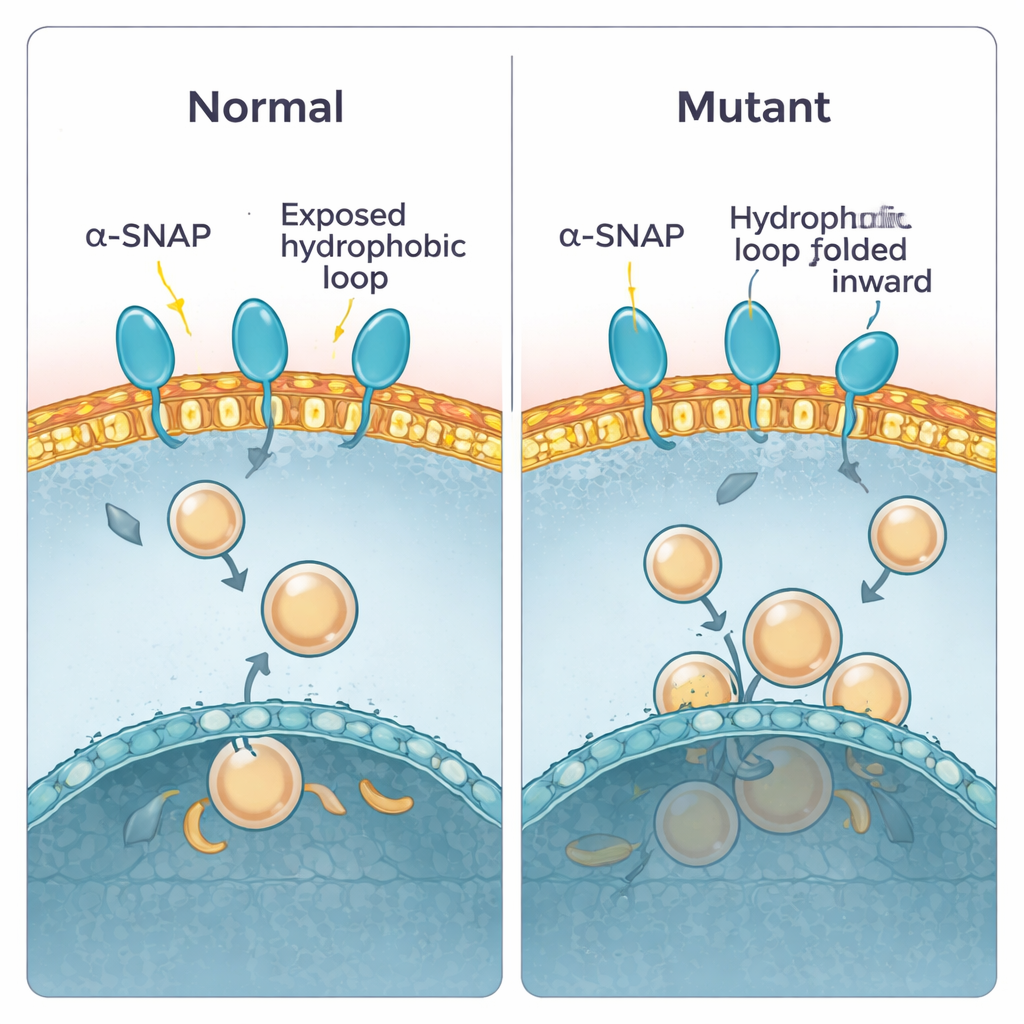
Weryfikacja przewidywań w laboratorium
Aby sprawdzić te przewidywania, zespół wyczyścił zarówno normalne, jak i zmutowane alpha‑SNAP i przetestował ich zachowanie w różnych układach eksperymentalnych. Najpierw użyto detergentu, który rozdziela się na fazę wodną i oleistą, imitując wybór między wodą a błoną. Normalne alpha‑SNAP dzieliło się równomiernie, zgodnie z balansem powierzchni częściowo hydrofobowej. Wersja zmutowana była mniej skłonna do wejścia w fazę oleistą, co sugeruje, że jej tłuste fragmenty są rzeczywiście bardziej ukryte. Następnie pozwolono białkom oddziaływać z płaskimi „arkuszami” błony plazmatycznej przygotowanymi z komórek i obrazowano liczbę miejsc wiązania. Ponownie, normalne alpha‑SNAP punktowało błonę, podczas gdy mutant wiązał się znacznie słabiej. Wreszcie unoszono sztuczne bańki błonowe (liposomy) z lipidów mózgowych przez gradienty cukrowe. Białko typu dzikiego unosiło się razem z pęcherzykami bogatymi w lipidy błony plazmatycznej, natomiast mutant zostawał w tyle, wiążąc się słabo, chyba że pęcherzyki zrobiono z innego, bardziej wewnętrznego składu błonowego.
Konsekwencje w rozwijającym się mózgu
Naukowcy zwrócili się następnie do mózgów rozwijających się zarodków mysich, koncentrując się na etapie, gdy rodzą się nowe neurony. Poprzez rozdzielenie zawartości komórek na puli rozpuszczalne i związane z błoną wykazali, że całkowity poziom alpha‑SNAP był już obniżony w mózgach hyh, ale co ważniejsze, ułamek przyłączony do błon był proporcjonalnie znacznie niższy w porównaniu z myszami kontrolnymi. Po dalszym rozdziale różnych typów błon okazało się, że największe straty dotyczyły błony plazmatycznej — zewnętrznej powierzchni komórki — podczas gdy błony wewnętrzne były znacznie mniej dotknięte. Mikroskopia potwierdziła te obserwacje: w tkance kontrolnej alpha‑SNAP obrysowywało komórki wzorem plastra miodu odpowiadającym znanemu markerowi powierzchniowemu. W mózgach hyh ten wyraźny obrys zanikał, zastępowany bardziej rozproszonym, wewnętrznym rozświetleniem, wskazując, że zmutowane białko nie utrzymuje się przy krawędzi komórki, gdzie fuzja pęcherzyków i sygnalizacja są najbardziej aktywne.
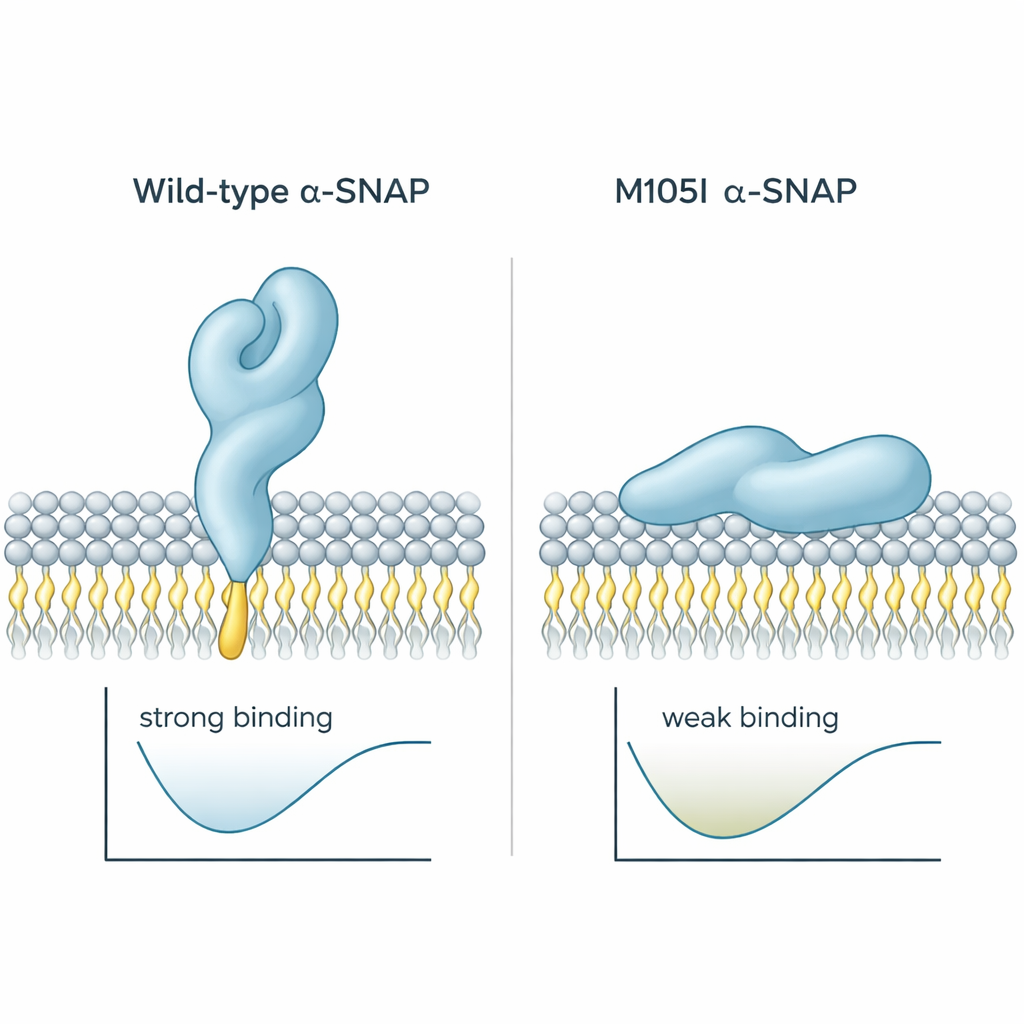
Dlaczego to ma znaczenie dla choroby
Podsumowując, praca pokazuje, że mutacja M105I robi więcej niż tylko obniża ilość alpha‑SNAP; zmienia sfałdowanie białka tak, że jego kluczowa, chwytająca błonę pętla zostaje ukryta. Utrudnia to alpha‑SNAPowi przyczepienie się do błony plazmatycznej i przyjęcie prawidłowej orientacji do organizowania aparatu fuzji. W rozwijającym się mózgu, gdzie precyzyjne dostarczanie sygnałów i materiałów budulcowych na powierzchnię komórki jest niezbędne, ta subtelna wada strukturalna prawdopodobnie przyczynia się do wodogłowia, nieprawidłowego okablowania kory i innych defektów obserwowanych u myszy hyh. Dla osób niebędących specjalistami przekaz jest jasny: nawet drobna zmiana kształtu pojedynczego białka może przekształcić sposób, w jaki komórki się komunikują, a w efekcie — jak budowany jest mózg.
Cytowanie: Méndez-Ruette, M., Bedoya, M., Hinrichsen, B. et al. A pathogenic mutation in α-SNAP impairs membrane lipid binding by concealing a critical hydrophobic loop. Commun Biol 9, 294 (2026). https://doi.org/10.1038/s42003-026-09578-y
Słowa kluczowe: alpha‑SNAP, wiązanie z błoną, mutacja białka, rozwój mózgu, fuzja pęcherzyków