Clear Sky Science · pl
ZFP42 utrzymuje „stemness” i rytmiczną transkrypcję w ludzkich komórkowych macierzystych i progenitorowych komórkach naskórka za pośrednictwem CRY1
Dlaczego wewnętrzny zegar twojej skóry ma znaczenie
Co noc, gdy śpisz, twoja skóra nie odpoczywa — naprawia się, odnawia i przygotowuje na następny dzień pełen słońca i zużycia. W tym badaniu badano, jak drobne biologiczne zegary w komórkach macierzystych skóry utrzymują ten proces odnowy w rytmie, oraz w jaki sposób mało znany czynnik o nazwie ZFP42 współdziała z białkiem zegara, CRY1, aby zachować młodość i funkcjonalność tych komórek. Zrozumienie powiązania między mechanizmami czasowymi a odnową skóry może w przyszłości pomóc w opracowaniu lepszych terapii przeciw starzeniu, wspomaganiu gojenia ran i leczeniu chorób skóry.
Zegary skóry
Podobnie jak nadrzędny zegar mózgu reagujący na światło, niemal każdy tkanka w organizmie ma swój „obwodowy” zegar. W zewnętrznej warstwie skóry, naskórku, komórki macierzyste i progenitorowe u podstawy nieustannie się dzielą, przesuwają ku górze i tworzą barierę ochronną, na którą polegamy. Autorzy badali te epidermalne komórki macierzyste i progenitorowe (EPSC) pochodzące zarówno z ludzkich płodów, jak i dorosłych, aby sprawdzić, ile genów włącza się i wyłącza w rytmie około 24 godzin. Stwierdzili, że około jedna na dziesięć aktywnych genów w tych komórkach wykazuje dobowe oscylacje, a wzorce czasowe wielu kluczowych genów zmieniają się między skórą płodową a dorosłą, co sugeruje, że komórkowe zegary skóry starzeją się razem z nami.
Płodowa kontra dorosła skóra: silniejsze rytmy w młodości
Synchronizując EPSC w hodowlach i mierząc aktywność genów co trzy godziny, zespół odkrył, że podstawowe geny zegara — takie jak BMAL1, PER1 i CRY1 — cyklują silnie zarówno w komórkach płodowych, jak i dorosłych. Jednak ogólna „głośność” rytmicznej aktywności genów, zwana amplitudą, była wyższa w komórkach płodowych i stłumiona w komórkach dorosłych. Wiele wspólnych genów rytmicznych wiązało się z replikacją DNA, podziałem komórkowym i naprawą — procesami kluczowymi dla utrzymania zdrowia komórek macierzystych. Czas szczytów ekspresji genów również się przesunął: komórki dorosłe wykazywały opóźnione i zmienione rytmy, szczególnie w genach związanych z obroną przed wirusami, starzeniem się komórek i zaprogramowaną śmiercią komórkową, co sugeruje, że dzienny program ochrony i odnowy zostaje przestrojony wraz z dojrzewaniem i starzeniem skóry.
Dzienny rytm wzrostu i dojrzewania
Kiedy badacze spojrzeli na geny rytmiczne występujące tylko u płodów lub tylko u dorosłych, zaobserwowali uderzające różnice. W płodowych EPSC fale genów zaangażowanych w odpowiedź na urazy, metabolizm i intensywne dzielenie się komórek miały tendencję do osiągania szczytu wcześniej w dobowym cyklu, co odpowiada ich szybkiemu wzrostowi i zdolności regeneracyjnej. W dorosłych EPSC geny związane z budową bariery skórnej i pchaniem komórek w kierunku pełnej różnicowania często osiągały szczyt wcześniej niż geny kontrolujące replikację DNA i podział. To rozdzielenie sugeruje, że dorosłe komórki macierzyste skóry mogą wykorzystywać porę dnia do przełączania między przygotowaniem komórek do utwardzenia się w powierzchnię ochronną a późniejszym zasilaniem proliferacji, być może by zrównoważyć utrzymanie bariery z ochroną przed dziennymi stresorami, takimi jak promieniowanie UV.
ZFP42 i CRY1: utrzymanie młodości komórek macierzystych
Zagłębiając się dalej, zespół szukał regulatorów, które mogłyby stać powyżej tych genów rytmicznych. Zidentyfikowali ZFP42, lepiej znany jako marker bardzo wczesnych komórek macierzystych, jako silnie aktywny w płodowych EPSC i mocno związany z promotorami płodowych genów rytmicznych. Gdy poziomy ZFP42 zostały obniżone w młodych EPSC, komórki dzieliły się rzadziej, gromadziły w wczesnej fazie cyklu komórkowego i wykazywały więcej oznak różnicowania i śmierci komórkowej. Odwrotny efekt również zaobserwowano: zwiększenie ZFP42 w EPSC od starszych dorosłych poprawiło ich zdolność do tworzenia kolonii, sprawiając, że zachowywały się bardziej jak młodsze komórki macierzyste. Co istotne, ZFP42 bezpośrednio aktywował gen zegara CRY1 i był niezbędny do jego prawidłowego rytmicznego funkcjonowania. Obniżenie poziomu samego CRY1 naśladowało wiele efektów utraty ZFP42 — wolniejszą proliferację i zwiększone różnicowanie — podczas gdy przywrócenie CRY1 częściowo ratowało defekty wzrostu, wskazując, że oś ZFP42–CRY1 jest kluczowa dla utrzymania zachowań podobnych do komórek macierzystych.
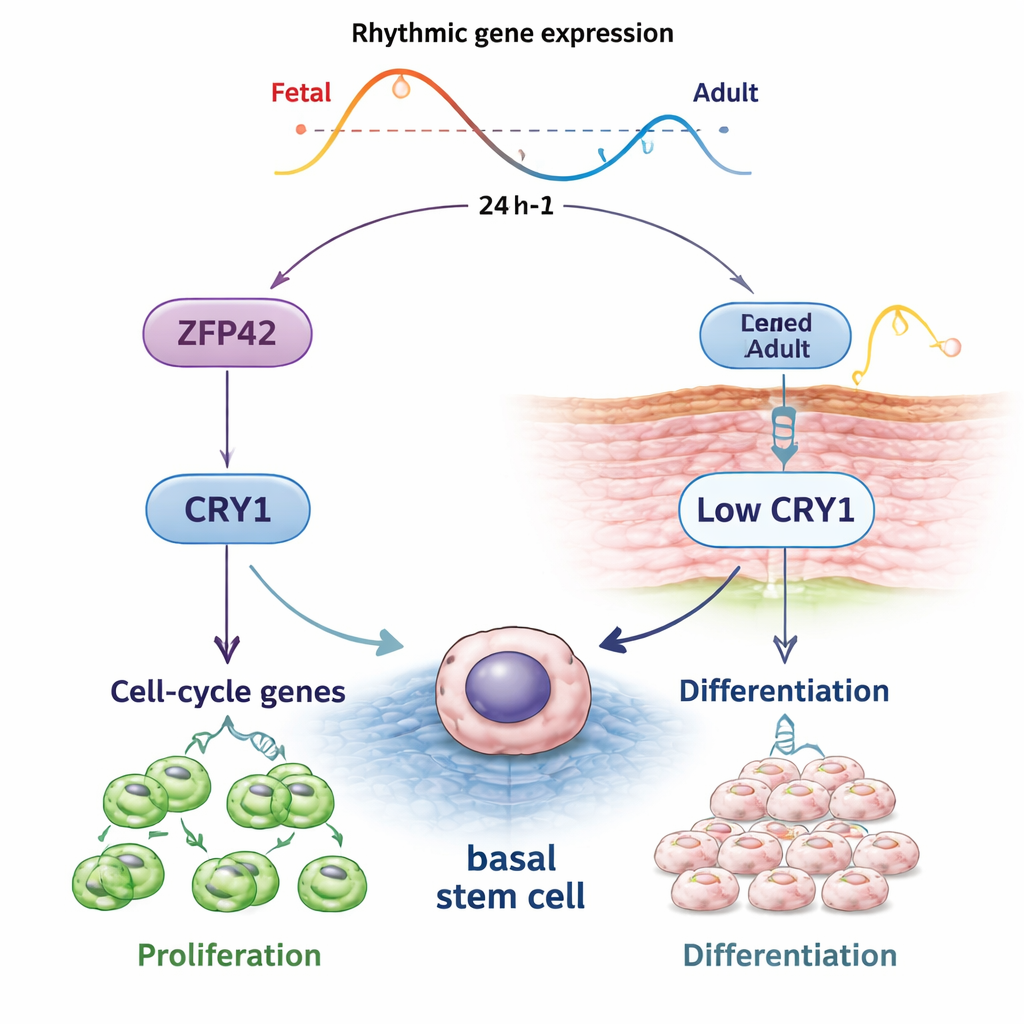
Co to oznacza dla zdrowia skóry
Dla czytelników niebędących specjalistami kluczowy wniosek jest taki, że komórki macierzyste skóry nie reagują na uszkodzenia i starzenie biernie — podążają za codziennym harmonogramem zaplanowanym przez molekularne zegary, a ten harmonogram zmienia się w ciągu życia. ZFP42 działa jako związany z młodością przełącznik, który utrzymuje aktywność i rytmiczność genu zegara CRY1, pomagając komórkom naskórka odnawiać się i zapobiegać przedwczesnemu dojrzewaniu. W miarę słabnięcia programów związanych z ZFP42 wraz z wiekiem, kontrolowane przez zegar cykle odnowy skóry wydają się zanikać. Chociaż prace przeprowadzono na hodowlanych komórkach i wymagają potwierdzenia w tkance żywej, wyniki te wskazują na możliwość, że regulacja ścieżki ZFP42–CRY1 lub dostosowanie terapii do wewnętrznego czasu skóry może w przyszłości poprawić leczenie starzejącej się skóry, przewlekłych ran i innych zaburzeń największego narządu ciała.
Cytowanie: Gao, S., Tan, H., Xu, S. et al. ZFP42 maintains stemness and rhythmic transcription in human epidermal stem and progenitor cells via CRY1. Commun Biol 9, 291 (2026). https://doi.org/10.1038/s42003-026-09576-0
Słowa kluczowe: rytm dobowy, komórki macierzyste skóry, naskórek, CRY1, ZFP42