Clear Sky Science · pl
Opracowanie ligandów prohibityny pochodnych kapsaicyny w celu modulacji interakcji kinazy Aurora A/PHB2 oraz mitofagii w komórkach nowotworowych
Dlaczego związek z papryczki chili ma znaczenie dla raka
Papryczkom chili zawdzięczamy ich palący smak dzięki kapsaicynie, niewielkiej cząsteczce, która wiąże się z białkami w naszych komórkach. W tym badaniu badacze przedstawiają zaskakujący obrót tej znanej przyprawy: przeprojektowali kapsaicynę, tworząc nowe cząsteczki o właściwościach lekopodobnych, które celują w „elektrownie” komórek nowotworowych — mitochondria — i modulują proces, którego te komórki używają, by utrzymywać swoje fabryki energii w dobrej kondycji. Ponieważ komórki nowotworowe w dużym stopniu polegają na wydajnych mitochondriach do napędzania gwałtownego wzrostu, możliwość selektywnego zakłócenia tego systemu wsparcia może otworzyć nową ścieżkę terapii przeciwnowotworowej.
Elektrownie komórkowe i ich wewnętrzny zespół sprzątający
Mitochondria nieustannie równoważą budowę nowych jednostek z recyklingiem uszkodzonych. Strona recyklingowa, zwana mitofagią, działa jak system kontroli jakości: zużyte mitochondria są znakowane i rozkładane, podczas gdy zdrowsze pozostają. Wiele komórek nowotworowych przejmuje tę równowagę, wykorzystując mitofagię do eliminowania słabych mitochondriów i wzbogacania „superwydajnych”, które produkują duże ilości ATP, waluty energetycznej komórki. Białko zwane kinazą Aurora A (AURKA), często nadmiernie eksprymowane w guzach, niedawno odkryto wewnątrz mitochondriów, gdzie współdziała z innym białkiem, Prohibityną‑2 (PHB2), oraz adapterem autofagii LC3. Razem tworzą kompleks, który promuje mitofagię i wspiera wysoką produkcję energii w komórkach nowotworowych.
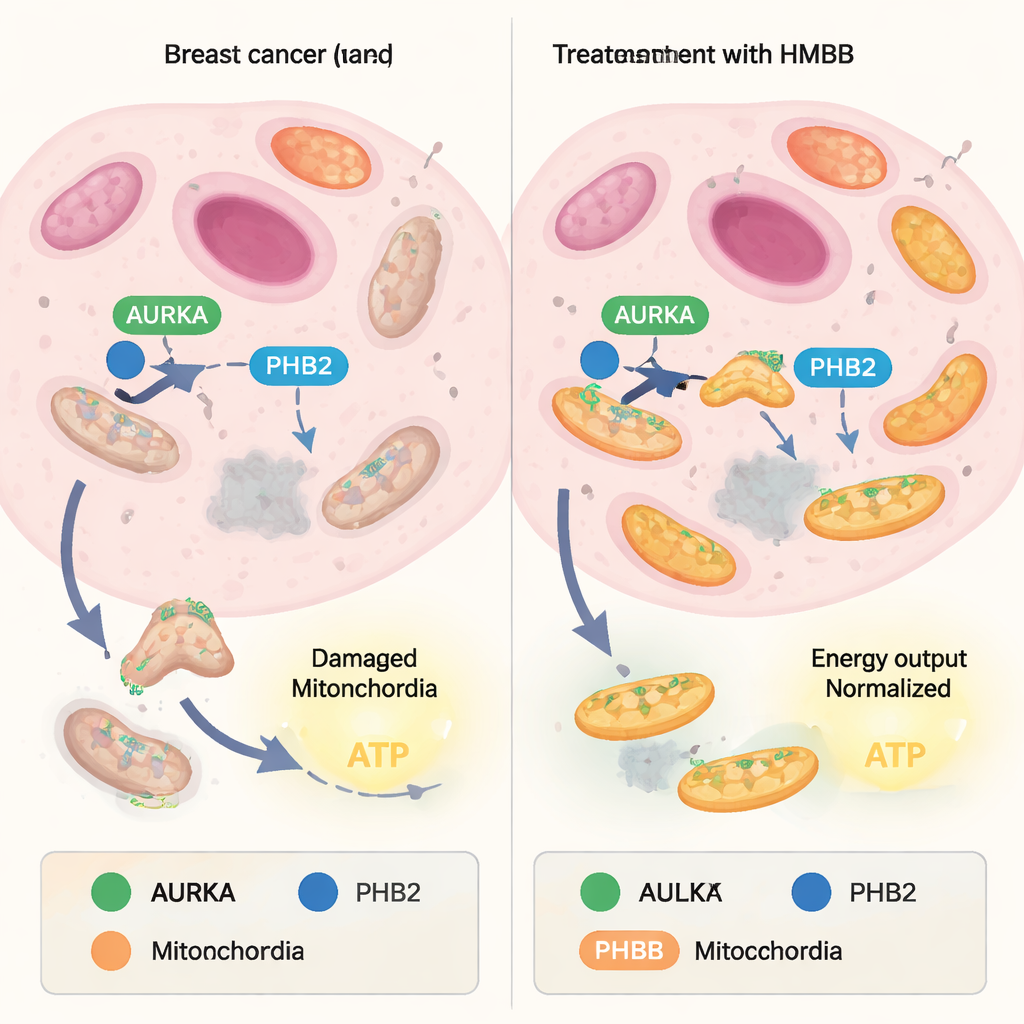
Od ostrej kapsaicyny do dopasowanych narzędzi molekularnych
Wcześniejsze prace wykazały, że naturalny związek zwany xanthohumolem może wiązać się z PHB2 i zakłócać kompleks AURKA–PHB2–LC3, blokując mitofagię i zmniejszając produkcję mitochondrialnego ATP. Jednak struktura chemiczna xanthohumolu nie jest idealna dla rozwoju leków. W tym badaniu autorzy zwrócili się ku kapsaicynie, innemu naturalnemu ligandowi PHB, i zapytali, czy można ją przekształcić w bardziej praktyczne narzędzia. Najpierw potwierdzili, że kapsaicyna nieznacznie osłabia interakcję między AURKA i PHB2 w żywych komórkach raka piersi, używając techniki obrazowania (FRET/FLIM), która mierzy, jak blisko siebie znajdują się dwa znakowane białka. Następnie zsyntetyzowali 16 molekuł inspirowanych kapsaicyną poprzez modyfikację „ogona” i aromatycznej „głowy” oryginalnej struktury i systematycznie testowali, jak każda wersja wpływa na partnerstwo AURKA–PHB2 wewnątrz mitochondriów.
Odkrycie molekularnego „kleju”, który skleja białka
Zmienione cząsteczki wywołały wyraźnie różne efekty. Niektóre, jak sama kapsaicyna czy pochodna nazwana związek 5, ułatwiały rozdzielenie AURKA i PHB2. Inne niemal nie wywierały wpływu. Jednak podzbiór — zwłaszcza cząsteczka nazwana związek 13, później określona jako HMBB — miał efekt odwrotny i znacząco wzmacniał wiązanie między AURKA i PHB2. Symulacje dokowania komputerowego pomogły wyjaśnić to zachowanie. Kapsaicyna i związek 5 miały tendencję do wklinowywania się w miejsce aktywne AURKA w sposób powodujący fizyczne konflikty z PHB2, popychając dwa białka w stronę rozdzielenia. Natomiast związki 12 i 13 osadzały się w miejscu aktywnym AURKA i jednocześnie kontaktowały znane kieszenie hamujące na PHB2 bez powodowania zderzenia. Ich kształty pozwalały działać jak „molekularny klej”, łącząc AURKA i PHB2 i stabilizując kompleks.
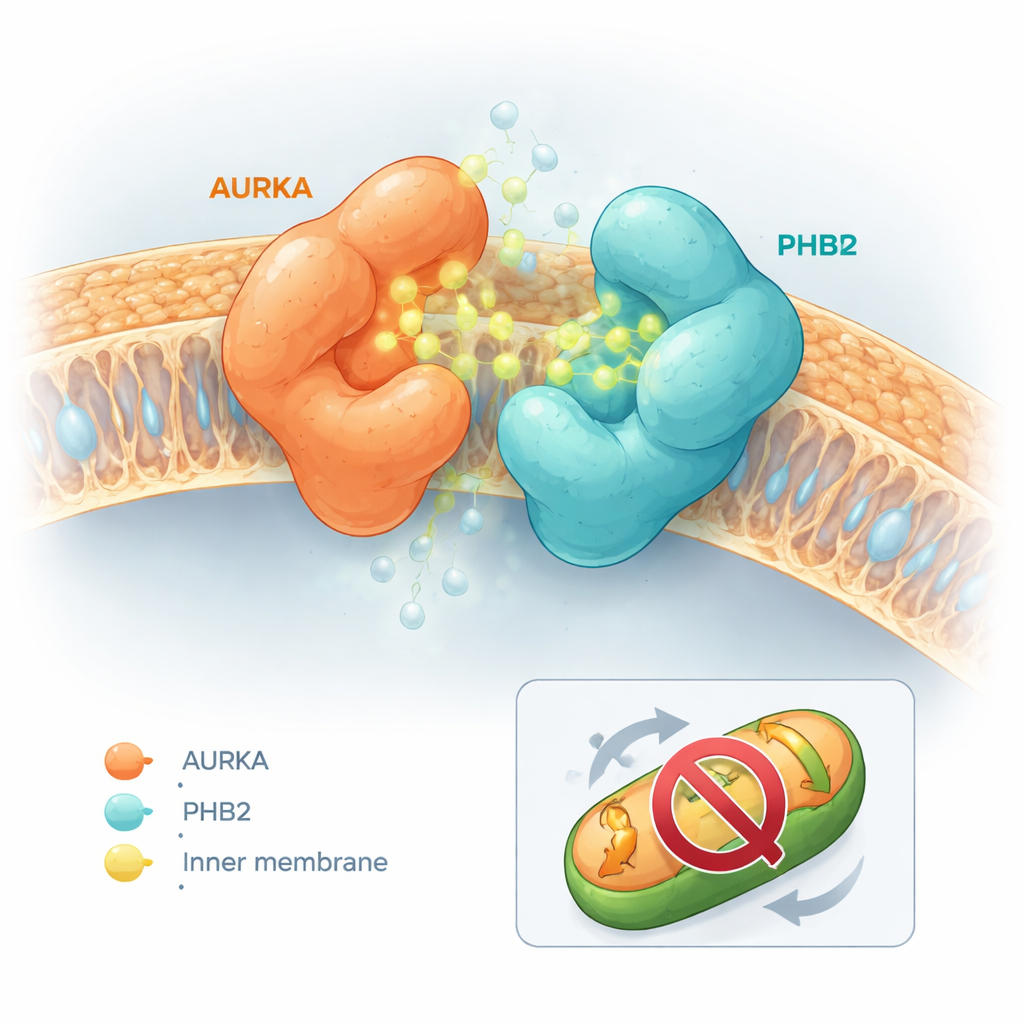
Blokowanie mitochondrialnego sprzątania bez wyłączania centrum sterowania komórki
Kluczowym pytaniem było, czy zachowanie jak molekularny klej po prostu dezaktywuje AURKA w całej komórce, co wiązałoby się z szerokimi efektami ubocznymi, czy działa bardziej selektywnie. Używając osobnego fluorescencyjnego biosensora raportującego o aktywacji AURKA w centrosomach — strukturach organizujących maszynerię podziału komórki — zespół zaobserwował, że HMBB nie tłumił aktywności AURKA w tych miejscach. Jednak w testach mitochondrialnych HMBB odwracał utratę masy mitochondrialnej normalnie wywoływaną przez nadekspresję AURKA w komórkach raka piersi. W komórkach naturalnie produkujących wysokie poziomy AURKA HMBB zwiększał zawartość mitochondriów, co wskazuje, że mitofagia napędzana przez AURKA została zablokowana. W komórkach z niskim poziomem AURKA HMBB miał niewielki wpływ, podkreślając jego zależność od szlaku AURKA–PHB2.
Co to może oznaczać dla przyszłych terapii przeciwnowotworowych
Podsumowując, wyniki pokazują, że starannie zaprojektowane pochodne kapsaicyny mogą precyzyjnie modulować sposób, w jaki AURKA i PHB2 wchodzą w interakcję w mitochondriach. Działając jak molekularny klej, HMBB i pokrewne związki blokują AURKA i PHB2 w konfiguracji, która uniemożliwia przejście zwykłego programu mitofagii, bez wyłączania niezbędnych ról AURKA w innych częściach komórki. Dla czytelnika niebędącego specjalistą kluczowa idea jest taka, że autorzy stworzyli prototypowe cząsteczki, które selektywnie ingerują w sposób, w jaki komórki nowotworowe utrzymują swoje elektrownie w optymalnym stanie, potencjalnie osłabiając ich źródło energii przy zachowaniu funkcji normalnych komórek. Chociaż związki te są nadal na wczesnym, laboratoryjnym etapie, ilustrują obiecującą strategię: wykorzystanie małych, lekopodobnych cząsteczek do celowania w specyficzne partnerstwa białkowe wewnątrz mitochondriów i w ten sposób podważanie metabolicznych przewag, od których zależy wiele guzów.
Cytowanie: Djehal, A., Caron, C., Giordano, D. et al. Development of capsaicin-derived prohibitin ligands to modulate the Aurora kinase A/PHB2 interaction and mitophagy in cancer cells. Commun Biol 9, 320 (2026). https://doi.org/10.1038/s42003-026-09573-3
Słowa kluczowe: mitochondria, mitofagia, kinaza Aurora A, pochodne kapsaicyny, metabolizm nowotworowy