Clear Sky Science · pl
Funkcjonalna przebudowa komórek iNKT przez sulfatyd-reaktywne komórki typu II NKT przekształca makrofagi pęcherzykowe, aby złagodzić niedokrwienno–reperfuzyjne uszkodzenie płuc
Dlaczego ochrona płuc dawcy ma znaczenie
Gdy chirurdzy przeszczepiają płuco lub przywracają przepływ krwi po zablokowaniu naczynia, nagły napływ tlenu może paradoksalnie uszkodzić tkankę. Ten problem, zwany niedokrwienno–reperfuzyjnym uszkodzeniem płuc, jest główną przyczyną wczesnych niepowodzeń po przeszczepie płuca i innych krytycznych zabiegach. Streszczeniu przedstawionemu tutaj przyglądano się, jak rzadki zestaw komórek odpornościowych można „przeprogramować”, by uspokoić stan zapalny, co otwiera potencjalną nową drogę ochrony wrażliwych płuc, gdy są najbardziej potrzebne.
Komórki odpornościowe, które mogą leczyć lub szkodzić
Nasze płuca patrolują makrofagi pęcherzykowe — komórki odpornościowe osadzone w pęcherzykach powietrznych, które szybko reagują na zagrożenie. Komórki te mogą przełączać się między dwoma głównymi trybami. W trybie „walki” (często nazywanym M1) uwalniają substancje prozapalne, które pomagają zabić drobnoustroje, ale mogą też uszkadzać tkankę. W trybie „naprawy” (często nazywanym M2) wydzielają środki łagodzące, które ograniczają zapalenie i wspierają gojenie. W niedokrwienno–reperfuzyjnym uszkodzeniu płuc równowaga przesuwa się w stronę szkodliwego trybu walki. Badacze założyli, że jeśli uda się delikatnie przesunąć makrofagi w stronę trybu naprawczego w odpowiednim momencie, można by złagodzić skutki tego urazu.
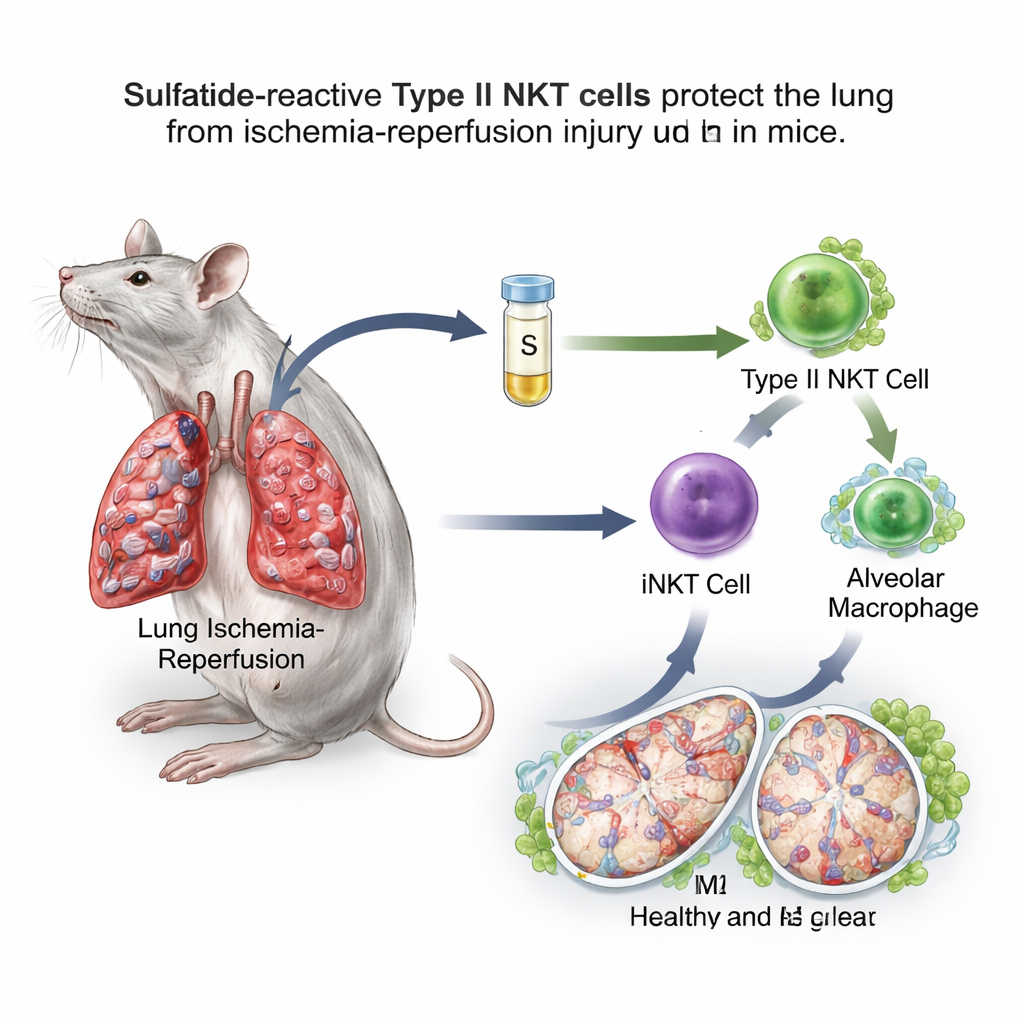
Cukrowo‑tłuszczowa cząsteczka przełącza immunologiczny wyłącznik
Zespół skupił się na komórkach natural killer T (NKT), nietypowych komórkach odpornościowych zajmujących miejsce pomiędzy szybko działającą odpornością wrodzoną a wolniejszymi, ukierunkowanymi odpowiedziami. Komórki NKT występują w dwóch głównych typach. Typ I, zwany też inwariantnymi komórkami NKT (iNKT), w modelach mysich jest znany z pogarszania niedokrwienno–reperfuzyjnego uszkodzenia płuc. Komórki typu II NKT potrafią natomiast hamować reakcje immunologiczne w innych narządach. Tłuszczowa cząsteczka nazwana sulfatydem jest rozpoznawana specyficznie przez komórki typu II NKT. W modelu myszy, w którym przepływ krwi do jednego płuca był zaciskany przez godzinę, a następnie przywracany, badacze podawali sulfatyd kilka godzin przed urazem. Stwierdzili, że myszy leczone sulfatydem miały mniejsze obrzęki płuc, mniej nieszczelnych naczyń, niższy stres oksydacyjny, lepsze parametry utlenowania i zmniejszoną ilość substancji zapalnych w płukance płucnej w porównaniu z zwierzętami nieleczonymi.
Przeprogramowanie makrofagów przez przekaźnik sygnałów
Bliższe badania wykazały, że sulfatyd przesuwa makrofagi pęcherzykowe w stronę stanu M2 ukierunkowanego na naprawę. Te makrofagi wykazywały więcej markerów powierzchniowych i genów związanych z gojeniem oraz lepiej tłumiły stan zapalny po przeszczepieniu do innych myszy. Gdy naukowcy selektywnie usunęli makrofagi pęcherzykowe, uraz płuc się pogorszył, a ochronny efekt sulfatydu w dużej mierze zniknął, co pokazuje, że te komórki są kluczowym węzłem w tej ścieżce. Co ważne, korzyść z sulfatydu znikała u myszy pozbawionych albo komórek typu II NKT, albo komórek iNKT typu I, i można ją było przywrócić przez transfer iNKT uprzednio wystawionych na działanie sulfatydu. Razem te eksperymenty ujawniły przekaźnik sygnałów: sulfatyd aktywuje komórki typu II NKT, które z kolei przekształcają zachowanie komórek iNKT, a te przeprogramowują makrofagi pęcherzykowe.
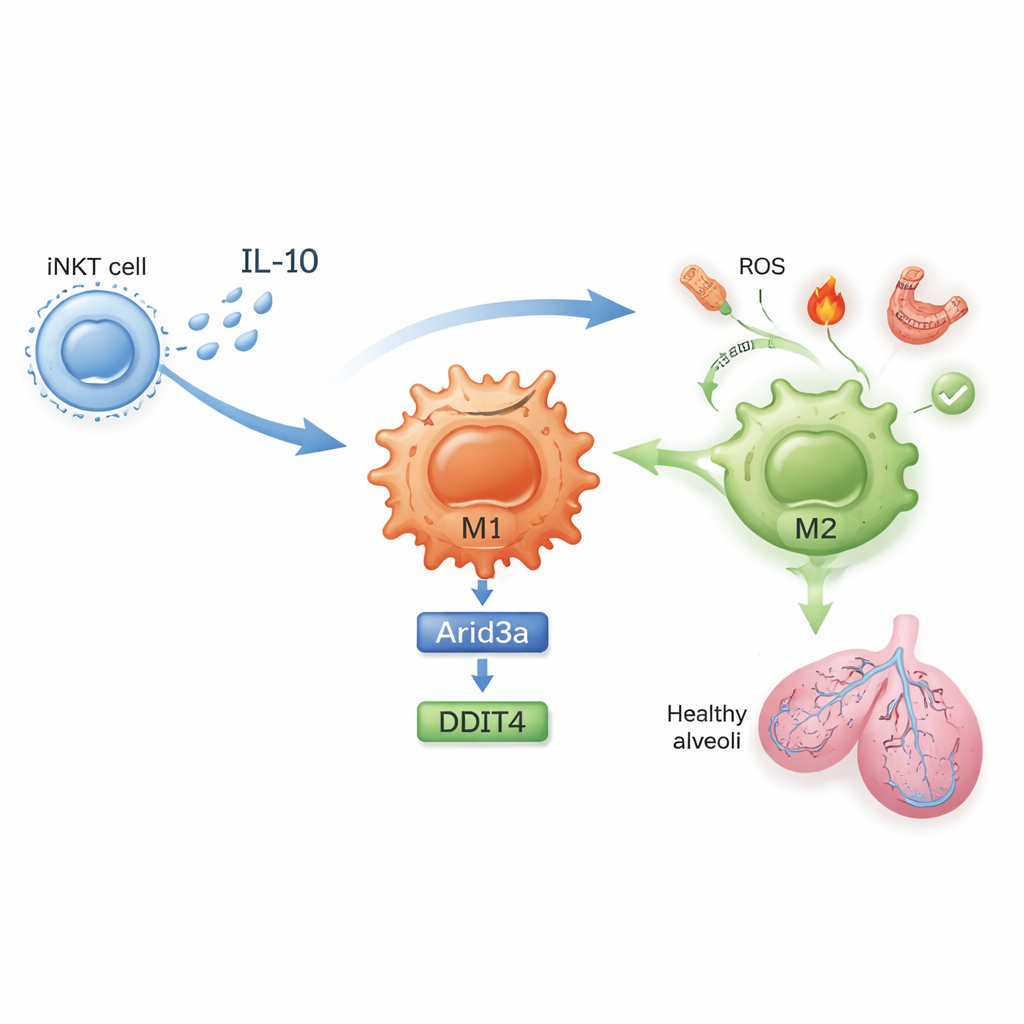
Molekularny łańcuch, który uspokaja zapalenie
Co dokładnie zmienia się we wnętrzu tych komórek? U myszy nieleczonych komórki iNKT płuc proliferowały podczas niedokrwienia–reperfuzji i produkowały duże ilości interferonu-gamma, silnego sygnału prozapalnego. Po ekspozycji na sulfatyd komórki iNKT wytwarzały natomiast więcej interleukiny‑10 (IL‑10), silnej cząsteczki przeciwzapalnej, i mniej interferonu-gamma. Badanie pokazuje, że IL‑10 pochodząca z iNKT działa bezpośrednio na makrofagi, napędzając ich polaryzację w kierunku M2. Dzięki profilowaniu ekspresji genów i starannie zaprojektowanym eksperymentom w hodowlach komórkowych autorzy odkryli molekularny łańcuch wewnątrz makrofagów: IL‑10 zwiększa poziom czynnika transkrypcyjnego nazwanego Arid3a, który z kolei podnosi ekspresję genu odpowiedzi na stres DDIT4. Ta oś Arid3a–DDIT4 pomaga wyłączyć szlak kontroli wzrostu, który inaczej utrzymuje makrofagi w stanie zapalnym, przesuwając je ku ochronnemu programowi M2.
Z mysich płuc ku przyszłym terapiom
Aby sprawdzić, jak centralna jest ta molekularna sekwencja, badacze zastosowali małe interferujące RNA do wyciszenia Arid3a lub DDIT4 w makrofagach przed ich transferem do myszy. Gdy którykolwiek z tych genów został stłumiony, sulfatyd nie był już w stanie w pełni przesunąć makrofagów w stronę trybu naprawczego, a ochrona płuc osłabła. Dalsze analizy sugerują, że białko sygnałowe zwane YES1 pomaga komórkom typu II NKT aktywowanym przez sulfatyd przestawić iNKT w kierunku produkcji IL‑10. Chociaż te odkrycia pochodzą z modeli mysich i z manipulowanych komórek w laboratorium, przedstawiają jasną narrację: krótkotrwała aktywacja określonej podgrupy komórek NKT sulfatydem może umożliwić przekształcenie potencjalnie szkodliwych odpowiedzi immunologicznych w takie, które chronią przeszczepione lub uszkodzone płuca. W przyszłości leki naśladujące tę ścieżkę mogłyby pomóc większej liczbie pacjentów przeżyć i dobrze funkcjonować po ratujących życie zabiegach płucnych.
Cytowanie: Li, Q., Yin, J., Lin, Q. et al. Functional remodeling of iNKT cells by sulfatide-reactive type II NKT cells reprograms alveolar macrophages to alleviate lung ischemia-reperfusion injury. Commun Biol 9, 289 (2026). https://doi.org/10.1038/s42003-026-09572-4
Słowa kluczowe: niedokrwienno reperfuzyjne uszkodzenie płuc, makrofagi pęcherzykowe, komórki NK T, interleukina-10, modulacja odporności