Clear Sky Science · pl
MHC1-TIP umożliwia jednorurkowe, multimodalne profilowanie immunopeptydomu i ujawnia wewnątrztumorową heterogenność prezentacji antygenów
Rzut oka na „dowody tożsamości” raka
Każda komórka nosi na powierzchni drobne molekularne „dowody tożsamości”, które pomagają układowi odpornościowemu zdecydować, czy komórka jest zdrowa, czy niebezpieczna. W raku te identyfikatory — krótkie fragmenty białek zwane antygenami — mogą ujawnić, co czyni komórkę nowotworową odmienną i oznaczyć ją do zniszczenia przez komórki odpornościowe. W badaniu przedstawiono nową metodę laboratoryjną, MHC1-TIP, która znacznie ułatwia i obniża koszty odczytu tych „dowodów” z bardzo małych ilości tkanki pacjenta, otwierając możliwości dla bardziej precyzyjnych immunoterapii przeciwnowotworowych.
Dlaczego sygnały z powierzchni komórki mają znaczenie
Nasz układ odpornościowy nieustannie kontroluje komórki, sprawdzając antygeny prezentowane na specjalnych cząsteczkach zwanych MHC klasy I. Komórki nowotworowe często pokazują nietypowe antygeny, które — w teorii — mogą być rozpoznawane przez limfocyty T i celem terapii, takich jak szczepionki spersonalizowane. Jednak rzeczywiste zmierzenie, które antygeny występują w próbkach pacjentów, było technicznie wymagające. Tradycyjne metody potrzebują ogromnej liczby komórek, wielu etapów obróbki i drogich przeciwciał, przez co są słabo dopasowane do maleńkich biopsji czy rzadkich próbek klinicznych. Jednocześnie nowotwory nie są jednorodne: różne obszary mogą wyrażać różne białka, co sugeruje, że prezentacja antygenów również może się różnić w obrębie pojedynczego guza.
Jednorurkowy skrót do antygenów nowotworowych
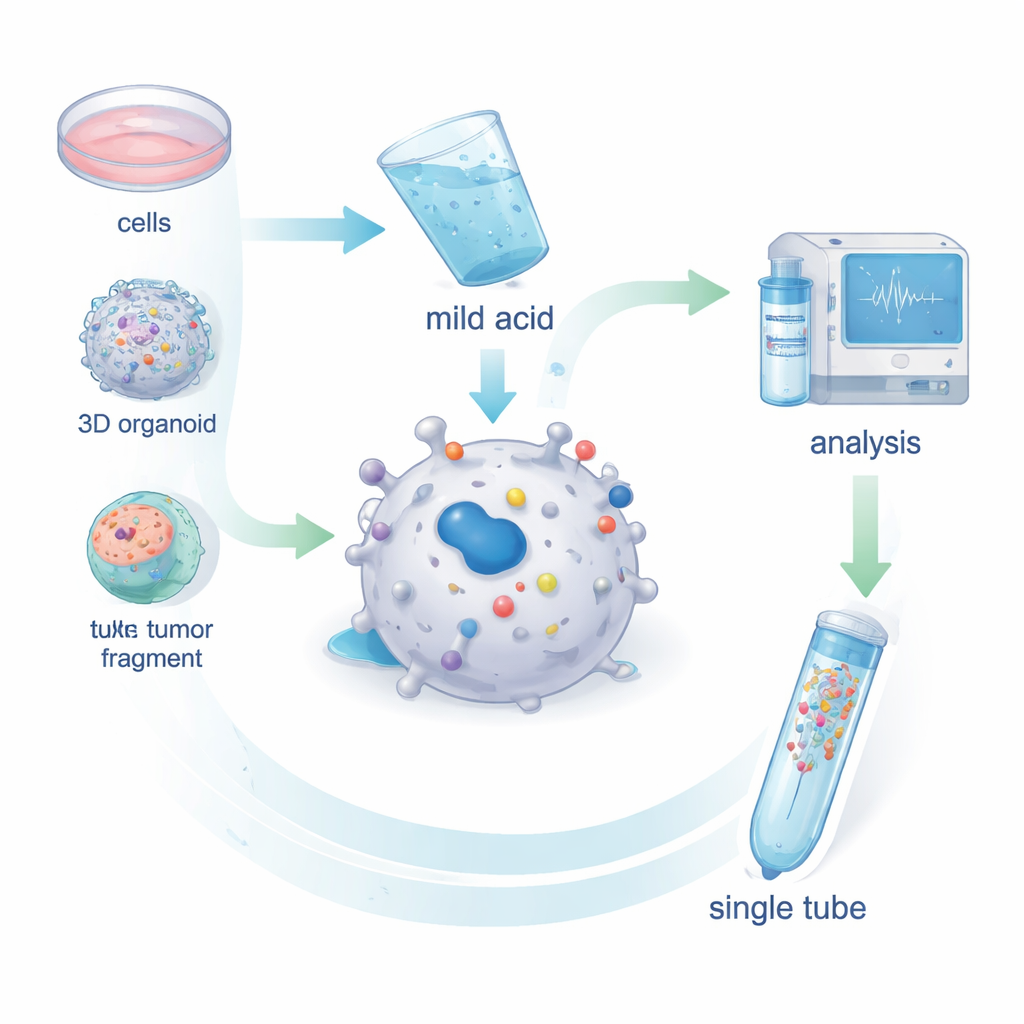
Naukowcy opracowali MHC1-TIP (MHC-I 1-Tube Immunopeptidomics) jako uproszczony sposób zbierania antygenów z żywych komórek. Zamiast rozbijać komórki i wyławiać cząsteczki MHC za pomocą przeciwciał, krótko płuczą nieuszkodzone komórki — albo drobne fragmenty guza — łagodnym roztworem kwasowym. To delikatne traktowanie powoduje, że antygeny siedzące w rowku MHC odrywają się, nie zabijając komórek. Uwolnione peptydy przechodzą następnie przez mały filtr usuwający większe zanieczyszczenia i są zatrzymywane na niewielkiej kolumnie wewnątrz jednej rurki. Stamtąd trafiają bezpośrednio do spektrometru mas, który identyfikuje sekwencje peptydowe. Testy na komórkach czerniaka wykazały, że ten łagodny krok kwasowy usuwa niemal wszystkie kompleksy MHC–antygen z powierzchni, a odzyskane peptydy wyglądają jak autentyczne antygeny związane z MHC pod względem długości i wzorców sekwencji.
Więcej danych z mniejszej próbki
MHC1-TIP zaprojektowano tak, by działał przy bardzo niewielkiej liczbie komórek i jednocześnie dostarczał wielu identyfikowalnych antygenów. Łącząc nowy przebieg pracy z nowoczesnym trybem spektrometrii mas zwanym akwizycją niezależną od danych (data-independent acquisition), zespół wykrył setki antygenów z zaledwie 100 000 komórek i tysiące z kilku milionów komórek — głębokość porównywalną ze złotym standardem metody z użyciem przeciwciał, ale przy mniejszej ilości materiału i niższych kosztach. Metoda zadziałała także na organoidach pochodzenia pacjenta, czyli trójwymiarowych mini-guzach hodowanych w laboratorium, oraz na maleńkich fragmentach guza ex vivo mniejszych niż milimetr sześcienny. Co ważne, ponieważ płukanie kwasem pozostawia komórki w dużej mierze nienaruszone, pozostały materiał można wykorzystać do pełnoskalowego profilowania białek z tej samej próbki, co pozwala na bezpośrednie porównanie, ile danego białka jest obecne, a ile z niego jest faktycznie prezentowane jako antygen.
Ukryte różnice wewnątrz pojedynczego guza
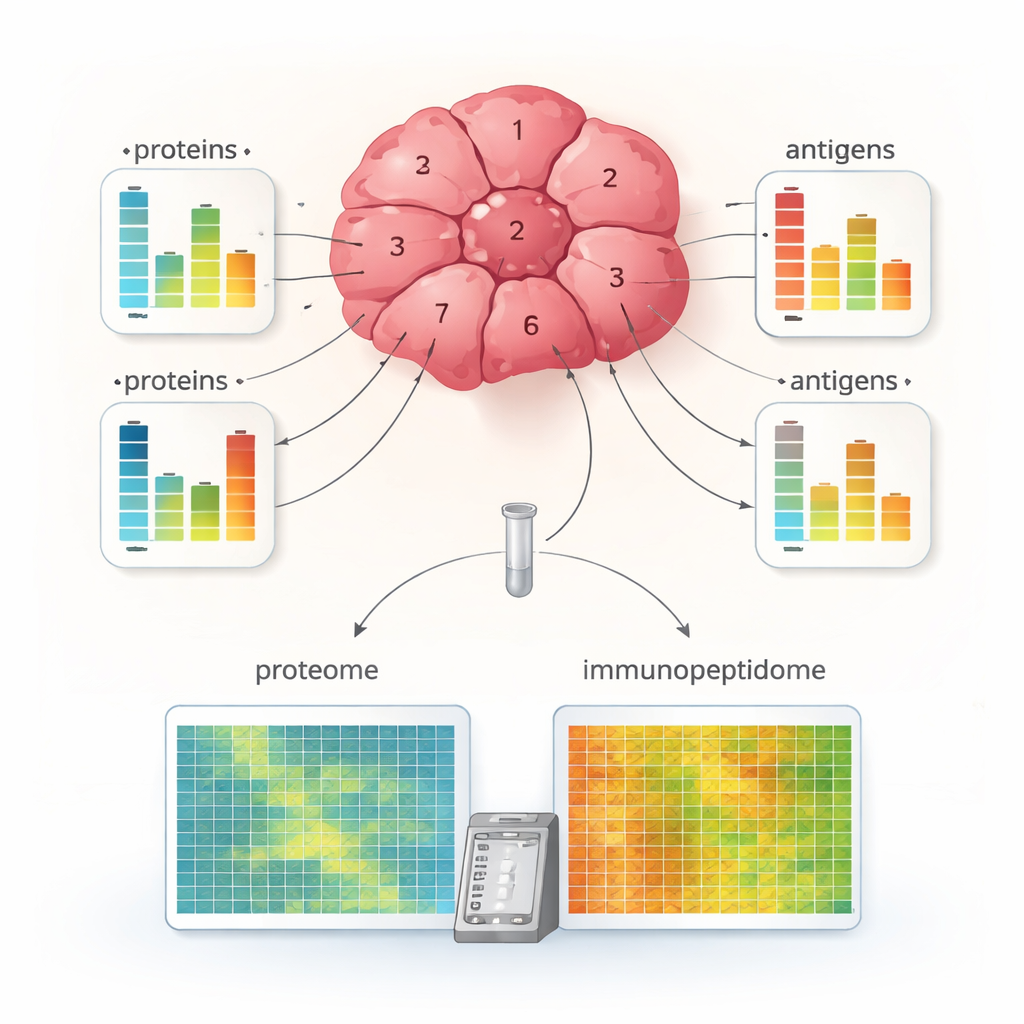
Zastosowanie MHC1-TIP do wielu małych fragmentów pobranych z różnych rejonów guza raka nerkowego ujawniło uderzającą różnorodność wewnętrzną. Niektóre fragmenty wykazywały bogatą prezentację antygenów, inne bardzo mało antygenów, mimo że ich ogólna zawartość białek mogła być podobna. Dla wielu białek zmiany w poziomach antygenów nie odpowiadały zmianom w ich obfitości białkowej, co sugeruje, że przetwarzanie antygenów i ich umieszczanie na cząsteczkach MHC są regulowane niezależnie od ilości białka macierzystego. Zespół połączył także dane o antygenach z markerami komórek odpornościowych i mechanizmu MHC, identyfikując regiony guza „gorące immunologicznie” — z wysoką ekspozycją antygenów i oznakami aktywnych limfocytów T — oraz „zimne immunologicznie” — z mniejszą liczbą antygenów i słabszymi sygnałami ataku immunologicznego. Taki poziom szczegółu rzadko był możliwy do uzyskania z tak drobnych fragmentów tkanki.
Co to oznacza dla przyszłej opieki nad pacjentem z rakiem
Dla osoby niebędącej specjalistą główny przekaz jest taki, że samo zmierzenie, jakie białka produkuje guz, nie wystarcza, by wiedzieć, co układ odpornościowy naprawdę widzi. Nowa metoda MHC1-TIP oferuje praktyczny sposób odczytu rzeczywistej ekspozycji antygenów z bardzo małych, klinicznie realistycznych próbek, równocześnie mierząc szerszy pejzaż białkowy. Odkrycie, że prezentacja antygenów może znacznie różnić się w różnych częściach tego samego guza i nie zawsze podąża za poziomem białek, ostrzega przed wybieraniem celów do szczepionek lub terapii komórkowych wyłącznie na podstawie ekspresji genów czy białek. W przyszłości podejścia takie jak MHC1-TIP mogą pomóc w projektowaniu skuteczniejszych, spersonalizowanych immunoterapii poprzez koncentrację na antygenach faktycznie widocznych na powierzchni i prezentowanych bardziej konsekwentnie w całym guzie.
Cytowanie: Bathini, M., Bocaniciu, D., Johnson, F.D. et al. MHC1-TIP enables single-tube multimodal immunopeptidome profiling and uncovers intratumoral heterogeneity in antigen presentation. Commun Biol 9, 296 (2026). https://doi.org/10.1038/s42003-026-09570-6
Słowa kluczowe: prezentacja antygenów, immunopeptydomika, immunoterapia przeciwnowotworowa, heterogenność guza, spektrometria mas