Clear Sky Science · pl
Reewaluacja specyficzności Gα białko–element odpowiedzi w sygnalizacji GPCR
Dlaczego małe przełączniki komórkowe mają znaczenie dla medycyny
Wiele współczesnych leków działa przez przełączanie molekularnych „wyłączników” na powierzchni komórek, zwanych receptorami sprzężonymi z białkiem G (GPCR). Te przełączniki przekazują sygnały do wnętrza komórki za pośrednictwem białek pomocniczych zwanych białkami G i ostatecznie włączają lub wyłączają geny. Przez dekady badacze polegali na prostych testach produkujących światło, aby sprawdzić, których białek G używa dany lek lub receptor. Niniejsze badanie stawia podstawowe, ale kluczowe pytanie: czy te testy rzeczywiście informują nas o tym, co myślimy — i czy można im ufać przy projektowaniu następnej generacji precyzyjnych leków?
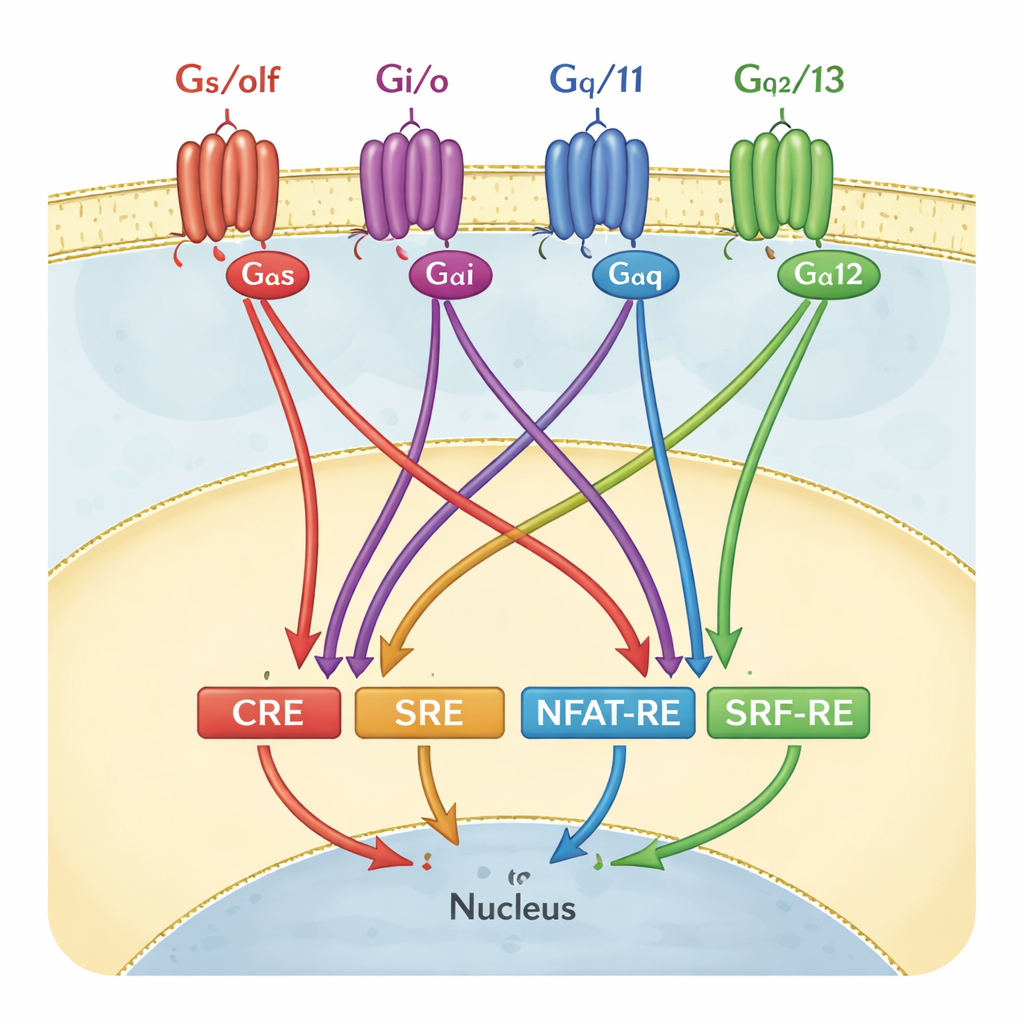
Jak naukowcy zazwyczaj odczytują sygnały GPCR
Aby śledzić aktywność GPCR, wiele laboratoriów używa testów z genami reporterowymi. W tych eksperymentach komórki są zmodyfikowane tak, że gdy aktywowany jest określony przełącznik genowy, czyli „element odpowiedzi”, komórki świecą. Cztery takie elementy są szczególnie popularne: CRE, SRE, NFAT‑RE i SRF‑RE. Każdy z nich długo był traktowany jako zastępstwo dla jednego odgałęzienia sygnalizacji białek G — na przykład CRE dla rodziny Gαs/olf, czy SRF‑RE dla Gα12/13. W podręcznikach i w procesach screeningowych powiązania te często rysowane są niemal jak schematy połączeń jeden do jednego: włącz konkretne białko G, a zapali się tylko jeden reporter.
Testowanie starego schematu połączeń
Autorzy systematycznie poddali ten obraz próbie, używając ludzkich komórek HEK293, w których konkretne rodziny białek G — a nawet wszystkie białka G — usunięto przy pomocy edycji genomu. Następnie przywracali pojedyncze typy białek G jeden po drugim. W tych komórkach ekspresjonowali dziewięć różnych GPCR, wybranych tak, by reprezentować receptory sygnalizujące bardzo selektywnie lub za pośrednictwem wielu partnerów białek G. Mierząc, jak mocno każdy z czterech reporterów świecił przy różnych stężeniach leku, mogli ustalić, które białka G są faktycznie niezbędne dla każdego elementu odpowiedzi, a które mogą pośrednio wspomagać reakcję.
Zachodzące nakładanie się szlaków zamiast czystych kanałów
Wyniki obalają uporządkowany model „jeden receptor — jeden reporter”. Chociaż CRE nadal zależał głównie od białek Gαs/olf — klasycznej ścieżki podnoszącej cAMP — inne rodziny białek G mogły zauważalnie wpływać na aktywność CRE, ale tylko gdy obecne było Gαs/olf. Dla pozostałych trzech reporterów, SRE, NFAT‑RE i SRF‑RE, głównym kierowcą okazała się rodzina Gαq/11, mimo że SRE i SRF‑RE tradycyjnie łączono z innymi odgałęzieniami białek G. SRE i SRF‑RE zachowywały się szczególnie podobnie, co sugeruje, że korzystają ze wspólnego aparatu efektorowego, a nie z odrębnych, izolowanych dróg. W wielu przypadkach dodatkowe białka G, takie jak Gα12/13 i Gαi/o, dostarczały dodatkowego wsparcia lub tła aktywności, podkreślając sieć sprzężeń zamiast oddzielnych kanałów.
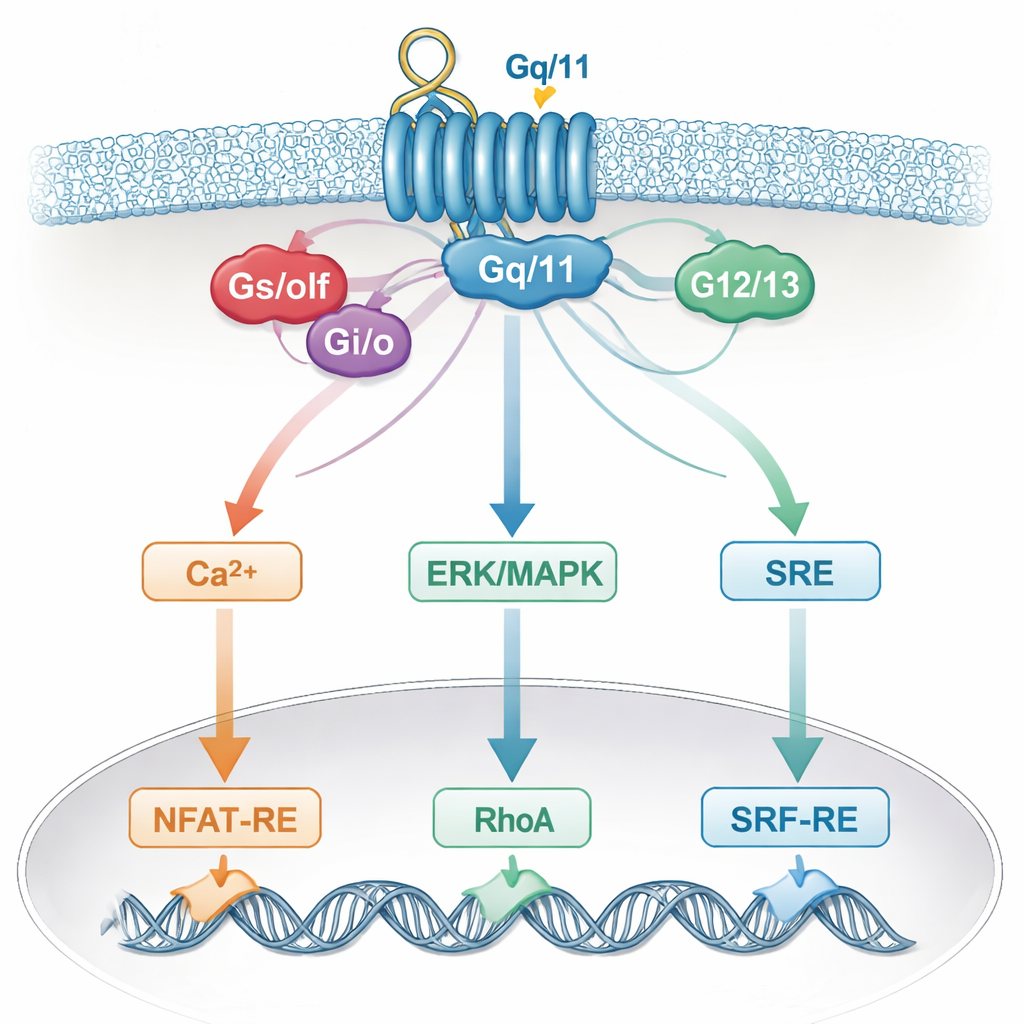
Dlaczego sieć komórki zaciera nasze odczyty
Ta zacierająca się specyficzność prawdopodobnie odzwierciedla sposób, w jaki prawdziwe komórki integrują sygnały. Pojedynczy receptor może aktywować wiele białek G, które następnie zbiegają się na wspólnych przekaźnikach, takich jak wapń, ERK/MAPK, RhoA czy cAMP, oraz na wspólnych pomocnikach, takich jak podjednostki Gβγ. Te wspólne ścieżki z kolei oddziałują na te same przełączniki genowe w jądrze. W rezultacie reporter, który uważano za reagujący na jedną rodzinę białek G, właściwie „nasłuchuje” kilku. Czynniki specyficzne dla typu komórki i dokładny zestaw obecnych receptorów dodają jeszcze więcej złożoności, co oznacza, że wnioski wyciągnięte w jednym systemie komórkowym mogą nie mieć zastosowania w innym.
Co to oznacza dla odkrywania leków
Dla osób niebędących specjalistami kluczowy wniosek jest taki, że wiele powszechnie używanych testów GPCR opartych na emisji światła jest mniej specyficznych, niż sugerują ich etykiety. Nadal potrafią one pokazać, że receptor jest aktywny i mniej więcej które szerokie ścieżki są zaangażowane, ale nie stanowią wiarygodnego dowodu, że zaangażowana jest konkretna rodzina białek G — i tylko ona. Autorzy zalecają, by badacze i twórcy leków traktowali te reportery jako przybliżone wskaźniki i łączyli je z bardziej bezpośrednimi metodami, które obserwują interakcje białek w czasie rzeczywistym. Taka kombinacja da wierniejszy obraz tego, jak potencjalne leki kierują sygnalizacją komórkową i pomoże uniknąć mylących skrótów w poszukiwaniu bezpieczniejszych, bardziej ukierunkowanych terapii.
Cytowanie: Saito, A., Kise, R., Yamaguchi, S. et al. Re-evaluating Gα protein–response element specificity in GPCR signaling. Commun Biol 9, 288 (2026). https://doi.org/10.1038/s42003-026-09569-z
Słowa kluczowe: Sygnalizacja GPCR, Białka G, testy reporterowe, sieci sygnalizacyjne komórek, odkrywanie leków