Clear Sky Science · pl
Testy aktywności kinaz sprzężonych z białkami G oparte na komórkach i wybiórcze dla izoform — kompleksowa ocena inhibitorów
Dlaczego ważne jest przyciszanie „pokręteł głośności” w komórce
Wiele naszych leków działa przez zwiększanie lub zmniejszanie aktywności receptorów na powierzchni komórek, które wykrywają hormony, neuroprzekaźniki i leki. Receptory te muszą być potem starannie wyłączane, aby komórki nie pozostawały nadmiernie pobudzone — proces ten jest częściowo kontrolowany przez enzymy zwane kinazami GRK. Gdy GRK są zbyt aktywne, co obserwuje się w niewydolności serca i niektórych nowotworach, sygnalizacja ulega zakłóceniu. W tym badaniu opracowano praktyczne, oparte na komórkach testy, które mierzą, jak skutecznie eksperymentalne związki blokują konkretne izoformy GRK, pomagając naukowcom projektować inteligentniejsze leki, precyzyjnie regulujące te kluczowe „pokrętła głośności” komórek.
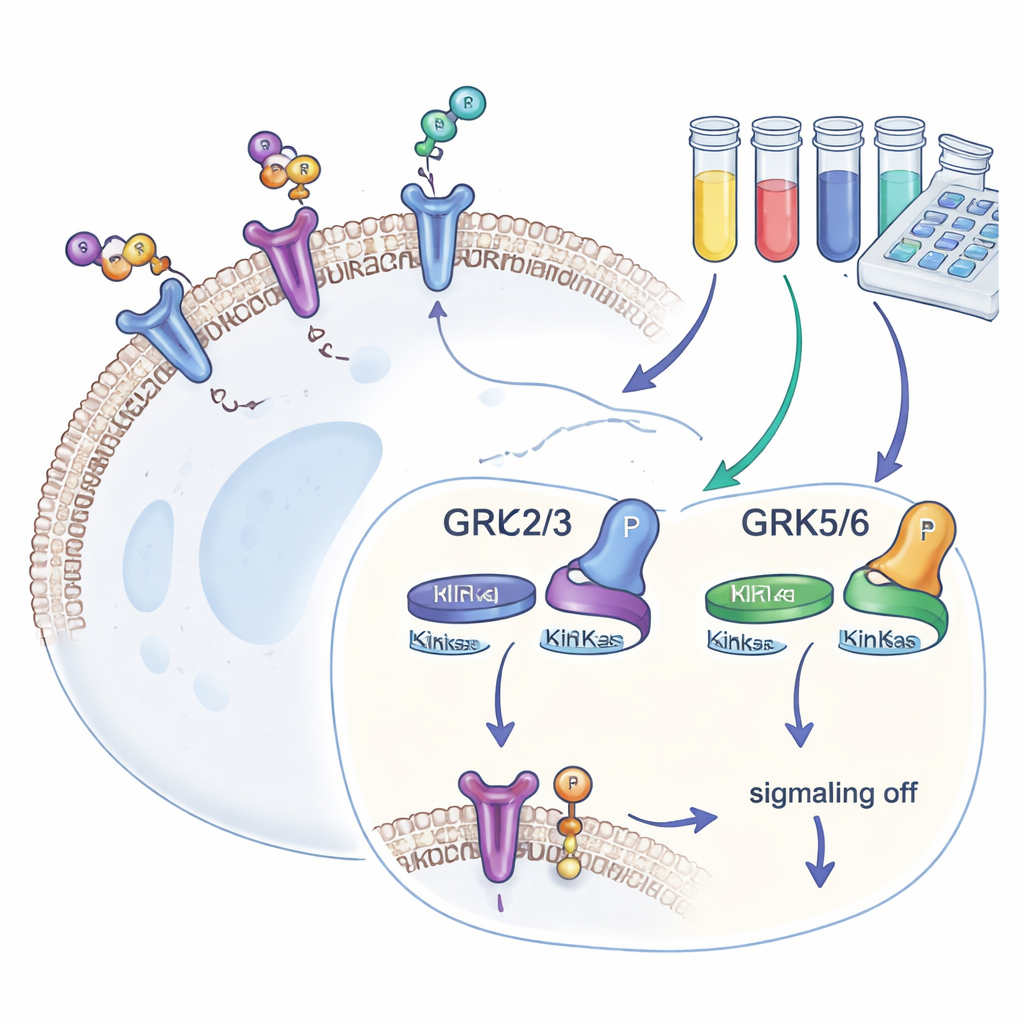
Bramkarze na powierzchni komórki
Nasze komórki mają setki typów receptorów sprzężonych z białkiem G (GPCR), które wykrywają sygnały z zewnątrz i przekładają je na odpowiedzi wewnętrzne. Po aktywacji GPCR, GRK przyłączają małe „flagi” fosforanowe do jego końcówki ogonowej. Te flagi przyciągają kolejne białko — beta‑arrestynę — które zatrzymuje dalszą sygnalizację i często powoduje internalizację receptora. Cztery izoformy GRK — GRK2, GRK3, GRK5 i GRK6 — występują w wielu tkankach. Ponieważ kształtują one siłę reakcji GPCR i ich poziomy zmieniają się w chorobach takich jak niewydolność serca, nowotwory czy uzależnienia, odkrywcy leków poszukują blokerów GRK, które są zarówno silne, jak i wybiórcze.
Budowanie przejrzystego pola testowego w komórkach
Większość wcześniejszych badań nad GRK bazowała na modelowaniu komputerowym lub chemii w probówce, co pokazuje, jak mocno inhibitor wiąże się z kinazą, ale nie jak działa w zatłoczonym wnętrzu żywej komórki. Aby wypełnić tę lukę, autorzy zmodyfikowali ludzkie komórki HEK293 tak, by brakowało w nich wszystkich czterech powszechnych GRK, a następnie ponownie wprowadzili po jednej izoformie GRK na raz. Każda linia komórkowa miała też znakowany, dobrze poznany receptor — receptor beta‑2 adrenergiczny — tak, by jego fosforylacja w określonym miejscu na ogonie (oznaczonym jako T360/S364) mogła być odczytana za pomocą czułego testu opartego na przeciwciałach. Ponieważ to miejsce jest modyfikowane tylko przez GRK, ilość obecnego fosforanu służy jako bezpośredni, ilościowy wskaźnik aktywności danej izoformy GRK w żywych komórkach.
Oddzielanie dobrych, słabych i nieswoistych związków
Wykorzystując to zestaw narzędzi, zespół przetestował panel komercyjnie dostępnych blokerów GRK. Najpierw pogrupowano związki głównie celujące w GRK2 i GRK3 oraz inną grupę skierowaną na GRK5 i GRK6. Porównując, o ile każdy związek zmniejszał fosforylację receptora w komórkach wyrażających tylko jedną podtypową izoformę GRK, badacze mogli zmapować rzeczywistą wybiórczość. Jeden związek, oznaczony jako 8h, okazał się najsilniejszym inhibitorem GRK2/3, podczas gdy związek 18 wyróżniał się selektywnym hamowaniem GRK5/6. Niektóre powszechnie używane cząsteczki wykazały niewielki efekt przy testowanych dawkach, prawdopodobnie dlatego, że słabo wnikały do komórek, a bardzo silny inhibitor kowalencyjny zaburzał zdrowie komórek, przez co był nieodpowiedni do eksperymentów obrazowania.
Od chemicznych odcisków palców do zachowania receptorów
Aby wykazać, że te inhibitory wpływają nie tylko na pojedynczy testowy receptor, lecz na biologię GPCR bardziej ogólnie, autorzy zbadali kilka receptorów o istotnym znaczeniu medycznym, w tym receptor mu‑opioidowy i receptor wazopresyny V2. Mierzyli zarówno fosforylację, jak i internalizację receptorów przy użyciu mikroskopii. Samodzielne podanie 8h lub 18 częściowo zmniejszało fosforylację i przemieszczanie receptorów do wnętrza komórek dla wielu celów, lecz kombinacja 8h i 18 niemal całkowicie zapobiegała tym zmianom i utrzymywała receptory na powierzchni komórki. Dodatkowe eksperymenty śledzące rekrutację beta‑arrestyny potwierdziły, że te same związki mogą modulować sygnalizację przy innych receptorach regulowanych przez nakładające się zestawy GRK.
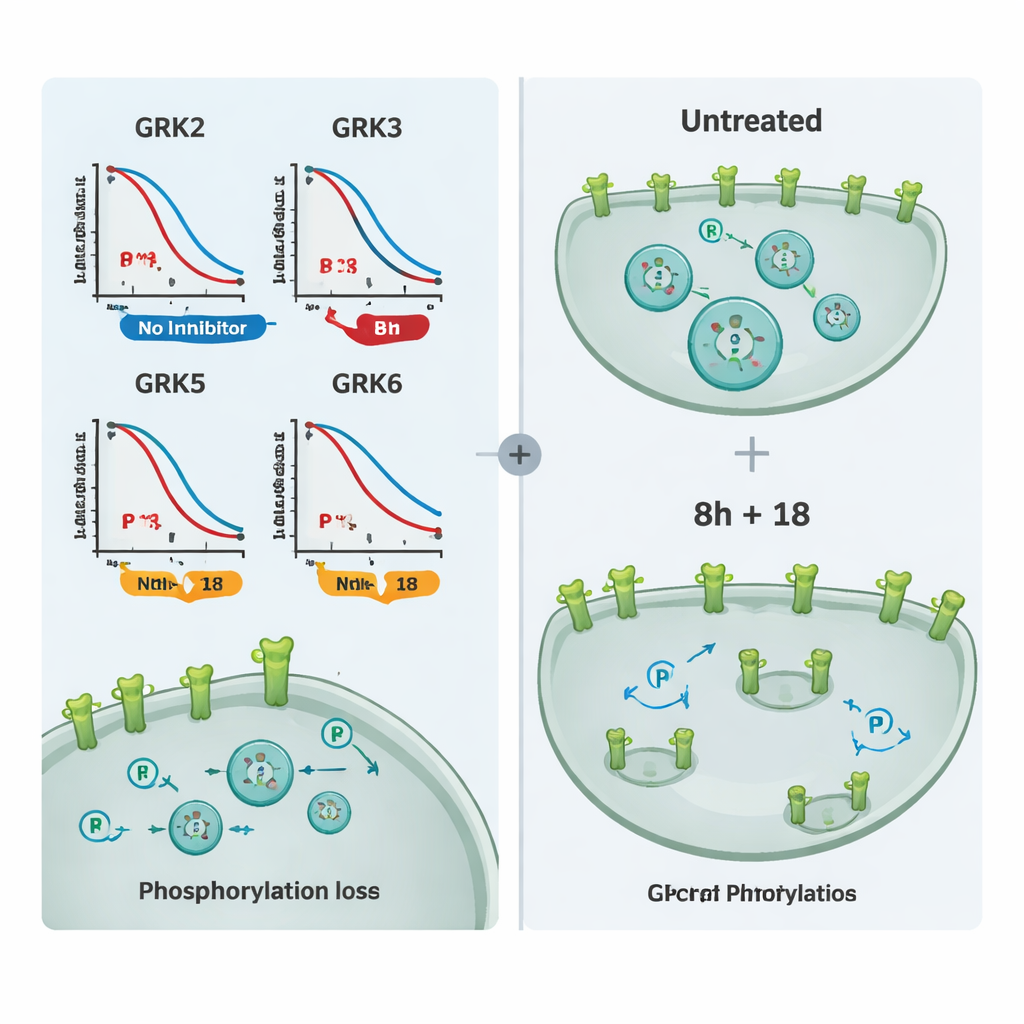
Co to oznacza dla przyszłych leków
Dla osób niebędących specjalistami kluczowy przekaz jest taki, że badanie dostarcza wiarygodny zestaw testów opartych na komórkach — oraz dwie szczególnie użyteczne narzędziowe cząsteczki, 8h i 18 — które pozwalają badaczom zobaczyć w żywych komórkach, jak dokładnie wyłącza się poszczególne izoformy GRK. Zamiast polegać na domysłach z uproszczonych danych z probówki, naukowcy mogą teraz zestawiać kandydatów obok siebie i decydować, czy oddziałują głównie na GRK2/3, GRK5/6, czy na wszystkie cztery jednocześnie. Ta przejrzystość powinna przyspieszyć rozwój leków, które precyzyjniej modulują sygnalizację GPCR, z potencjalnymi korzyściami w leczeniu chorób serca, nowotworów, zaburzeń bólowych i innych schorzeń związanych z zaburzeniem równowagi sygnalizacji.
Cytowanie: Blum, N.K., Kiefer, M.C., Decker, A. et al. Cell-based and isoform-selective G protein-coupled receptor kinase assays for comprehensive inhibitor evaluation. Commun Biol 9, 287 (2026). https://doi.org/10.1038/s42003-026-09568-0
Słowa kluczowe: sygnalizacja GPCR, inhibitory GRK, receptor beta‑adrenergiczny, test oparty na komórkach, odkrywanie leków