Clear Sky Science · pl
HBP1 zwiększa aktywność receptora progesteronu i ekspresję IGFBP1 napędzając decidualizację endometrium
Dlaczego ma to znaczenie dla płodności
Gdy zaczyna się ciąża, zarodek może się zagnieździć w macicy tylko wtedy, gdy błona śluzowa macicy przeszła kluczową przemianę zwaną decidualizacją. Wiele przypadków niepłodności i powtarzających się niepowodzeń transferu zarodka pozostaje niewyjaśnionych, a rosnące dowody sugerują, że problem leży w tej przemianie, a nie w samym zarodku. W badaniu odkryto wcześniej niedoceniany molekularny „przełącznik”, czynnik transkrypcyjny o nazwie HBP1, który pomaga przygotować błonę śluzową do implantacji i może dawać nowe możliwości diagnostyki i leczenia zaburzeń implantacji.
Ukryty przełącznik w błonie śluzowej macicy
Wewnętrzna wyściółka macicy, endometrium, zmienia się rytmicznie w każdym cyklu miesiączkowym. Pod wpływem estrogenu rośnie, a pod wpływem progesteronu dojrzewa, stając się przyjaznym podłożem dla zarodka. W tej pracy badacze skupili się na ludzkich komórkach zrębu endometrium — komórkach strukturalnych, które przekształcają się w większe, bardziej sekrecyjne komórki decidualne w czasie implantacji. Przeszukując istniejące dane o aktywności genów i przeprowadzając nowe eksperymenty, stwierdzili, że poziomy HBP1 gwałtownie rosną, gdy komórki zrębu zaczynają decidualizować, co sugeruje, że HBP1 jest częścią wbudowanego systemu czasowego przygotowującego macicę.
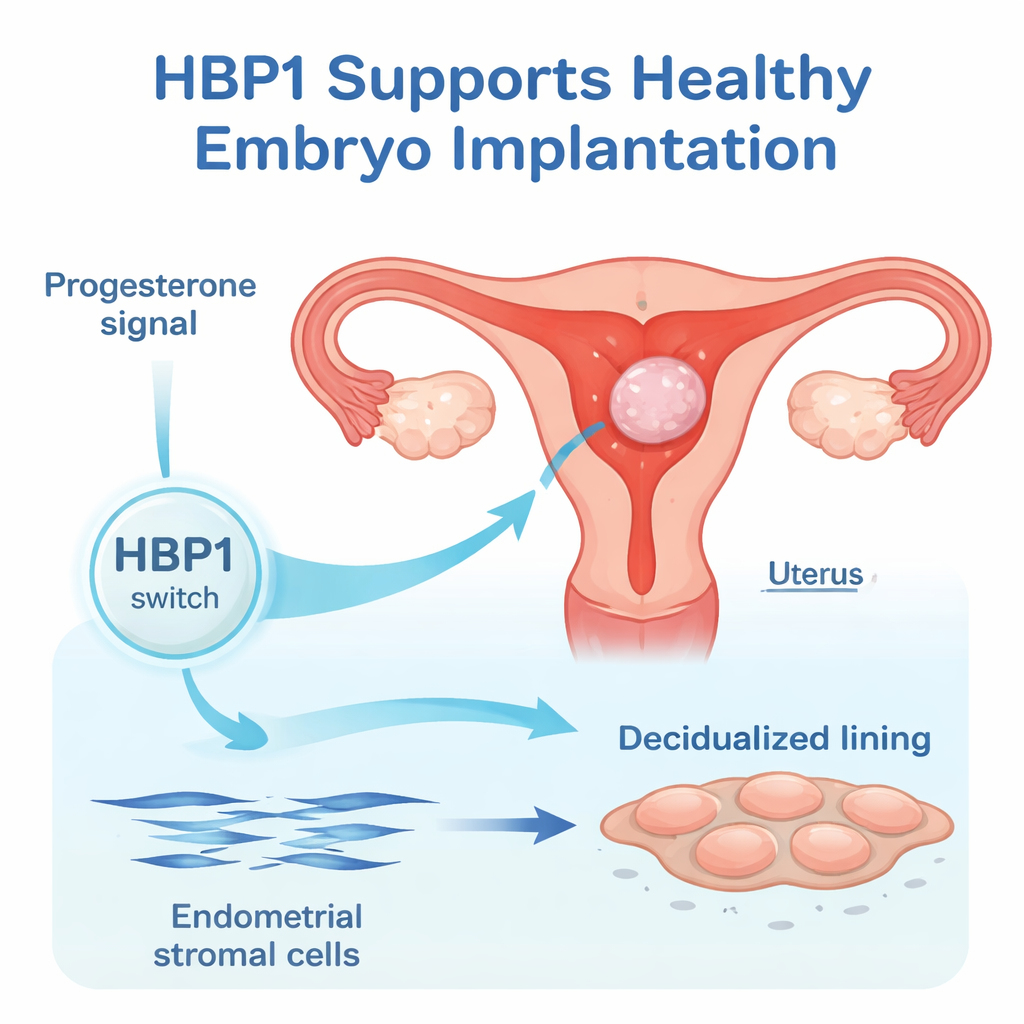
Pomoc w zmianie kształtu komórek i hamowaniu podziałów
Aby sprawdzić, czy HBP1 jest tylko obecny, czy rzeczywiście niezbędny, zespół regulował jego poziomy w hodowanych ludzkich komórkach zrębu endometrium. Gdy HBP1 został zmniejszony, klasyczne markery decidualizacji, takie jak IGFBP1, FOXO1 i prolaktyna, spadły zarówno na poziomie RNA, jak i białka. Komórki nie przechodziły też typowej zmiany kształtu — ze smukłych, wrzecionowatych do szerszych, wielokątnych — zamiast tego nadal intensywnie się dzieliły. Gdy zwiększono HBP1, poziomy IGFBP1 wzrosły, a podziały komórkowe zwolniły. Te wyniki łącznie pokazują, że HBP1 pomaga komórkom wyjść z trybu wzrostu i wejść w wyspecjalizowany stan decidualny wspierający wczesną ciążę.
Dostrajanie sygnałów hormonalnych wewnątrz komórki
Progesteron i jego receptor są kluczowe dla przygotowania macicy, ale nie wszystkie tkanki reagują równie dobrze na ten hormon. Badacze odkryli, że sama sygnalizacja progesteronowa zwiększa poziomy HBP1, tworząc pętlę dodatniego sprzężenia zwrotnego. Co ciekawe, obniżenie HBP1 nie zmieniało ilości receptora progesteronu wytwarzanego przez komórki, ale osłabiało aktywność istotnych genów zależnych od progesteronu, w tym FKBP4, FKBP5, FOSL2 oraz kofaktora SRC1. Przy użyciu podejść analizy całego genomu wykazali, że HBP1 wiąże się w pobliżu wielu z tych genów i jest związany ze wzrostem specyficznej modyfikacji histonu, H3K4me3, która oznacza aktywne fragmenty DNA. W istocie HBP1 nie włącza ani nie wyłącza receptora; ułatwia odczytanie genów będących celem receptora.
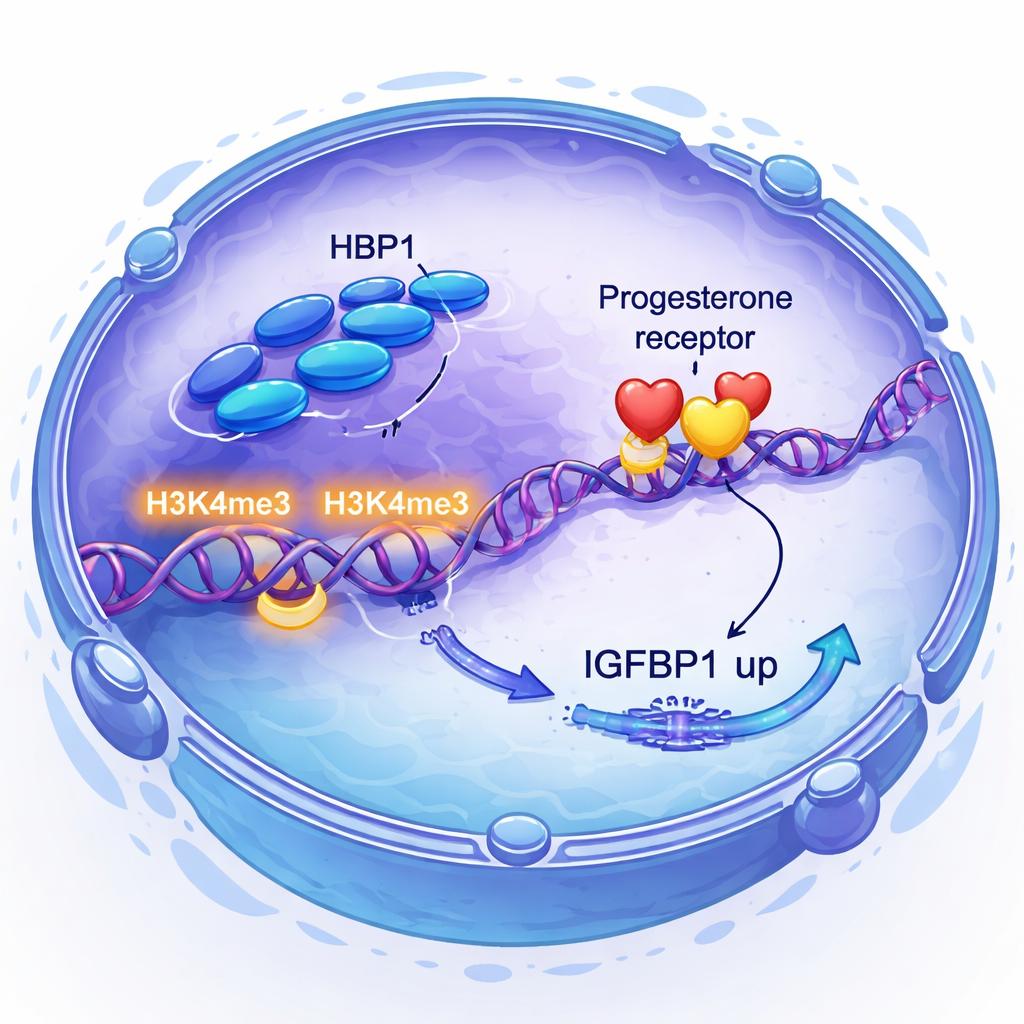
Bezpośrednia kontrola kluczowego sygnału implantacji
Zespół następnie zbadał, jak HBP1 łączy się z IGFBP1 — białkiem od dawna używanym jako marker prawidłowej decidualizacji i znanym z wpływu na komunikację między zarodkiem a macicą. Łącząc sekwencjonowanie RNA z sekwencjonowaniem immunoprecypitacji chromatyny, wykazali, że HBP1 siedzi bezpośrednio na regionie promotora IGFBP1 i zwiększa tam poziom H3K4me3, co napędza wyższą produkcję IGFBP1. Stwierdzili też, że obniżenie HBP1 aktywuje szlak PI3K–AKT, sygnał związany ze wzrostem, który przy nadmiernej aktywności tłumi IGFBP1. Zablokowanie tego szlaku przywracało poziomy IGFBP1. Tak więc HBP1 wspiera decidualizację na dwa sposoby: bezpośrednio włączając IGFBP1 i tłumiąc sygnał wzrostowy, który w przeciwnym razie blokowałby geny decidualne.
Powiązanie defektu molekularnego z nieudaną implantacją
Na koniec badacze zbadali próbki endometrium od kobiet z nawracającą niepowodzeniem implantacji i porównali je z tkankami od płodnych kontrolnych w fazie środkowo-sekretorycznej, gotowej do implantacji. Kobiety z powtarzającymi się niepowodzeniami miały wyraźnie niższe poziomy HBP1 i jego późniejszych partnerów IGFBP1, FKBP5 i FOSL2, choć poziomy receptora progesteronu były podobne w obu grupach. Ten wzorzec pasuje do koncepcji „oporności na progesteron” — hormon jest obecny, ale tkanka nie potrafi w pełni odpowiedzieć, ponieważ brakuje kluczowych czynników wspierających, takich jak HBP1.
Co to oznacza dla pacjentek
Mówiąc w przystępny sposób, badanie sugeruje, że HBP1 działa jak główne ustawienie na panelu sterowania wyściółki macicy. Gdy jest prawidłowo włączony, umożliwia usłyszenie sygnałów progesteronu, zachęca komórki do zaprzestania podziałów i wyspecjalizowania się oraz zwiększa produkcję cząsteczek sprzyjających implantacji, takich jak IGFBP1. Gdy HBP1 jest zbyt niski, wyściółka może wyglądać normalnie pod mikroskopem, ale działać słabo, co prowadzi do sytuacji, w której zarodki nie są w stanie się zakotwiczyć. Zrozumienie i oznaczanie HBP1 oraz jego sieci może w przyszłości pomóc lekarzom zidentyfikować kobiety zagrożone problemami z implantacją i zainspirować nowe terapie przywracające podatność macicy.
Cytowanie: Guo, Y., Tian, W., Nie, C. et al. HBP1 enhances progesterone receptor activity and IGFBP1 expression driving endometrial decidualization. Commun Biol 9, 286 (2026). https://doi.org/10.1038/s42003-026-09567-1
Słowa kluczowe: decidualizacja endometrium, implantacja zarodka, sygnalizacja progesteronowa, niepłodność, HBP1